
����Ŀ������P(s)��Cl2(g)������Ӧ����PCl3(g)��PCl5(g)����Ӧ���̺�������ϵ��ͼ��ʾ��ͼ�еġ�H��ʾ����1mol��������ݣ���
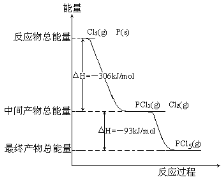
������ͼ�ش��������⣺
��1��P��Cl2��Ӧ����PCl3���Ȼ�ѧ����ʽ___��
��2��PCl5�ֽ��PCl3��Cl2���Ȼ�ѧ����ʽ___��
��3��P��Cl2��������Ӧ����1molPCl5�ġ�H3��__��P��Cl2һ����Ӧ����1molPCl5�ġ�H4___��H3 (����ڡ�����С�ڡ����ڡ�)��
��4��PCl5������ˮ��ַ�Ӧ���������������ᣬ��֪��Ӧǰ���Ԫ�ػ��ϼ۲��䣬�仯ѧ����ʽ��__��
���𰸡�P��s��+![]() Cl2��g���TPCl3��g����H=-306kJmol-1 PCl5��g���TPCl3��g��+Cl2��g����H=+93kJmol-1 -399kJmol-1 ���� PCl5+4H2O�TH3PO4+5HCl
Cl2��g���TPCl3��g����H=-306kJmol-1 PCl5��g���TPCl3��g��+Cl2��g����H=+93kJmol-1 -399kJmol-1 ���� PCl5+4H2O�TH3PO4+5HCl
��������
��1������ͼ��ó���Ӧ��������Լ���Ӧ��=�������������-��Ӧ�����������Ȼ��������д�Ȼ�ѧ����ʽ��ԭ����д��
��2������ͼ��ó���Ӧ��������Լ���Ӧ��=�������������-��Ӧ�����������Ȼ��������д�Ȼ�ѧ����ʽ��ԭ����д��
��3�����ݸ�˹���ɷ��������ݷ�Ӧ������������м������������Լ����ղ��������������ϻ�ѧ����ʽ�Լ��Ȼ�ѧ����ʽ����д�������ע���˹���ɵ�Ӧ�ã�
��4��PCl5������ˮ��ַ�Ӧ������������������ᡣ
��1������ͼʾ��֪��P��s��+![]() Cl2��g���TPCl3��g������Ӧ�����������������������������÷�Ӧ�Ƿ��ȷ�Ӧ����Ӧ����H=-306 kJ/mol�����Ȼ�ѧ����ʽΪ��P��s��+
Cl2��g���TPCl3��g������Ӧ�����������������������������÷�Ӧ�Ƿ��ȷ�Ӧ����Ӧ����H=-306 kJ/mol�����Ȼ�ѧ����ʽΪ��P��s��+![]() Cl2��g���TPCl3��g����H=-306 kJ/mol��
Cl2��g���TPCl3��g����H=-306 kJ/mol��
�ʴ�Ϊ��P��s��+![]() Cl2��g���TPCl3��g����H=-306kJmol-1��
Cl2��g���TPCl3��g����H=-306kJmol-1��
��2������ͼʾ��֪��Cl2��g��+PCl3��g���TPCl5��g�����м������������������ղ�������������÷�Ӧ�Ƿ��ȷ�Ӧ����H=������������-��Ӧ��������=-93 kJ/mol������PCl5��g���TPCl3��g��+Cl2��g�������ȷ�Ӧ���Ȼ�ѧ����ʽΪPCl5��g���TPCl3��g��+Cl2��g����H=+93 kJ/mol��
�ʴ�Ϊ��PCl5��g���TPCl3��g��+Cl2��g����H=+93kJmol-1��
��3������ͼ����д��������Ӧ���Ȼ�ѧ����ʽ��
P��s��+![]() Cl2��g���TPCl3��g����H1=-306 kJ/mol��
Cl2��g���TPCl3��g����H1=-306 kJ/mol��
Cl2��g��+PCl3��g���TPCl5��g����H2=-93 kJ/mol��
��P��Cl2������Ӧ����1molPCl5����H3=-306 kJ/mol+��-93 kJ/mol��=-399 kJ/mol��
��ͼ���֪��P��Cl2һ����Ӧ����1molPCl5����H4=-306kJ/mol+��-93kJ/mol��=-399kJ/mol�����ݸ�˹���ɿ�֪����Ӧ����һ����ɻ��Ƿֶಽ��ɣ�������ͬ�IJ����Ӧ����ȣ���P��Cl2һ����Ӧ����1molPCl5�ķ�Ӧ�ȵ���P��Cl2��������Ӧ����1molPCl5�ķ�Ӧ�ȣ�
�ʴ�Ϊ��-399kJmol-1�����ڣ�
��4��PCl5������ˮ��ַ�Ӧ���������������ᣬ��֪��Ӧǰ���Ԫ�ػ��ϼ۲��䣬��������Ϊ��������ᣬ��ԭ���غ��֪��ѧ����ʽΪPCl5+4H2O�TH3PO4+5HCl��
�ʴ�Ϊ��PCl5+4H2O�TH3PO4+5HCl��


 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д� �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ˮ��Һ�е�����ƽ������������ȷ����
A.��10mL0.1mol��L��1������뵽10mL0.1mol��L��1̼������Һ�У�c(Na��)��c(Cl��)��c(HCO![]() )��c(CO
)��c(CO![]() )
)
B.ij�¶���0.1mol��L��1�Ĵ���pHΪ3����ˮϡ��10������ϡ�ͺ����ҺpH����4
C.0.02mol��L��1HCN��Һ��0.02mol��L��1NaCN��Һ��������c(HCN)��c(CN��)��0.04mol��L��1
D.��0.01mol��L��1������Һ�м�ˮ��ϡ�ͺ���Һ��![]() ��ֵ������ϡ��������Һ�¶ȱ仯��
��ֵ������ϡ��������Һ�¶ȱ仯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���![]() ��Һ�ζ�
��Һ�ζ�![]() ��Һ��������ͼ��ʾ������˵���������
��Һ��������ͼ��ʾ������˵���������
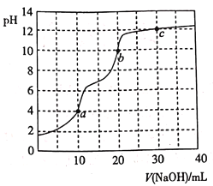
A.�ζ��յ�a��ѡ�������ָʾ��
B.c����Һ��![]()
C.b����Һ��![]()
D.a��b��c������ˮ�ĵ���̶�������c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�����Ϊ1L���ܱ������з���ij��ѧ��Ӧ��2A(g)![]() B(g)��C(g)�����ֲ�ͬ�����½��У�����ʵ�����800�棬ʵ�����950�棬B��C����ʼŨ�ȶ�Ϊ0����Ӧ��A��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ���Իش��������⣺
B(g)��C(g)�����ֲ�ͬ�����½��У�����ʵ�����800�棬ʵ�����950�棬B��C����ʼŨ�ȶ�Ϊ0����Ӧ��A��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ���Իش��������⣺
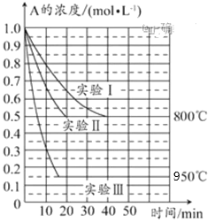
��1����ʵ����У���Ӧ��20��40min��A��ƽ����Ӧ����Ϊ__mol��L��1��min��1��ʵ����ʵ�����ȣ����������ķ�Ӧ������___��
��2���÷�Ӧ����H___0�����ж�������___��
��3��ʵ����40minĩ�������ͷ�Ӧ�¶ȣ��ﵽ�µ�ƽ���A��Ũ�Ȳ�����Ϊ___(�����)��
A��0.35mol��L��1 B��0.4mol��L��1 C��0.7mol��L��1 D��0.8mol��L��1
��4������Ӧ��800����У��ڸ�1L���ܱ������м���1molA��0.2molHe���ﵽƽ��ʱA��ת����Ӧ___��
A������86% B������50% C��С��50% D������50%��86%֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ������������ȡ��������(��Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3����������������)��ȡ��ˮ����������(FeSO4��7H2O)��������������̣�

����˵������ȷ���ǣ� ��
A. �ܽ�����ѡ���������ᣬ�Լ�Xѡ������
B. ����1��һ������SiO2������pH��Ϊ��ʹAl3+ת��ΪAl(OH)3���������2
C. ����Һ2�õ�FeSO4��7H2O��Ʒ�Ĺ����У������������ֹ�������ͷֽ�
D. ���ı䷽��������Һ1��ֱ�Ӽ�NaOH���������õ��ij����������ܽ⣬����Һ���ᾧ����Ҳ�ɵõ�FeSO4��7H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪![]() �Ƕ�Ԫ���ᣬ��������ijŨ�ȵIJ�����Һ����μ���KOH��Һ��������Һ��
�Ƕ�Ԫ���ᣬ��������ijŨ�ȵIJ�����Һ����μ���KOH��Һ��������Һ��![]() ��
��![]() ��
��![]() ����ɰٷ�����pH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����( )
����ɰٷ�����pH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����( )
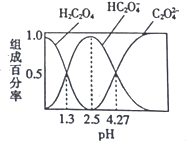
A.![]() ����Һ�У�
����Һ�У�![]()
B.��Ӧ![]() ��ƽ�ⳣ��Ϊ
��ƽ�ⳣ��Ϊ![]()
C.����Һ�м���KOH��Һ��pH��1.3����4.27�Ĺ�����ˮ�ĵ���̶���������С
D.![]() ����Һ�У�
����Һ�У�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.NO��һ�ֳ����������������о�������Ҫ�ļ�ֵ�����塣
��1��2NO(g)+O2(g)=2NO2(g) ��H=akJ/mol�ķ�Ӧ�����������仯��ϵ��ͼ��ʾ��
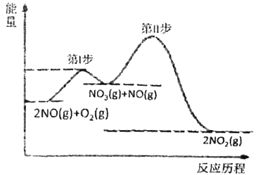
��a___0(���)
����֪���ڢ�ӦΪ��NO3(g)+NO(g)=2NO2(g) ��H=bkJ/mol
��I����Ӧ���Ȼ�ѧ����ʽΪ___��
��2������β���г�����NO��NH3�ڼ��Ⱥʹ������ڵ�������������NO����Ⱦ��
��֪��4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ��H=��905kJ/mol
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ��H=��1268kJ/mol
NH3��NO��Ӧ���Ȼ�ѧ����ʽΪ___��
��3����ҵ��NO����Ҫ��Դ��NH3��NH3Ҳ����Ϊȼ����Ƴɼ���ȼ�ϵ�أ��ڼ��������£�ȼ�ϵ�ز�����ҪΪN2��ȼ�ϵ�ظ����ĵ缫��ӦʽΪ___��������Ϊȼ�ϵĵ�غͺ�̼��������Ϊȼ�ϵĵ����ȣ���Ҫ���ŵ���___��
II.�������ƺͶ��ȷ�![]() �ķ�ˮ��ͨ������װ�ô�������ԭ����ͼ��ʾ��
�ķ�ˮ��ͨ������װ�ô�������ԭ����ͼ��ʾ��
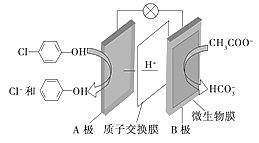
��1��д��HCO3-�ĵ���ʽ___���������к��еĻ�ѧ��������___��
��2����ص�������___����Һ��H+���ƶ�������___(��A��B��B��A)
��3��B�������ĵ缫��Ӧ����ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̼����������ָͨ��һ���ķ�������ҵ�����в�����CO2������������á��������NaOH��Һ��������CO2�������������ͼ��ʾ(��������������δ���)��
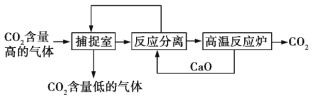
�����йظ÷�������������ȷ����
���ܺ�С�Ǹ÷�����һ���ŵ�
�����������У����������ʿ���ѭ������
������Ӧ�����������У��������ʵĻ��������ǹ��ˡ��������ᾧ
�ܸ÷����ɼ���̼�ŷţ�����������CO2���������Ʊ��״��Ȳ�Ʒ
A.�٢�B.�ڢ�C.�ۢ�D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��������ܱ������о�������Ӧ��C(s)��2H2O(g) ![]() CO2(g)��2H2(g)����H��0���й�ʵ���������±���ʾ��
CO2(g)��2H2(g)����H��0���й�ʵ���������±���ʾ��
���� | �ݻ�/L | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ƽ�ⳣ�� | |
C(s) | H2O(g) | H2(g) | |||||
�� | 2 | T1 | 2 | 4 | 3.2 | 3.5 | K1 |
�� | 1 | T2 | 1 | 2 | 1.2 | 3 | K2 |
����˵����ȷ����(����)
A.T1<T2B.�������У�����Ӧ���е�1.5 minʱ��n(H2O)��1.4 mol
C.���������ܶ�ʼ�ձ��ֲ���D.K2��1.35
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com