
科目: 来源: 题型:
【题目】有机合成是制药工业中的重要手段。G是某抗炎症药物的中间体,其合成路线如图:
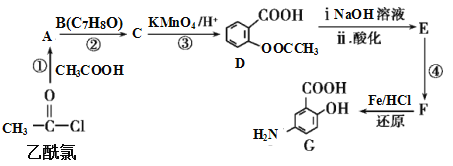
已知:
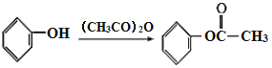 ,
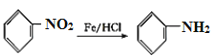
,
(1)B的结构简式为_____。
(2)反应④的条件为____;①的反应类型为___;反应②的作用是____。
(3)下列对有机物G的性质推测正确的是____(填选项字母)。
A.具有两性,既能与酸反应也能与碱反应
B.能发生消去反应、取代反应和氧化反应
C.能聚合成高分子化合物
D.1mol G与足量NaHCO3溶液反应放出2mol CO2
(4)D与足量的NaOH溶液反应的化学方程式为_____。
(5)符合下列条件的C的同分异构体有___种。
A.属于芳香族化合物,且含有两个甲基 B.能发生银镜反应 C.与FeCl3溶液发生显色反应
其中核磁共振氢谱有4组峰,且峰面积之比为6∶2∶1∶1的是___(写出其中一种的结构简式)。
(6)已知:苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位;苯环上有羧基时,新引入的取代基连在苯环的间位。根据题中的信息,写出以甲苯为原料合成有机物![]() 的流程图(无机试剂任选)。_______
的流程图(无机试剂任选)。_______
合成路线流程图示例如图:X![]() Y
Y![]() Z…目标产物
Z…目标产物
查看答案和解析>>
科目: 来源: 题型:
【题目】钨![]() 具有很大的工业价值,主要用于电子工业,合金添加剂等。工业上利用白钨矿精矿为原料
具有很大的工业价值,主要用于电子工业,合金添加剂等。工业上利用白钨矿精矿为原料![]() 主要成分为钨酸钙
主要成分为钨酸钙![]() ,还含有CaO、
,还含有CaO、![]() 等杂质
等杂质![]() 生产钨粉的一种工艺流程如下:
生产钨粉的一种工艺流程如下:
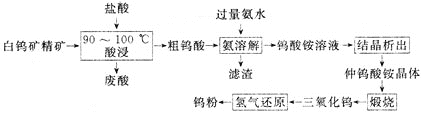
已知:
![]() 钨酸钙微溶于水,能溶解在热盐酸中。
钨酸钙微溶于水,能溶解在热盐酸中。
![]() 降低溶液pH可以从钨酸铵溶液中析出仲钨酸铵晶体,常温时可析出带11个结晶水的仲钨酸铵晶体,但是由于颗粒很细小,难以进一步提纯。在
降低溶液pH可以从钨酸铵溶液中析出仲钨酸铵晶体,常温时可析出带11个结晶水的仲钨酸铵晶体,但是由于颗粒很细小,难以进一步提纯。在![]() 时可析出颗粒较大的带5个结晶水的仲钨酸铵晶体,可进一步提纯精制。
时可析出颗粒较大的带5个结晶水的仲钨酸铵晶体,可进一步提纯精制。
![]() 酸浸时为了提高浸出率,可采取的措施有___________。
酸浸时为了提高浸出率,可采取的措施有___________。![]() 答出两条即可
答出两条即可![]()
![]() 酸浸时,需控制反应温度在
酸浸时,需控制反应温度在![]() 之间的原因是________。
之间的原因是________。
![]() 酸浸时发生的主要反应的化学方程式是____。
酸浸时发生的主要反应的化学方程式是____。
![]() 将废酸与粗钨酸分离的操作是_____
将废酸与粗钨酸分离的操作是_____![]() 填操作名称
填操作名称![]() 。
。
![]() 加入过量氨水后过滤,得到滤渣的主要成分是______
加入过量氨水后过滤,得到滤渣的主要成分是______![]() 填化学式
填化学式![]() 。
。
![]() 工艺流程中“结晶析出”,采用的结晶方法是________。
工艺流程中“结晶析出”,采用的结晶方法是________。
![]() 仲钨酸铵的化学式为
仲钨酸铵的化学式为![]() ,写出仲钨酸铵煅烧转化为
,写出仲钨酸铵煅烧转化为![]() 的化学方程式_______________。
的化学方程式_______________。
![]() 已知白钨矿精矿中的钨酸钙质量分数为
已知白钨矿精矿中的钨酸钙质量分数为![]() ,
,![]() 该精矿经上述流程制得
该精矿经上述流程制得![]() 钨粉。则该生产中钨的产率为_______
钨粉。则该生产中钨的产率为_______![]() 用含“a”“w”“m”的代数式表示
用含“a”“w”“m”的代数式表示![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一密闭容器中充入1 mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g) ![]() 2HI(g)
2HI(g)
(1)保持容器容积不变,向其中充入1 mol H2,反应速率_____(填“增大”、“减小”或“不变”,下同)。
(2)升高温度,反应速率_____。
(3)扩大容器体积,反应速率_____。
(4)保持容器内气体压强不变,向其中充入1 mol H2(g)和1 mol I2(g),反应速率_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚砜(SOCl2)常用于医药、农药、染料工业,也可在有机合成工业中作氯化剂。已知:SOCl2的相关性质如下表所示:
颜色、状态 | 熔点 | 沸点 | 腐蚀性 | 水解 |
无色或微黄液体 | -105℃ | 78℃ | 强 | 极易水解 |
现利用如图装置制备SOCl2。
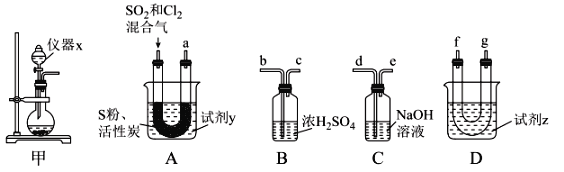
请回答下列问题:
Ⅰ.制备SO2和Cl2。
(1)本实验选用装置甲制备SO2和Cl2,装置甲中仪器x的名称为___;若以KMnO4和浓盐酸反应制备Cl2,反应的离子方程式为___。
Ⅱ.制备SOCl2。
以活性炭作为催化剂,SO2和C12可以和S粉在180~200℃时反应合成SOCl2,选用装置A、B、C、D进行制备(夹持、加热装置略去)。
(2)按气流从左到右的方向,装置A、B、C、D的连接顺序为____(填仪器接口的字母编号)。
(3)试剂y为___(填选项字母,下同);试剂z为___。
A.热水 B.乙醇 C.石蜡油 D.冰水
(4)装置A中U形管内发生反应的化学方程式为___。
(5)装置C的作用为___;若装置A处通入的SO2和Cl2的物质的量之比为1:3,则装置C中生成的盐为___(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在2A+B![]() 3C+4D(A、B、C、D均是气体)反应中,表示该反应速率最快的是
3C+4D(A、B、C、D均是气体)反应中,表示该反应速率最快的是
A.υ(A)= 0.5 mol/(Ls)B.υ(B)= 0.3 mol/(Ls)
C.υ(C)= 0.8 mol/(Ls)D.υ(D)= 1 mol/(Ls)
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物G是合成某种耐热聚合物的单体,其合成方法如下:
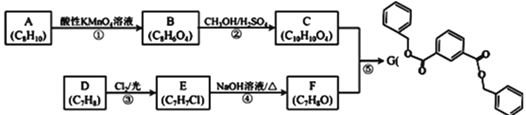
已知:R1COOR2+R3OH![]() R1COOR3+R2OH
R1COOR3+R2OH
![]() 中含氧官能团的名称是 ______ ,F的名称是 ______ 。
中含氧官能团的名称是 ______ ,F的名称是 ______ 。
![]() 上述流程中的取代反应除
上述流程中的取代反应除![]() 、
、![]() 外还有 ______
外还有 ______ ![]() 填序号
填序号![]() ,化合物E的核磁共振氢谱图中共有 ______ 个吸收峰,峰面积比为 ______ 。
,化合物E的核磁共振氢谱图中共有 ______ 个吸收峰,峰面积比为 ______ 。
![]() 按下列合成路线可得到F的同分异构体H,则可鉴别H与F的试剂是 ______ 。
按下列合成路线可得到F的同分异构体H,则可鉴别H与F的试剂是 ______ 。
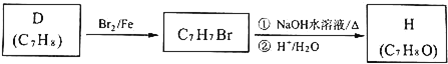
![]() 与NaOH溶液反应的化学方程式为 ______ 。
与NaOH溶液反应的化学方程式为 ______ 。
![]() 的同分异构体K具有如下性质:
的同分异构体K具有如下性质:![]() 能与NaOH溶液反应,且1molK完全反应消耗4molNaOH
能与NaOH溶液反应,且1molK完全反应消耗4molNaOH![]() 能发生银镜反应,且1molK与足量的银氨溶液反应生成4molAg
能发生银镜反应,且1molK与足量的银氨溶液反应生成4molAg![]() 分子中苯环上的一氯取代物只有一种。则K的结构简式为 ______ 。
分子中苯环上的一氯取代物只有一种。则K的结构简式为 ______ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知热化学方程式SO2(g)+1/2O2(g)![]() SO3(g) △H=-98.32kJ·mol-1,在容器中充入2mol SO2和1mol O2充分反应,最终放出的热量
SO3(g) △H=-98.32kJ·mol-1,在容器中充入2mol SO2和1mol O2充分反应,最终放出的热量
A. 等于196.64kJ B. 等于196.64kJ·mol-1
C. 小于196.64kJ D. 大于196.64kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】硼及其化合物在工农业生产中具有广泛应用。
请回答下列问题:
(1)基态B原子的价电子排布图___,B属于元素周期表中的___区元素。
(2)NaBO2可用于织物漂白。
①第二周期中第一电离能介于B和O之间的元素为___(填元素符号)。
②BO2-的空间构型为____,写出两种与其互为等电子体的分子的化学式:____。
(3)BF3和F-可以形成BF4-,BF3和BF4-中B原子的杂化方式分别为_____、____。
(4)立方BN和立方AlN均为原子晶体,结构相似,BN的熔点高于AlN的原因为______。
(5)一种新型轻质储氢材料的晶胞结构如图所示:
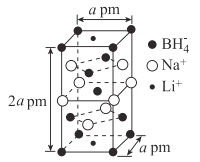
①该化合物的化学式为____。
②设阿伏加德罗常数的值为NA,该晶体的密度为___g·cm-3(用含a、NA的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙烯的分子式为C2H4,是一种重要的化工原料和清洁能源,研究乙烯的制备和综合利用具有重要意义。请回答下列问题:
(1)乙烯的制备:工业上常利用反应C2H6(g)=C2H4(g)+H2(g)△H制备乙烯。
已知:Ⅰ.C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) △H1=-1556.8kJ·mol-1;
Ⅱ.H2(g)+![]() O2(g)=H2O(1) △H2=-285.5kJ·mol-1;
O2(g)=H2O(1) △H2=-285.5kJ·mol-1;
Ⅲ.C2H6(g)+![]() O2(g)=2CO2(g)+3H2O(l) △H3= -1559.9kJ·mol-1。
O2(g)=2CO2(g)+3H2O(l) △H3= -1559.9kJ·mol-1。
则△H=___kJ·mol-1。
(2)乙烯可用于制备乙醇:C2H4(g)+H2O(g)=C2H5OH(g)。向某恒容密闭容器中充入amolC2H4(g)和amol H2O(g),测得C2H4(g)的平衡转化率与温度的关系如图所示:
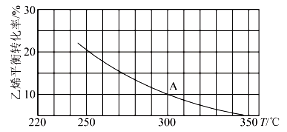
①该反应为___热反应(填“吸”或“放”)。
②A点时容器中气体的总物质的量为___。已知分压=总压×气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数(KP),测得300℃时,反应达到平衡时该容器内的压强为bMPa,则A点对应温度下的KP=___MPa-1(用含b的分数表示)。
③已知:C2H4(g)+H2O(g)=C2H5OH(g)的反应速率表达式为v正=k正c(C2H4)·c(H2O),v逆=k逆c(C2H5OH),其中,k正、k逆为速率常数,只与温度有关。则在温度从250℃升高到340℃的过程中,下列推断合理的是___(填选项字母)。
A.k正增大,k逆减小 B.k正减小,k逆增大
C.k正增大的倍数大于k逆 D.k正增大的倍数小于k逆
④若保持其他条件不变,将容器改为恒压密闭容器,则300℃时,C2H4(g)的平衡转化率___10%(填“>”“<”或“=”)。
(3)乙烯可以被氧化为乙醛(CH3CHO),电解乙醛的酸性水溶液可以制备出乙醇和乙酸,则生成乙酸的电极为____极(填“阴”或“阳”),对应的电极反应式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知H2(g)+Cl2(g)=2HCl(g) ΔH= -184.6kJ/mol,则![]() H2(g)+
H2(g)+![]() Cl2(g)=HCl(g)的ΔH为( )
Cl2(g)=HCl(g)的ΔH为( )
A.+184.6kJ/molB.-92.3kJ/molC.-369.2kJ/molD.+92.3kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com