
科目: 来源: 题型:
【题目】草酸亚铁(FeC2O4)可作为生产电池正极材料磷酸铁锂的原料,受热容易分解,为探究草酸亚铁的热分解产物,按下面所示装置进行实验。
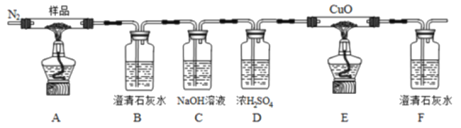
下列说法不正确的是
A.实验中观察到装置B、F中石灰水变浑浊,E中固体变为红色,则证明分解产物中有CO2和CO
B.反应结束后,取A中固体溶于稀硫酸,向其中滴加1~2滴KSCN溶液,溶液无颜色变化,证明分解产物中不含Fe2O3
C.装置C的作用是除去混合气中的CO2
D.反应结束后,应熄灭A,E处酒精灯后,持续通入N2直至温度恢复至室温
查看答案和解析>>
科目: 来源: 题型:
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是( )

A. 燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH-
B. a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C. a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D. a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
科目: 来源: 题型:
【题目】高分子化合物H的合成路线如下:

已知:i. 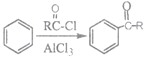
ii. 
回答下列问题
(1)A的化学名称为___________。
(2)B→C的化学方程式为______________________。
(3)E的结构简式为___________;由E生成F的反应类型为______________________。
(4)G中官能团名称为___________;由G→H的化学方程式为______________________。
(5)芳香族化合物L与G的官能团相同,但L的相对分子质量比G小28。则符合下列条件的L的同分异构体有___________种。
①与FeCl3溶液发生显色反应 ②苯环上有3个取代基
(6)按 有机合成路线可以制备
有机合成路线可以制备 。结合题中流程和已知信息,可推知M、N的结构简式分别为___________、___________。
。结合题中流程和已知信息,可推知M、N的结构简式分别为___________、___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A.![]() 与氢气完全反应后,生成2,2,
与氢气完全反应后,生成2,2,![]() 三甲基戊烷
三甲基戊烷
B.工业上由乙烯制乙醇、苯制环己烷均属于加成反应
C.![]() 的同分异构体共有3种
的同分异构体共有3种
D.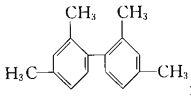 分子中所有碳原子一定在同一平面上
分子中所有碳原子一定在同一平面上
查看答案和解析>>
科目: 来源: 题型:
【题目】将Mg、Cu组成的3.96g混合物投入适量稀硝酸中恰好反应,固体完全溶解时,得到唯一的还原产物NO气体1.344L(标准状况),向反应后溶液中加入2molL-1NaOH溶液至金属离子恰好沉淀完全.则消耗的NaOH溶液的体积为( )
A.60mLB.90mLC.120mLD.150mL
查看答案和解析>>
科目: 来源: 题型:
【题目】有一固体混合物,可能由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 混合而成,为检验它的成分,做了如下实验:
混合而成,为检验它的成分,做了如下实验:![]() 已知
已知![]() 不能被稀
不能被稀![]() 氧化,
氧化,![]() 微溶于水
微溶于水![]()
![]() 将固体溶于足量水,搅拌后静置,得到无色透明溶液和白色沉淀;
将固体溶于足量水,搅拌后静置,得到无色透明溶液和白色沉淀;
![]() 取等量固体加入足量的稀硝酸中,有刺激性气味黄绿色气体产生,同时有白色沉淀生成。根据以上实验现象,你认为以下判断正确的是
取等量固体加入足量的稀硝酸中,有刺激性气味黄绿色气体产生,同时有白色沉淀生成。根据以上实验现象,你认为以下判断正确的是![]()
![]()
A.一定含有![]() 、
、![]() 、
、![]()
B.无法判断是否含有![]()
C.一定含有![]() 、
、![]() 、
、![]() ,不能肯定是否含有
,不能肯定是否含有![]()
D.是否含![]() ,只要把实验
,只要把实验![]() 产生的气体通入少量澄清石灰水中,若没有变浑浊,则一定不含
产生的气体通入少量澄清石灰水中,若没有变浑浊,则一定不含![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列溶液中的微粒浓度关系不正确的是
A. pH=8.3的某酸式盐NaHB的水溶液中:c (Na+) > c (HB-) > c (H2B) > c (B2-)
B. 等物质的量浓度的Na2S和NaHS溶液中:c (Na+)=2c (S2-) + c (HS-)
C. NH4HSO4溶液中滴加NaOH溶液至恰好呈中性:c (Na+) > c (SO42-) > c (NH4+) > c (OH-)=c (H+)
D. 0.1 mol / L NaH2PO4溶液中:c (Na+)=c (PO43-) + c (HPO42-) + c (H2PO4-) + c (H3PO4)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
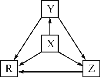
选项 | X | Y | Z | R |
A | Al | AlCl3 | Al(OH)3 | NaAlO2 |
B | Na | Na2O | Na2O2 | NaOH |
C | H2S | S | SO2 | SO3 |
D | N2 | NH3 | NO | NO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A. 3.2g铜溶于过量的浓硝酸完全反应生成的气体的物质的量一定为0.1mol
B. 78gNa2S和Na2O2的混合物中阳离子与阴离子的个数比不能确定
C. 25℃HCN的电离平衡常数为5.0×10-10,则浓度均为0.10mol·L-1NaCN和HCN的混合溶液中有c(Na+)>c(CN-)>c(OH-) >c(H+)
D. Fe(NO3)2溶液中加入过量的HI溶液:Fe2++NO3-+4H++2I-=I2+Fe3++NO↑+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Z、Q、R、T为前四周期元素,且原子序数依次增大。X和Q属同族元素,X和R可形成化合物XR4;R2为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;T2+的3d 轨道中有5个电子。请回答下列问题:
(1)Z基态原子的电子排布式是______;Z所在周期元素中,最高价氧化物对应的水化物酸性最强的是______(填化学式)。
(2)利用价层电子对互斥理论判断 RZ3-的立体构型是______;RZ3-的中心原子的杂化轨道类型为______。
(3)水中T含量超标,容易使洁具和衣物染色.RZ2可以用来除去水中超标的T2+,生成黑色沉淀TZ2,当消耗0.2molRZ2时,共转移了1mol电子,则反应的离子方程式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com