
科目: 来源: 题型:
【题目】去年下半年我省雾霾天气十分严重。PM2.5细颗粒物含有的毒性物质来源之一是汽车尾气排放。通过排气管加装催化装置,可有效减少CO和NO的排放,催化装置内发生的反应为:NOx+CO→N2+CO2,下列关于此反应的说法中,不正确的是
A.所涉及元素的第一电离能:N>O>C
B.当x=2时,每生成1molN2,转移电子数为4mol
C.等物质的量N2和CO2中,![]() 键的个数比为1:1
键的个数比为1:1
D.氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价
查看答案和解析>>
科目: 来源: 题型:
【题目】已知NO2和N2O4可以相互转化:![]()
![]() 。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如下图。
。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如下图。

(1)图中共有两条曲线X和Y,其中曲线________表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是________。下列不能说明该反应已达到平衡状态的是________。
A. 容器内混合气体的压强不随时间变化而改变
B. 容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D. 容器内混合气体的平均分子量不随时间变化而改变
(2)反应25 min时,若只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是____________________________________ (用文字表达);
(3)若要准确测定NO2相对分子质量,应采取的有效措施是_________ (填字母序号)
A.升高温度,降低压强 B.降低温度,升高压强
C.降低温度,降低压强 D.升高温度,升高压强
(4)根据图像,计算反应![]() 在该温度下的平衡常数K=________
在该温度下的平衡常数K=________
(5)现用3.2gCu与足量的浓HNO3反应,制得1.68 L N2O4和NO2的混合气体(体积以标况折算),则含有NO2的物质的量为____ ,化学反应__________ (填向逆方向进行、向正方向进行、已达平衡)(温度不变)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,A为电源,B为浸透饱和食盐水和酚酞的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。

(1)闭合K1 ,断开K2 ,通电后,d端显红色,则电源a端为______极,若c、d为惰性电极,c端的电极反应是____________________________________
检验c端产物的方法_______________________________________________
高锰酸钾液滴现象__________________________________________________
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3 ,且均为0.1 mol,断开K1,闭合K2,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+ 氧化能力由大到小的顺序是_______;

(3)D装置中反应的方程式 ___________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】某混合物浆液含Al(OH)3、MnO2和少量Na2Cr2O4。考虑到胶体的吸附作用使Na2Cr2O4不易完全被水浸出,某研究小组利用设计的电解分离装置(如图1),使浆液分离成固体混合物和含铬元素溶液,并回收利用。

固体混合物的分离和利用的流程图如图2所示(流程图中的部分分离操作和反应条件未标明):

(1)反应①所加试剂NaOH的电子式为___,B→C的反应条件为___,C→Al的制备方法称为___。
(2)该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化;加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有___(填序号)。
a.温度 b.Cl-的浓度 c.溶液的酸度
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化铁是一种重要的无机材料,化学性质稳定,催化活性高,具有良好的耐光性、耐热性和对紫外线的屏蔽性,从某种工业酸性废液(主要含Na+、Fe2+、Fe3+、Mg2+、Al3+、Cl-、![]() )中回收氧化铁流程如图所示:
)中回收氧化铁流程如图所示:

已知:常温下Ksp[Mg(OH)2]=1.2×10-11;Ksp[Fe(OH)2]=2.2×10-16;Ksp[Fe(OH)3]=3.5×10-38;Ksp[Al(OH)3]=1.0×10-33
(1)写出在该酸性废液中通入空气时发生反应的离子方程式: _________,指出使用空气比使用氯气好的原因是__________。
(2)已知Fe3+(aq)+3OH-(aq)=Fe(OH)3(s) ΔH=-Q1 kJ·mol-1,题(1)中每生成1 mol含铁微粒时,放热Q2,请你计算1 mol Fe2+全部转化为Fe(OH)3(s)的热效应ΔH=________。
(3)常温下,根据已知条件计算在pH=5的溶液中,理论上Fe3+在该溶液中可存在的最大浓度c(Fe3+)=____________。
(4)有人用氨水调节溶液pH,在pH=5时将Fe(OH)3沉淀出来,此时可能混有的杂质是________(填化学式,下同),用________试剂可将其除去。
查看答案和解析>>
科目: 来源: 题型:
【题目】依据甲、乙、丙三个图回答下列问题:

(1)①甲装置中,锌为_____极,锌电极上电极反应式为________________
②乙装置中,锌为_____极,锌电极上电极反应式为________________
(2)丙装置中,Cu2+浓度________(填“增大”“减小”或“不变”),原因是_______________________________________________________________________
(3)在25 ℃时,用石墨电极电解2.0 L 0.5 mol·L-1CuSO4溶液。5 min后,在一个石墨电极上有6.4 g Cu生成。试回答下列问题:
若电解后溶液的体积不变,则电解后溶液的[H+]为___________。
若将溶液恢复到与电解前一样,则需加入_____mol的______。
查看答案和解析>>
科目: 来源: 题型:
【题目】关于反应过程中的先后顺序,下列评价正确的是
A.向浓度都为0.1mol/L的FeCl3和CuCl2加入铁粉,溶质CuCl2首先与铁粉反应
B.向过量的Ba(OH)2溶液中滴加少量的KAl(SO4)2溶液,开始没有白色沉淀生成
C.向浓度都为0.1mol/L 的Na2CO3和NaOH的混合溶液通入CO2气体,NaOH首先反应
D.向浓度为0.1mol/L的FeCl3溶液中,加入质量相同、颗粒大小相同的铁和铜,铜单质首先参加反应
查看答案和解析>>
科目: 来源: 题型:
【题目】以烯烃为原料,合成某些高聚物的路线如下:
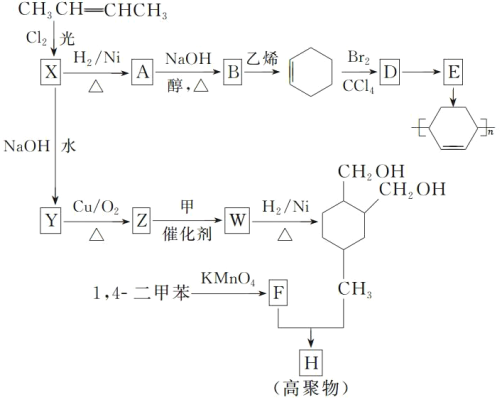
已知:

(1)CH3CH=CHCH3 的名称是_____。
(2)X 中含有的官能团是_____。
(3)A→B 的化学方程式是_____。
(4)D→E 的反应类型是_____。
(5)甲为烃,F 能与 NaHCO3 反应产生 CO2。
①下列有关说法正确的是_____。
a.有机物Z 能发生银镜反应
b.有机物Y 与HOCH2CH2OH 互为同系物
c.有机物Y 的沸点比 B 低
d.有机物F 能与己二胺缩聚成聚合物
②Y 的同分异构体有多种,写出分子结构中含有酯基的所有同分异构体的结构简式____。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国成功发射的“嫦娥”卫星和“玉兔”月球车对探究月球结构和资源开发具有极为重要的战略意义。请回答下列问题:
(1)发射“嫦娥”卫星使用了大功率运载火箭,火箭推进器中装有还原剂肼![]() 和强氧化剂过氧化氢
和强氧化剂过氧化氢![]() ,其反应为
,其反应为 ,已知生成
,已知生成![]() 释放出
释放出![]() 热量。
热量。
①写出![]() 在催化剂作用下分解的化学方程式:_______。
在催化剂作用下分解的化学方程式:_______。
②用电子式表示![]() 的形成过程:_______。
的形成过程:_______。
③若该火箭推进器中![]() 有
有![]() 共价键发生断裂,释放出的热量为_______
共价键发生断裂,释放出的热量为_______![]() 。
。
(2)镍氢蓄电池具有能量密度大、电压高、可多次反复充放电等特性而被用于“玉兔”月球车上,![]() 溶液作电解液,其放电时,正极的电极反应式为
溶液作电解液,其放电时,正极的电极反应式为![]() ,负极的电极反应式为
,负极的电极反应式为 ,利用太阳能充电时负极的电极反应式为
,利用太阳能充电时负极的电极反应式为 。
。
①该镍氢蓄电池放电时的总反应方程式为_______。
②该电池利用太阳能充电时正极的电极反应式为_______。
③该电池工作时,![]() 向_______(填“正极”或“负极”)迁移。
向_______(填“正极”或“负极”)迁移。
④假设电池工作时有![]() 个电子从负极流向正极,则消耗的H2在标准状况下的体积为_______L。
个电子从负极流向正极,则消耗的H2在标准状况下的体积为_______L。
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 是重要的储氢材料,其组成类似于
是重要的储氢材料,其组成类似于 ![]() 常见的供氢原理如下:
常见的供氢原理如下:
①2LiAlH4![]() 2LiH+2Al+3H2↑
2LiH+2Al+3H2↑
②![]()
下列说法正确的是( )
A.![]() 是共价化合物,LiH 是离子化合物
是共价化合物,LiH 是离子化合物
B.若反应①中生成![]() 氢气,则一定有
氢气,则一定有![]() 铝生成
铝生成
C.生成等质量的氢气,反应①、②转移电子数之比为4:3
D.离子半径:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com