
【题目】氧化铁是一种重要的无机材料,化学性质稳定,催化活性高,具有良好的耐光性、耐热性和对紫外线的屏蔽性,从某种工业酸性废液(主要含Na+、Fe2+、Fe3+、Mg2+、Al3+、Cl-、![]() )中回收氧化铁流程如图所示:
)中回收氧化铁流程如图所示:

已知:常温下Ksp[Mg(OH)2]=1.2×10-11;Ksp[Fe(OH)2]=2.2×10-16;Ksp[Fe(OH)3]=3.5×10-38;Ksp[Al(OH)3]=1.0×10-33
(1)写出在该酸性废液中通入空气时发生反应的离子方程式: _________,指出使用空气比使用氯气好的原因是__________。
(2)已知Fe3+(aq)+3OH-(aq)=Fe(OH)3(s) ΔH=-Q1 kJ·mol-1,题(1)中每生成1 mol含铁微粒时,放热Q2,请你计算1 mol Fe2+全部转化为Fe(OH)3(s)的热效应ΔH=________。
(3)常温下,根据已知条件计算在pH=5的溶液中,理论上Fe3+在该溶液中可存在的最大浓度c(Fe3+)=____________。
(4)有人用氨水调节溶液pH,在pH=5时将Fe(OH)3沉淀出来,此时可能混有的杂质是________(填化学式,下同),用________试剂可将其除去。
【答案】4Fe2++O2+4H+=4Fe3++2H2O 耗费少且无污染 -(Q2+Q1)kJ·mol-1 3.5×10-11 mol·L-1 Al(OH)3 NaOH
【解析】
(1)酸性废液中通入空气时,Fe2+被空气中的氧气所氧化,离子方程式为4Fe2++O2+4H+═4Fe3++2H2O.该方法的优点是耗费少且无污染;
(2)根据盖斯定律计算;
(3)溶液pH=5,则c(OH-)=10-9molL-1,根据Ksp[Fe(OH)3]=3.5×10-38可计算;
(4)根据Ksp[Al(OH)3]=1.0×10-33,可计算出溶液pH=5时,c(Al3+)<1.0×10-5,Al3+也几乎完全沉淀,故可能混有的杂质是Al(OH)3,Al(OH)3溶于强碱,而Fe(OH)3不溶,故可用NaOH溶液除去。
(1)酸性废液中通入空气时,Fe2+被空气中的O2所氧化,离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,该方法的优点是耗费少且无污染;
(2)4Fe2++O2+4H+=4Fe3++2H2O,1 molFe3+时,放热Q2,1molFe3+转化为Fe(OH)3放热热量Q1,根据盖斯定律,1mol Fe2+全部转化为Fe(OH)3(s)的热效应ΔH=-(Q2+Q1)kJ·mol-1;
(3)溶液pH=5,则c(OH-)=10-9mol·L-1,根据Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-)=3.5×10-38,可计算出c(Fe3+)为3.5×10-11 mol·L-1;
(4)根据Ksp[Al(OH)3]=1.0×10-33,可计算出溶液pH=5 时,Ksp[Al(OH)3]=c(Al3+)·c3(OH-)=3.5×10-33,求得c(Al3+)=1.0×10-6 mol·L-1,小于1.0×10-5 mol·L-1,Al3+也完全沉淀,故可能混有的杂质是Al(OH)3;Al(OH)3溶于强碱溶液,而 Fe(OH)3不溶于强碱溶液,故可用NaOH溶液除去。


科目:高中化学 来源: 题型:
【题目】有机物H是一种广谱高效食品防腐剂,如图所示是H分子的球棍模型,下列有关说法正确的是

A. 有机物H的分子式为C9H11O3
B. 有机物H的官能团有羟基、羰基和醚键
C. 有机物H能发生加成反应、取代反应和氧化反应
D. 1mol有机物H最多可与1molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用![]() 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是![]()
A.![]() mol基态氧原子中含有的未成对电子数为
mol基态氧原子中含有的未成对电子数为![]()
B.1L![]()
![]() 溶液,阴离子的总数等于
溶液,阴离子的总数等于![]()
C.![]() 和CuO的混合物中含有铜原子数为
和CuO的混合物中含有铜原子数为![]()
D.由化合态的铁制备![]() 铁,转移电子总数为
铁,转移电子总数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)锂空气电池比传统的锂离子电池拥有更强的蓄电能力,是传统锂离子电池容量的10倍,其工作原理示意图如图所示。

放电时,b电极为电源的极_______,电极反应式为_______。
(2)汽车尾气中![]() 、
、![]() 在一定条件下可发生反应
在一定条件下可发生反应![]() ,定温度下,向容积固定的
,定温度下,向容积固定的![]() 密闭容器中充入一定量的
密闭容器中充入一定量的![]() 和
和![]() ,
,![]() 的物质的量随时间的变化曲线如图所示。
的物质的量随时间的变化曲线如图所示。

①![]() 内该反应的平均速率
内该反应的平均速率![]() _______,从
_______,从![]() 起其他条件不变,压缩容器的容积变为
起其他条件不变,压缩容器的容积变为![]() ,则
,则![]() 的变化曲线可能为图中的_______(填字母)。
的变化曲线可能为图中的_______(填字母)。
②恒温恒容条件下,不能说明该反应已经达到平衡状态的是_______(填序号)。
a.容器内混合气体颜色不再变化 b.容器内的压强保持不变 c.容器内混合气体密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是重要的储氢材料,其组成类似于
是重要的储氢材料,其组成类似于 ![]() 常见的供氢原理如下:
常见的供氢原理如下:
①2LiAlH4![]() 2LiH+2Al+3H2↑
2LiH+2Al+3H2↑
②![]()
下列说法正确的是( )
A.![]() 是共价化合物,LiH 是离子化合物
是共价化合物,LiH 是离子化合物
B.若反应①中生成![]() 氢气,则一定有
氢气,则一定有![]() 铝生成
铝生成
C.生成等质量的氢气,反应①、②转移电子数之比为4:3
D.离子半径:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应![]() 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
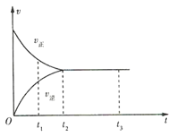
A.t1时,反应只向正方向进行B.t2时,反应未达到限度
C.t2~t3,反应已停止D.t2~t3,各物质的浓度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将FeO与Cu(NO3)2的混合物9.08g全部溶于300mL、1mol/L的盐酸中,有部分Fe2+被酸性条件下的NO3-氧化(其化学反应方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O),放出NO气体448mL(标准状况);继续向溶液中通入一定量的Cl2恰好将溶液中的Fe2+完全氧化;再加入10g过量的铁粉,充分反应放出H2,过滤,得到不溶固体。下列叙述不正确的是
A.Cu(NO3)2的物质的量为0.01mol
B.通入Cl2的体积(标准状况)为448mL
C.放出H2的体积(标准状况)为112mL
D.得到不溶固体的质量为6.72g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2![]() 2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成nmolO2的同时,生成2nmolNO2
②单位时间内生成nmolO2的同时,生成2nmolNO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
A.②③④B.①③⑤C.①④⑥D.②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 锶(Sr)原子序数为 38,在周期表中的位置为_____关于锶及其化合物的说法中不正确的是_________
a. 锶能与冷水剧烈反应
b. 锶的失电子能力比钙强
c. Sr(OH)2 的碱性比 Ca(OH)2 弱
d. 氧化锶是碱性氧化物
II.高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,61℃时晶体开始失去结晶水,100℃时失去全部结晶水。用工业碳酸锶粉末(含少量 Ba、Fe 的化合物等杂质)制备高纯六水氯化锶晶体的过程如下图所示。
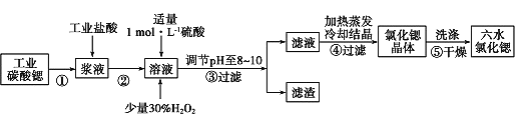
请回答:
(1)已知常温下,NaCl 溶液、BaCl2 溶液呈中性,而 MgCl2 、CuCl2 溶液呈酸性。常温下,SrCl2 溶液 pH_____7(填“大于”、“等于”或“小于”);
(2)步骤③所得滤渣的主要成分是_________(填化学式),调节溶液 pH 至 8~10,宜选用的试剂为_____。
a.稀硫酸 b.氢氧化锶粉末 c.氢氧化钠 d.氧化锶粉末
(3)步骤⑤中,洗涤氯化锶晶体最好选用_____。
a.水 b.稀硫酸 c.氢氧化钠溶液 d.氯化锶饱和溶液
(4)工业上用热风吹干六水氯化锶,选择的适宜温度范围是_____(填字母)。
a.50~60℃ b.70~80℃ c.80~100℃ d.100℃以上
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com