
科目: 来源: 题型:
【题目】将一定量的氯气通入300 mL 浓度为lmol/L的NaOH 溶液中恰好完全反应,加热少许时间后溶液中形成NaCl、NaClO及NaClO3的共存体系.下列判断不正确的是
A. n(Na+):n(C1-)可能为7:3
B. n(NaCl):n(NaClO):n(NaClO3)可能为11:1:2
C. 参加反应氯气物质的量为0.15mol
D. 反应中转移电子物质的量n的范围:0.15mol<n<0.25mol
查看答案和解析>>
科目: 来源: 题型:
【题目】石蜡油分解可产生乙烯。乙烯是一种重要的化工原料,某同学设计实验探究工业制备乙烯的原理和乙烯的主要化学性质,实验装置如图所示。
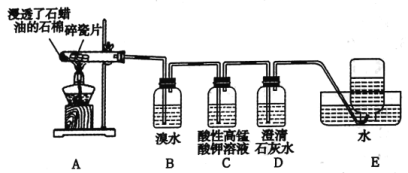
(1)用化学反应方程式解释B装置中的实验现象:_________。
(2)C装置中的现象是_________,其发生反应的类型是__________。
(3)查阅资料可知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_______(填序号)中的实验现象可判断该资料是否真实。
查看答案和解析>>
科目: 来源: 题型:
【题目】运用有关概念判断下列叙述正确的是( )
A.1mol H2燃烧放出的热量为H2的燃烧热
B.Na2SO3和H2O2的反应为氧化还原反应
C.![]() 和
和![]() 互为同系物
互为同系物
D.BaSO4的水溶液不导电,故BaSO4是弱电解质
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式与所述事实相符的是( )。
A.锅炉水垢中的CaSO4用饱和Na2CO3溶液浸泡:![]() +CaSO4=CaCO3+
+CaSO4=CaCO3+![]()
B.向氯化亚铁溶液中加入稀硝酸:Fe2++2H++![]() =Fe3++H2O+NO2↑
=Fe3++H2O+NO2↑
C.用铁电极电解饱和食盐水:2Cl-+2H2O=Cl2↑+H2↑+2OH-
D.向碳酸氢铵溶液中加入足量石灰水:Ca2++![]() +OH-=CaCO3↓+H2O
+OH-=CaCO3↓+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )。
①3.9 g苯与足量的H2反应时,参与反应的碳碳双键数为0.15NA
②3.1 g氧化钠和3.9 g过氧化钠的混合物中含有的阴离子总数为0.1NA
③1.8 g 14CH4和水蒸气(H218O)的混合气体中含有的电子数目为NA
④常温下1 L 0.5 mol·L-1 NH4Cl溶液与2 L 0.25 mol·L-1 NH4Cl溶液所含![]() 的数目相同
的数目相同
⑤常温下,4.6 g NO2和N2O4的混合气体中所含原子总数为0.3NA
⑥将1 mol Cl2通入足量水中,溶液中HClO、Cl-、ClO-数目之和为2NA
⑦高温下,16.8 g Fe与足量水蒸气完全反应转移的电子数为0.8NA
A.①②④⑥B.②⑤⑦
C.②③⑥⑦D.③⑤⑥⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组为了探究一种浅绿色盐X(仅含四种元素,不含结晶水,M(X)<908gmol-1)的组成和性质,设计并完成了如下实验:
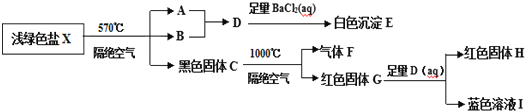
取一定量的浅绿色盐X进行上述实验,充分反应后得到23.3g白色沉淀E、28.8g红色固体G和12.8g红色固体H。
已知:①浅绿色盐X在570℃、隔绝空气条件下受热分解为非氧化还原反应;
②常温下B呈液态且1个B分子含有10个电子。
请回答如下问题:
(1)写出B分子的电子式___。
(2)已知G溶于稀硝酸,溶液变成蓝色,并放出无色气体。请写出该反应的离子方程式为___。
(3)在隔绝空气、570℃温度下加热X至完全分解的化学反应方程式为___。
(4)一定条件下,NH3与黑色固体C发生氧化还原反应得到红色固体和气体丙(丙是大气主要成分之一),写出一个可能的化学反应方程式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)一种铜金合金晶体具有面心立方体结构,在晶胞中Cu原子处于面心,Au原子处于顶点,则该合金中Cu原子与Au原子数量之比为________。
(2)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(如下图)的结构相似,该晶体储氢后的化学式应为________。
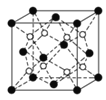
(3)立方BP(磷化硼)的晶胞结构如下图所示,晶胞中含B原子数目为________。
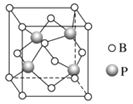
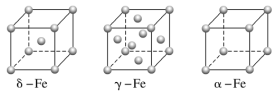
(4)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为________,δ、α两种晶胞中铁原子的配位数之比为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 铜镁合金完全溶解于50mL密度为
铜镁合金完全溶解于50mL密度为![]() 、质量分数为
、质量分数为![]() 的浓硝酸中,得到
的浓硝酸中,得到![]() 和
和![]() 的混合气体
的混合气体![]() ,向反应后的溶液中加入
,向反应后的溶液中加入![]() NaOH溶液,当金属离子全部沉淀时,得到
NaOH溶液,当金属离子全部沉淀时,得到![]() 沉淀。下列说法不正确的是
沉淀。下列说法不正确的是![]()
A.该合金中铜与镁的物质的量之比是2:1
B.得到![]() g沉淀时,加入NaOH溶液的体积是600mL
g沉淀时,加入NaOH溶液的体积是600mL
C.![]() 和
和![]() 的混合气体中,
的混合气体中,![]() 的体积分数是
的体积分数是![]()
D.该浓硝酸中![]() 的物质的量浓度是
的物质的量浓度是![]()
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一](1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是_____________________。
(2)称取碳素钢6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用_______(选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液C.浓氨水 D.酸性KMnO4溶液
②乙同学取560 mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66 g。由此推知气体Y中SO2的体积分数为_______。
[探究二]根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893 g·L-1。为此设计了下列探究实验装置(假设有关气体完全反应)。
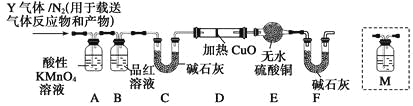
(3)装置B中试剂的作用是_______________________。
(4)分析Y气体中的Q2气体是如何生成的_____________(用化学方程式表示)。
(5)已知洗气瓶M中盛装澄清石灰水,为确认Q2的存在,需在装置中添加洗气瓶M于_______(填序号)。
A.A之前 B.A—B间
C.B—C间 D.C—D间
(6)如果气体Y中含有Q1,预计实验现象应是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com