
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЖЈЮТЖШЯТЃЌдквЛШнЛ§ВЛБфЕФУмБеШнЦїжаЃЌГфШывЛЖЈСПHIЦјЬхЃЌЗЂЩњШчЯТПЩФцЗДгІЃК
2HIЃЈgЃЉ![]() H2ЃЈgЃЉЃЋI2ЃЈgЃЉІЄHЃО0ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
H2ЃЈgЃЉЃЋI2ЃЈgЃЉІЄHЃО0ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
AЃЎШєУПЯћКФ2n mol HIЕФЭЌЪБЩњГЩn mol H2ЃЌБэУїИУЗДгІвбДяЦНКт
BЃЎШнЦїФкЕФбЙЧПВЛЗЂЩњБфЛЏЃЌБэУїИУЗДгІвбДяЦНКт
CЃЎЦНКтЪБЃЌШєЦфЫћЬѕМўВЛБфЃЌдйГфШывЛЖЈСПHIЃЌжиаТДяЦНКтКѓЃЌI2ЕФАйЗжКЌСПдіДѓ
DЃЎЦНКтЪБЃЌШєЦфЫћЬѕМўВЛБфЃЌЩ§ИпЮТЖШЃЌЛьКЯЦјЬхЕФбеЩЋМгЩю
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвдСђЬњПѓЮЊдСЯжЦБИТШЛЏЬњОЇЬх(FeCl3ЁЄ6H2OЃЌ270.5 gЁЄmol-1)ЕФЙЄвеСїГЬШчЭМЫљЪОЁЃ

ЧыЛиД№ЯТСаЮЪЬтЃК
(1)ЮЊМгПьБКЩеЗДгІЕФЛЏбЇЗДгІЫйТЪЃЌПЩВЩШЁЕФДыЪЉЮЊ______ЁЂ__________ЁЃЃЈШЮаДСНЬѕЃЉ
(2)БКЩеКѓЕУЕНЕФFe2O3дкЫсШмЙ§ГЬжаЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ__________ЁЃ
(3)Й§ТЫВйзїгУЕНЕФВЃСЇвЧЦїгаЩеБЁЂ________ЁЂ________ЁЃ
(4)БКЩеЙ§ГЬжаВњЩњЕФSO2ПЩгУЙ§СПЕФАБЫЎНјааЮќЪеЃЌЫљЕУШмвКжаШмжЪЕФУћГЦЮЊ______ЁЂ______ЁЃ
(5)ЯШЯђТШЛЏЬњШмвКжаМгЪЪСПбЮЫсЕФФПЕФЪЧ_________ЃЌдй____ЁЂ______ЁЂЙ§ТЫЁЂЯДЕгЃЌзюжеЕУЕНТШЛЏЬњОЇЬхЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкШчЭМЫљЪОЕФШ§ИіШнЛ§ЯрЭЌЕФШнЦїЂйЂкЂлжаНјааШчЯТЗДгІЃК3A(g)ЃЋB(g) ![]() 2C(g) ІЄH<0ЃЌШєЦ№ЪМЮТЖШЯрЭЌЃЌЗжБ№ЯђШ§ИіШнЦїжаЭЈШы3 mol AКЭ1 mol BЃЌдђДяЕНЦНКтЪБИїШнЦїжаCЮяжЪЕФЬхЛ§ЗжЪ§гЩДѓЕНаЁЕФЫГађЮЊЃЈ ЃЉ
2C(g) ІЄH<0ЃЌШєЦ№ЪМЮТЖШЯрЭЌЃЌЗжБ№ЯђШ§ИіШнЦїжаЭЈШы3 mol AКЭ1 mol BЃЌдђДяЕНЦНКтЪБИїШнЦїжаCЮяжЪЕФЬхЛ§ЗжЪ§гЩДѓЕНаЁЕФЫГађЮЊЃЈ ЃЉ
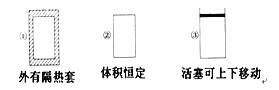
A. ЂлЂкЂйB. ЂлЂйЂкC. ЂйЂкЂлD. ЂкЂйЂл
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЪЕбщжа,ЯжЯѓМАЕУГіЕФНсТле§ШЗЕФЪЧ()
ЪЕбщ | ЯжЯѓ | НсТл | |
A |
| ЪдЙм(1)жазЯЩЋЭЪШЅ, ЪдЙм(2)жазЯЩЋЮДЭЪ | МзЛљЪЙБНЛЗЕФЛюаддіЧП |
B |
| ЪдЙмФкБкга вјОЕЩњГЩ | гаЛњЮяXжавЛЖЈКЌгаШЉЛљ |
C | ЯђЕэЗлШмвКжаМгШыЯЁСђЫс,ЫЎдЁМгШШ,вЛЖЮЪБМфКѓ,дйМгШыаТжЦЕФЧтбѕЛЏЭаќзЧвКВЂМгШШ | ЮДМћзЉКьЩЋГСЕэ | ЕэЗлЮДЫЎНт |
D |
| зюКѓвЛжЛЪдЙмжагаЧГЛЦЩЋГСЕэ | гаЛњЮяжаКЌгафхдзг |
A.AB.BC.CD.D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПввБНЪЧжївЊЕФЛЏЙЄВњЦЗЁЃФГПЮЬтзщФтжЦБИввБН:ВщдФзЪСЯШчЯТ:
ЂйМИжжгаЛњЮяЕФЗаЕуШчЯТБэ:
гаЛњЮя | БН | фхввЭщ | ввБН |
ЗаЕу/Ёц | 80 | 38.4 | 136.2 |
ЂкЛЏбЇдРэ: ![]() +CH3CH2Br
+CH3CH2Br![]()
![]() +HBrЁЃ
+HBrЁЃ
ЂлТШЛЏТСвзЩ§ЛЊЁЂвзГБНтЁЃ
IЃЎжЦБИТШЛЏТС
МзЭЌбЇбЁдёЯТСазАжУжЦБИТШЛЏТСЃЈзАжУВЛПЩжиИДЪЙгУЃЉ:

ЃЈ1ЃЉБОЪЕбщжЦБИТШЦјЕФЗЂЩњзАжУЕФВЃСЇвЧЦїга________жжЁЃ
ЃЈ2ЃЉСЌНгзАжУжЎКѓ,МьВщзАжУЕФЦјУмадЃЌзАвЉЦЗЁЃЯШЕуШМAДІОЦОЋЕЦЃЌЕБ___________ ЪБЃЈЬюЪЕбщЯжЯѓЃЉЕуШМFДІОЦОЋЕЦЁЃ
ЃЈ3ЃЉЦјЬхСїЖЏЗНЯђЪЧДгзѓжСгвЃЌзАжУЕМЙмНгПкСЌНгЫГађaЁњ______ЁњkЁњiЁњfЁњgЁњ_____ЁЃ
ЃЈ4ЃЉDзАжУДцдкУїЯдШБЯнЃЌШєВЛИФНјЃЌЕМжТЕФЪЕбщКѓЙћЪЧ______________ЁЃ
II.жЦБИввБН

ввЭЌбЇЩшМЦЪЕбщВНжшШчЯТ:
ВНжш1ЃКСЌНгзАжУВЂМьВщЦјУмадЃЈШчЭМЫљЪОЃЌМаГжзАжУЪЁТдЃЉЁЃ
ВНжш2ЃКгУОЦОЋЕЦЮЂШШЩеЦПЁЃ
ВНжш3ЃКдкЩеЦПжаМгШыЩйСПЮоЫЎТШЛЏТСЁЂЪЪСПЕФБНКЭфхввЭщЁЃ
ВНжш4ЃКМгШШЃЌГфЗжЗДгІАыаЁЪБЁЃ
ВНжш5ЃКЬсДПВњЦЗЁЃ
ЛиД№ЯТСаЮЪЬт:
ЃЈ5ЃЉБОЪЕбщМгШШЗНЪНвЫВЩгУ_______ ЃЈЬюЁАОЦОЋЕЦжБНгМгШШЁБЛђЁАЫЎдЁМгШШЁБЃЉЁЃ
ЃЈ6ЃЉШЗШЯБОЪЕбщAжавбЗЂЩњСЫЗДгІЕФЪдМСПЩвдЪЧ___ЁЃ
A ЯѕЫсвјШмвК B ЪЏШяЪдвК
C ЦЗКьШмвК D ЧтбѕЛЏФЦШмвК
ЃЈ7ЃЉЬсДПВњЦЗЕФВйзїВНжшгаЃК
ЂйЙ§ТЫЃЛ ЂкгУЯЁбЮЫсЯДЕгЃЛ ЂлЩйСПеєСѓЫЎЫЎЯД ЂмМгШыДѓСПЮоЫЎТШЛЏИЦЃЛЂнгУДѓСПЫЎЯДЃЛ ЂоеєСѓВЂЪеМЏ136.2ЁцСѓЗж ЂпЗжвКЁЃ
ВйзїЕФЯШКѓЫГађЮЊЂнЂп__ __Ђп__ __ЂоЃЈЬюЦфЫќДњКХЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈШнЛ§ЕФУмБеШнЦїжаНјааЗДгІЃЛN2(g)+3H2(g)![]() 2NH3(g)ЁЃМКжЊЗДгІЙ§ГЬжаФГвЛЪБПЬN2ЁЂH2ЁЂNH3ЕФХЈЖШЗжБ№ЮЊ0.1mol/LЁЂ0.3mol/LЁЂ0.2mol/LЁЃЕБЗДгІДяЕНЦНКтЪБЃЌПЩФмДцдкЕФЪ§ОнЪЧ
2NH3(g)ЁЃМКжЊЗДгІЙ§ГЬжаФГвЛЪБПЬN2ЁЂH2ЁЂNH3ЕФХЈЖШЗжБ№ЮЊ0.1mol/LЁЂ0.3mol/LЁЂ0.2mol/LЁЃЕБЗДгІДяЕНЦНКтЪБЃЌПЩФмДцдкЕФЪ§ОнЪЧ
A. N2ЮЊ0.2mol/LЃЛH2ЮЊ0.6mol/L B. N2ЮЊ0.15mol/L
C. N2ЁЂH2ОљЮЊ0.18 mol/L D. NH3ЮЊ0.4mol/L
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАБЗЈШмНўбѕЛЏаПбЬЛвжЦШЁИпДПаПЕФЙЄвеСїГЬШчЭМЫљЪОЁЃШмНўКѓбѕЛЏаПбЬЛвжааПЁЂЭЁЂягЁЂЩщдЊЫиЗжБ№вд[Zn(NH3)4]2ЃЋЁЂ[Cu(NH3)4]2ЃЋЁЂ[Cd(NH3)4]2ЃЋЁЂ[AsCl5]2ЃЕФаЮЪНДцдкЁЃ
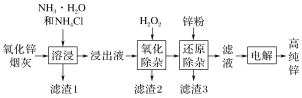
ЁАбѕЛЏГ§дгЁБжаЃЌ[AsCl5]2ЃзЊЛЏЮЊAs2O5НКЬхЮќИНОлГСГ§ШЅЃЌШмвКЪМжеНгНќжаадЃЌИУЗДгІЕФРызгЗНГЬЪНЮЊ_________________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЛЏбЇЪЕбщаЁзщФтЬНОПИФНјFe(OH)2ЕФжЦШЁЗНЗЈЁЃ
ЗНАИ1ЃК
ЂйЪЕбщвЉЦЗЃКFeSЙЬЬхЁЂЯЁСђЫсШмвКЁЂNaHCO3ШмвКЃЛ
ЂкЪЕбщзАжУШчЭМ1ЁЃ
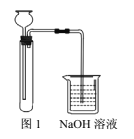
ЗНАИ2ЃК
ЂйШЁвЛжЛЪдЙмЃЌЯђЦфжаМгШывЛСЃNaOHЙЬЬхЃЌдйМгШыдМ2mLаТжЦЕФFeSO4ШмвКЃЛ
ЂкНЋЪдЙмжУгкОЦОЋЕЦЛ№бцЩЯЃЌЖдзХгаNaOHПХСЃЕФВПЮЛаЁаФМгШШ(ВЛФмЪЙвКЬхОчСвЗаЬк)ЁЃЪЙГСЕэздЯТжСЩЯТ§Т§діЖрЃЌЙлВьЯТВПГСЕэбеЩЋЁЃ
ЗНАИ3ЃК
ЂйЯШдкЪдЙмжаЕЮШы2~3 mLвКЬхЪЏРЏЃЛ
ЂкгУНКЭЗЕЮЙмаЁаФЭљЪдЙмЕзВПзЂШы4~5 mLаТжЦЕФFeSO4ШмвКЃЛ
ЂлдйЭљЪдЙмжаЭЖШы1СЃТЬЖЙДѓаЁЕФН№ЪєФЦЃЌЙлВьЗДгІЯжЯѓЁЃ
ЛиД№ЯТСаЮЪЬтЃК
(1)ЁАЗНАИ1ЁБжаЃЌКѓМгШыЪдЙмжаЕФвКЬхЪЧ______ЃЌNaOHШмвКЕФзїгУЪЧ_______ЁЃ
(2)ЁАЗНАИ2ЁБжаЃЌЖдзХгаNaOHПХСЃЕФВПЮЛаЁаФМгШШЕФФПЕФЪЧ________ЁЃ
(3)ЁАЗНАИ2ЁБЕФГСЕэжаЃЌЩЯВуГСЕэЕФбеЩЋЪЧ________ЃЌЯТВуГСЕэЕФбеЩЋЪЧ________ЃЌЗЂЩњДЫЯжЯѓЕФдвђЪЧ________ЁЃ
(4)ЁАЗНАИ3ЁБжаЗДгІЕФЛЏбЇЗДгІЗНГЬЪНЮЊ________ЁЃ
(5)ЁАЗНАИ3ЁБЕФЪЕбщЙ§ГЬжаМфЖЯадЕФГіЯжАзЩЋГСЕэЃЌЦфдвђЪЧ_________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШ§ТШЛЏСљАБКЯюм[Co(NH3)6]Cl3ЪЧГШЛЦЩЋЁЂЮЂШмгкЫЎЕФХфКЯЮяЃЌЪЧКЯГЩЦфЫќвЛаЉКЌюмХфКЯЮяЕФдСЯЁЃШчЭМЪЧФГПЦбааЁзщвдКЌюмЗЯСЯ(КЌЩйСПFeЁЂAlЕШдгжЪ)жЦШЁ[Co(NH3)6]Cl3ЕФЙЄвеСїГЬЃК
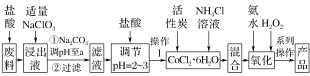
аДГіМгЁАЪЪСПNaClO3ЁБЗЂЩњЗДгІЕФРызгЗНГЬЪН__________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПбЧЯѕЫсФЦ(NaNO2)ЪЧЙЄвЕбЮЕФжївЊГЩЗжЃЌдкЦЏАзЁЂЕчЖЦЕШЗНУцгІгУЙуЗКЁЃЪЕбщЪвРћгУЯТЭМзАжУжЦБИбЧЯѕЫсФЦЃЌВЂВтЖЈЫљжЦбЧЯѕЫсФЦЕФДПЖШЁЃ(МгШШзАжУМАВПЗжМаГжзАжУвбТдШЅ)
Ђё.бЧЯѕЫсФЦЕФжЦБИЁЃ
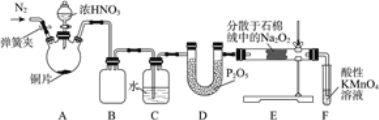
(1)ЪЂЗХХЈHNO3ЕФвЧЦїЕФУћГЦЮЊ__________ЃЛзАжУBЕФзїгУЪЧ______________ЁЃ
(2)зАжУEжажЦШЁNaNO2ЕФЛЏбЇЗНГЬЪНЮЊ___________________ЁЃ
(3)ЖргрЕФNOдкзАжУFжаБЛбѕЛЏЮЊNO3-ЃЌЗДгІЕФРызгЗНГЬЪНЮЊ_____________ЁЃ
(4)ЪЕбщНсЪјКѓДђПЊAжаЕЏЛЩМаЃЌЭЈШыN2ЕФФПЕФЪЧ_______________ЁЃ
Ђђ.бЧЯѕЫсФЦДПЖШЕФВтЖЈЁЃ
ЕБNa2O2ЭъШЋЗДгІКѓЃЌEжаВњЩњЕФЙЬЬхГ§NaNO2ЭтЃЌЛЙПЩФмгаNaNO3ЁЃВтЖЈбЧЯѕЫсФЦДПЖШЕФВНжшШчЯТЃК
ВНжшвЛЃКШЁЗДгІКѓЕФЙЬЬх4.30 gШмгкЯЁСђЫсЃЌЯђЫљЕУШмвКжаМгШызуСПKIЃЌНЋШмвКжаЕФNO2-КЭNO3-ШЋВПЛЙдЮЊNOЃЌВЂЭЈШызуСПN2ЃЌНЋNOШЋВПИЯГіЃЌзюКѓНЋШмвКЯЁЪЭжС1000 mLЁЃ
ВНжшЖўЃКШЁЩЯЪіЫљЕУШмвК10 mLЃЌгУЕэЗлзїжИЪОМСЃЌгУ0.050 mol/LЕФNa2S2O3БъзМвКЕЮЖЈЃЌЗЂЩњЕФЗДгІЮЊI2+2Na2S2O3=2NaI+Na2S4O6ЃЌзюжеЯћКФNa2S2O3ШмвКЬхЛ§ЮЊ16.00 mLЁЃ
(5)ВНжшЖўжаДяЕНЕЮЖЈжеЕуЕФБъжОЮЊ______________________ЁЃ
(6)ЛьКЯЙЬЬхжаNaNO2ЕФжЪСПЗжЪ§ЮЊ________ЁЃ(БЃСєШ§ЮЛгааЇЪ§зж)
(7)ШєдкЕЮЖЈжеЕуЖСШЁЕЮЖЈЙмПЬЖШЪБЃЌбіЪгБъзМвКвКУцЃЌдђВтЕУбЧЯѕЫсФЦЕФДПЖШ________ЁЃ(ЬюЁАЦЋИпЁБЁАЦЋЕЭЁБЛђЁАЮогАЯьЁБ)
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com