
科目: 来源: 题型:
【题目】已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去):
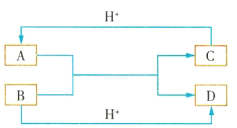
(1)若A、B、C、D均是10电子粒子,请写出A、D的化学式:A___;D___。
(2)若A和C均是18电子粒子,且A为阴离子,B和D均是10电子粒子,则A与B在溶液中反应的离子方程式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有 8 种元素的性质、数据如下表所列,它们属于第二或第三周期。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
-2 | -3 | -1 | -3 |
回答下列问题:
(1)④的元素名称是_____,⑧的元素符号是_____。②在元素周期表中的位置是(周期、族)_____ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_____;名称是________; 碱性最强的化合物的电子式是:_________; 属_____化合物(填“离子”或“共价”)。
(3)①的最简单氢化物的电子式为_____, ⑦的最简单氢化物的电子式为_____,结构式为_____。
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:_________________ 。
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列热化学方程式或离子方程式中,正确的是:
A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将0.5mol N2和1.5molH2置 于密闭的窗口中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:![]() △H=-38.6kJ·mol-1
△H=-38.6kJ·mol-1
C.氯化镁溶液与氨水反应:![]()
D.钢铁腐蚀时可能发生的正极反应:2H2O+ O2+ 4e-=4OH一
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,10mL0.40mol/L H2O2发生催化分解。不同时刻测定生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:v(H2O2)![]()
![]() mol/(L·min)
mol/(L·min)
B.6~10min的平均反应速率:v(H2O2)<![]() mol/(L·min)
mol/(L·min)
C.反应至6min时,c(H2O2)=0.3mol/L
D.反应至6min时,H2O2分解了50%
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下有浓度均为0.5 mol![]() 的四种溶液:
的四种溶液:
①Na2CO3;②NaHCO3;③HCl;④NH3![]() H2O。
H2O。
(1)上述溶液中,可发生水解的是_____(填序号)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为_______。
(3)向溶液④中加入少量氯化铵固体,此时![]() 的值_____(填“增大”“减小”或“不变”),c(OH-)变____(填“变大”“变小”或“不变”)
的值_____(填“增大”“减小”或“不变”),c(OH-)变____(填“变大”“变小”或“不变”)
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积____④的体积(填“大于”“小于”或“等于”),此时溶液中离子浓度由大到小的顺序是___。
(5)取10 mL溶液③,加水稀释到500 mL,则该溶液中由水电离出的c(H+)=___。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属材料、无机非金属材料、有机高分子材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要。
(1)金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于_______变化,钢铁是制造轮船的主要金属材料,船身外通常装上一定数目比铁更活泼的金属块以防止腐蚀,该金属块可以选择_______(选填“铜块”、“锌块”、“铅块”);
(2)无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:

请回答下列问题:
①硝酸钙与碳酸铵在溶液中反应,其基本反应类型为_______;
②实验室常采用_______操作进行沉淀分离;
③生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是_______;
④高纯氧化钙生产过程中,“干燥”的主要目的是为了防止______(用化学方程式表示);
(3)有机高分子材料“玉米塑料”,因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少_______污染,20世纪30年代,尼龙因其抽成细丝极像蚕丝而被推向世界,生活中可采用______方法区分尼龙和蚕丝。
查看答案和解析>>
科目: 来源: 题型:
【题目】相同温度、相同浓度的六种溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分别是
![]()
A.NH4Cl (NH4)2SO4 CH3COONa
B.(NH4)2SO4 NH4Cl CH3COONa
C.(NH4)2SO4 NH4Cl NaOH
D.CH3COOH NH4Cl (NH4)2SO4
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在高温、高压、催化剂作用下,1 mol 金刚石转化为石墨,放出 1.9 kJ 的热量。
(1)石墨和金刚石中,_____能量高,_____更稳定。
(2)推测石墨与金刚石各 1 mol 在相同条件下燃烧,_____放出的热量多。
(3)反应符合图示的是______________
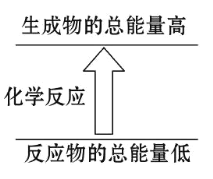
A.铝片与盐酸的反应
B.消石灰与 NH4Cl 晶体的反应
C.酸碱中和反应
D.甲烷在氧气中的燃烧反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作得到的现象和结论均正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液 | 溶液褪色 | BaCl2溶液显酸性 |
B | 向25mL沸水中滴加5~6滴FeCl3饱和溶液,继续煮沸 | 生成红褐色沉淀 | 制得Fe(OH)3胶体 |
C | 向H2S溶液中滴加CuSO4溶液 | 生成蓝色沉淀 | H2S酸性比H2SO4强 |
D | 向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液 | 前者溶液变蓝,后者有黄色沉淀 | KI3溶液中存在I2和I- |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ. (1)写出表示含有 8 个质子、10 个中子的原子的化学符号_____。
(2)原子种类由_________决定;元素种类由_____决定;元素的 同位素由_____决定;元素的化学性质由_________决定。
Ⅱ.有①![]() 、
、![]() 、
、![]() ②H2O、D2O ③石墨、金刚石④H、D、T 四组微粒或物质,回答下列问题:
②H2O、D2O ③石墨、金刚石④H、D、T 四组微粒或物质,回答下列问题:
(1)互为同位素的是_____;
(2)互为同素异形体的是_________;
(3)由①和④中微粒能结合成含三个原子的化合物,这些化合 物中相对分子质量最大的是_________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com