
科目: 来源: 题型:
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃。某小组在实验室中拟用下图所示装置制取并收集C1O2。冋答下列问题:
(1)C1O2的制备
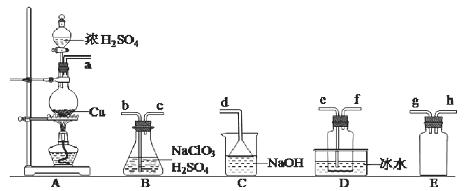
已知:SO2 +2NaClO3 +H2SO4 =2C1O2↑+2NaHSO4
①装置A中反应的化学方程式为_________________________。
②欲收集干燥的C1O2,选择上图中的装罝,其连接顺序为a→____________(按气流方向,用小写字母表示)。
③装置D的作用是_________________。
④若没有E装置,会造成的严重后果是____________________。
(2)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液.为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样;量取V1mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用c mol/LNa2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。(已知2Na2S2O3+I2=Na2S4O6+2NaI)
①步骤2的反应中氧化产物的电子式为______。
②滴定终点的实验现象是_________________。
③原C1O2溶液的浓度为____g/L(用少骤中的字母代数式表示)。
④若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_______;若滴定开始仰视读数,滴定终点时正确读数,则测定结果_____。(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸亚铁是合成锂离子电池正极材料磷酸亚铁锂的原料。某工厂以炼钢厂的脱硫渣(主要成分是Fe2O3)为原料生产电池级草酸亚铁晶体的工艺流程如下:
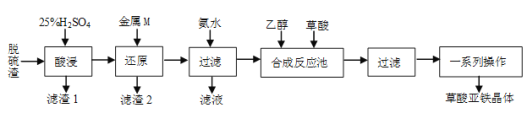
(1)要提高“酸浸”速率,宜采取的措施有___(填两条)。
(2)写出“还原”过程中既是化合反应又是氧化还原反应的离子方程式___。
(3)滤渣2中含有的TiOSO4在热水中易水解,生成H2TiO3,该反应的化学方程式为___。
(4)“滤液”经处理后得到一种化肥,其化学式为___。“一系列操作”指___。
(5)已知:298K时,Ksp[Fe(OH)2]=4.0×10-17,当离子浓度≤1.0×10-5molL-1时,视该离子已完全沉淀。上述流程中,加“氨水”调pH的范围为___(lg2≈0.3)。
(6)草酸亚铁晶体(FeC2O42H2O)纯度的测定:准确称取mg草酸亚铁晶体于锥形瓶中,加入一定量的稀硫酸溶液,并加热至50℃,用cmolL-1KMnO4标准溶液滴定,达到滴定终点时,用去标准溶液VmL。滴定反应(未配平):FeC2O42H2O+KMnO4+H2SO4→Fe2(SO4)3+CO2+MnSO4+K2SO4+H2O;则样品中FeC2O42H2O的纯度为___%(用含有m、c、V的代数式表示);若草酸亚铁晶体失去部分结晶水,测得的结果___(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知1,3-丁二烯和Br2 以物质的量之比为 1∶1 加成时的反应方程式和对应过程的能量变化曲线如图所示。下列说法不正确的是
1,2-加成:![]() +Br2→
+Br2→![]() (产物A)
(产物A)
1,4-加成:![]() +Br2→
+Br2→![]() (产物B)
(产物B)
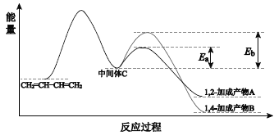
A.1,3-丁二烯和Br2 的加成反应是放热反应
B.其他条件相同时,生成产物A 的反应速率快于生成产物 B 的
C.其他条件相同时,产物A 比产物B 更稳定
D.改变反应温度可能改变产物A 和产物B 的比例
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.锌与稀硫酸反应时,加入少量CuSO4溶液可以使反应速率加快
B.将NaOH和氨水溶液各稀释一倍,两者的c(OH-)均减小到原来的![]()
C.某反应的△H=+100 kJ·mol-1,则正反应的活化能比逆反应的小100 kJ/mol
D.用电解法精炼铜时,用粗铜块作为电解槽的阴极,纯铜片作为电解糟的阳极
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应:2NO2(g) ![]() 2NO(g)+O2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
2NO(g)+O2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①③⑥⑦B.①④⑥⑦C.②③④⑦D.①②④⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液中有关微粒的物质的量浓度关系不正确的是( )
A.物质的量浓度相等的Na2S和NaHS混合溶液中:c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)
B.常温下将醋酸钠、盐酸两溶液混合后溶液呈中性,则混合后溶液中:c(Na+)=c(CH3COO-)>c(OH-)=c(H+)
C.常温下c(NH4+)相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中,溶质的物质的量浓度大小:①>②>③
D.等体积、等物质的量浓度的NaX和弱酸HX混合后呈酸性的溶液中:c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关常见高分子聚合物的说法正确的是
A.苯酚与甲醛在酸性条件下生成酚醛树脂的结构简式为![]()
B.聚-1,3-丁二烯(![]() )是一种碳碳双键和碳碳单键1:1依次交替排列的高分子
)是一种碳碳双键和碳碳单键1:1依次交替排列的高分子
C.![]() 是由对苯二甲酸和乙二醇通过缩聚反应得到的
是由对苯二甲酸和乙二醇通过缩聚反应得到的
D.硫化橡胶具有较高的强度和化学稳定性,是一种线型高分子
查看答案和解析>>
科目: 来源: 题型:
【题目】咖啡酸具有较广泛的抑菌作用,其结构简式如图。下列关于咖啡酸的说法不正确的是
![]()
A.分子中含有2种含氧官能团
B.能与FeCl3溶液发生显色反应
C.1mol咖啡酸最多能与3molBr2反应
D.1 mol咖啡酸最多能与3molNaOH反应
查看答案和解析>>
科目: 来源: 题型:
【题目】含硫化合物在生产生活中应用广泛,科学使用对人体健康及环境保护意义重大。
(1)红酒中添加一定量的SO2 可以防止酒液氧化,这应用了SO2 的___性。
(2)某水体中硫元素主要以S2O32-形式存在,在酸性条件下,该离子会导致水体中有黄色浑浊并可能有刺激性气味产生,原因是___________________________________。(用离子方程式说明)
(3)实验室采用滴定法测定某水样中亚硫酸盐含量:
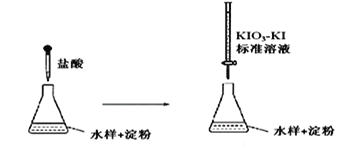
滴定时,KIO3 和KI 在盐酸作用下析出I2:5I-+ IO3- + 6H+ =3I2+3H2O
生成的I2 再和水样中的亚硫酸盐反应:I2 + SO32- + H2O = 2H++2I-+ SO42-
①滴定到终点时的现象是:________________________________
②若滴定前盛标准液的滴定管没有用标准液润洗,则测定结果将_________(填“偏大、偏小、不变”)。
③滴定终点时,100mL的水样共消耗x mL标准溶液。若消耗1mL标准溶液相当于SO32-的质量1g,则该水样中SO32-的含量为__________g / L
(4)已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
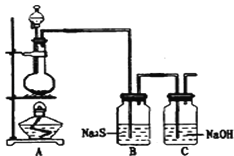
①若装置A的圆底烧瓶中盛装二氧化锰,则分液漏斗中盛装的试剂是_____________________
②装置B中实验现象为___________________________,证明氯元素的非金属性比硫元素的非金属性强。
③装置C中反应的作用是:____________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】I2在KI溶液中存在下列平衡:I2(aq)+I (aq)![]() (aq)。该反应的化学平衡常数K 随着温度的升高而减小。下列说法正确的是( )
(aq)。该反应的化学平衡常数K 随着温度的升高而减小。下列说法正确的是( )
A.反应 I2(aq)+I (aq)![]() (aq)的 ΔH>0
(aq)的 ΔH>0
B.利用上述反应,可以在碘量法滴定过程中加入过量 KI 以减少 I2 的挥发损失
C.在 I2 的 KI 溶液中加入CCl4,平衡不移动
D.一定温度下,向 I2 的KI 溶液中加入少量 KI 固体,化学平衡正向移动,平衡常数K 增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com