
科目: 来源: 题型:
【题目】下列图示与对应的叙述一定正确的是

A.图1所示反应:X(g)+Y(g)![]() 2Z(g),b的压强一定比a大
2Z(g),b的压强一定比a大
B.图2表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂
C.图3表示向Ca(HCO3)2溶液中滴入NaOH溶液所得沉淀的质量变化
D.图4表示明矾溶液受热时氢氧根浓度随温度的变化
查看答案和解析>>
科目: 来源: 题型:
【题目】铝元素含量居金属首位,主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。铝的单质及其化合物在生产、生活、科研等领城应用广泛。
Ⅰ.工业上用铝土矿制备铝的某种化合物的工艺流程如图:

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:___Fe2++___ClO-+___=___Fe(OH)3↓+___C1-+___
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为___(选填代号)
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、___(填操作名称)、过滤、洗涤。
Ⅱ.铵明矾(NH4Al(SO4)212H2O)是常见的食品添加剂,在日常生活、生产中也占有一席之地。
(1)铵明矾可用于净水,用离子方程式表示其净水原理___;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是___。
(2)实验证明铵明矾高温分解后气体的组成成份是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)=___。
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___(填代号)。
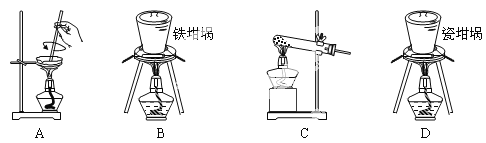
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是![]()
A.铅蓄电池放电时负极质量减轻充电时阳极质量增加
B.同温下,![]() 醋酸溶液
醋酸溶液![]() ,
,![]() 醋酸溶液
醋酸溶液![]() ,则
,则![]()
C.常温下向![]() 溶液中加入少量NaOH固体,溶液中
溶液中加入少量NaOH固体,溶液中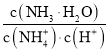 的值增大
的值增大
D.一定条件下反应![]() 当
当![]() ,则反应达到平衡
,则反应达到平衡
查看答案和解析>>
科目: 来源: 题型:
【题目】等物质的量的铁和铜的混合物24g与600mL稀硝酸恰好完全反应,生成NO6.72L(标准状况)。向反应后的溶液中加入1molL-1NaOH溶液使金属离子恰好沉淀。下列有关说法错误的是( )
A.混合物溶解后的溶液中c(Fe3+):c(Fe2+)=1:1
B.稀硝酸的物质的量浓度度是2molL-1
C.需要加入NaOH溶液1000mL
D.最后所得沉淀在空气中充分加热可得固体32g
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验设计能达到相应实验目的是![]()
选项 | 实验设计 | 实验目的 |
A | 在热的NaOH溶液中滴入饱和 | 制备 |
B | 将 | 验证 |
C | 向含少量 | 除去 |
D | 将 | 比较 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】某科研团队研究发现硼氢化钠(NaBH4)在催化剂Ru表面与水反应可生成H2,其反应机理如图所示:
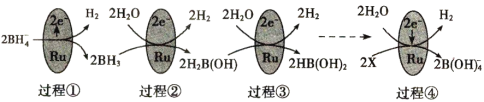
根据以上信息判断,下列叙述错误的是
A.过程①至过程④中硼元素的化合价不变
B.X是H3BO3,H3BO3和BH3两分子中H的化合价相等
C.过程③和过程④各产生1molH2时转移的电子数不相等
D.0.25molNaBH4的还原能力与标准状况下22.4LH2的还原能力相当(还原能力即生成H+失去电子的量)
查看答案和解析>>
科目: 来源: 题型:
【题目】在200℃时,将amol H2(g)和bmol I2(g)充入到体积为V L的密闭容器中,发生反应:I2(g)+H2(g)![]() 2HI(g)。
2HI(g)。
(1)反应刚开始时,由于c(H2)= ______,c(I2)= ______,而c(HI)=______,所以化学反应速率V正最大,而V逆最小(为零)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)______,c(I2)______,而c(HI)______,从而化学反应速率v(正)______,而v(逆)______。
(3)当反应进行到v(正)与v(逆)相等时,此可逆反应就达到了平衡。
查看答案和解析>>
科目: 来源: 题型:
【题目】图中反应![]() 是制备
是制备![]() 的一种方法,其副产物
的一种方法,其副产物![]() 是优质的镁资源。回答下列问题:
是优质的镁资源。回答下列问题:
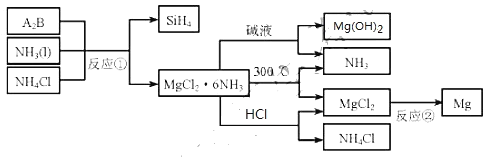
![]() 所含元素的简单离子半径由小到大的顺序
所含元素的简单离子半径由小到大的顺序![]() 除外
除外![]() :______。
:______。
Mg在元素周期表中的位置;______,![]() 的电子式:______。
的电子式:______。
![]() 的化学式为______,反应
的化学式为______,反应![]() 的必备条件是______。上图中可以循环使用的物质有______。
的必备条件是______。上图中可以循环使用的物质有______。
![]() 在一定条件下,由
在一定条件下,由![]() 和
和![]() 反应生成
反应生成![]() 和一种固体耐磨材料______
和一种固体耐磨材料______![]() 写化学式
写化学式![]() 。
。
![]() 为实现燃煤脱硫,向煤中加入浆状
为实现燃煤脱硫,向煤中加入浆状![]() ,使燃烧产生的
,使燃烧产生的![]() 转化为稳定的Mg化合物,写出该反应的化学方程式:______。
转化为稳定的Mg化合物,写出该反应的化学方程式:______。
![]() 用Mg制成的格氏试剂
用Mg制成的格氏试剂![]()
![]() 常用于有机合成,例如制备醇类化合物的合成路线如下:
常用于有机合成,例如制备醇类化合物的合成路线如下:
RBr![]() RMgBr
RMgBr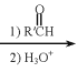
![]()
![]() :烃基;R’:烃基或
:烃基;R’:烃基或![]()
依据上述信息,写出制备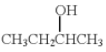 所需醛的可能结构简式:______。
所需醛的可能结构简式:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】判断A(g)+B(g) ![]() C(g)+D(g)是否达到平衡的依据为( )
C(g)+D(g)是否达到平衡的依据为( )
A. 压强不随时间改变
B. 气体的密度不随时间改变
C. c(A)不随时间改变
D. 单位时间里生成C和D的物质的量相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com