
科目: 来源: 题型:
【题目】有关物质的转化关系如图所示。A的摩尔质量为120 g·mol1且只含两种元素。B、E是常见气体,其中B为单质,E能使品红溶液褪色。D为红棕色固体,F为紫红色金属,C的浓溶液可干燥某些气体。

(1)A的化学式为______。
(2)H的电子式为______。
(3)写出反应③的离子方程式:______。
(4)写出反应④的化学方程式:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,某碳酸溶液中的H2CO3、HCO3-、CO32-的物质的量分数δ随pH的变化如下图所示。下列叙述错误的是( )
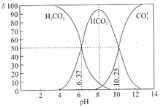
A.当溶液中δ(HCO3-)达到最大时:c(H2CO3)>c(CO32-)
B.Ka2(H2CO3)的数量级为10-11
C.调节溶液的pH由8~10的过程中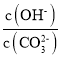 减小
减小
D.加入NaOH使溶液pH=9时,主要反应为HCO3-+OH-=CO32-+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如图所示,已知其燃烧时P被氧化为P4O10,下列有关P4S3的说法中不正确的是( )
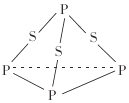
A.P4S3属于共价化合物
B.1mol P4S3分子中含有9mol共价键
C.P4S3充分燃烧的化学方程式为P4S3+8O2![]() P4O10+3SO2
P4O10+3SO2
D.P4S3中磷元素为+3价
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)根据分子中所含官能团可预测有机化合物的性质。
①下列化合物中,能与H2发生加成反应的是______(填字母)。
a.CH3Cl b.CH≡CH c.CH3CH2OH
②下列化合物中,能与NaHCO3发生反应的是______(填字母)。
a.CH3CH2OH b.CH3CHO c.CH3COOH
③下列化合物中,遇到FeCl3溶液显紫色的是______(填字母)。
a.![]() b.
b.![]() c.
c.![]()
(2)甲基丙烯酸甲酯(![]() )是合成有机玻璃的单体。
)是合成有机玻璃的单体。
①1 mol甲基丙烯酸甲酯最多与______ mol H2发生反应。
②写出甲基丙烯酸甲酯在酸性条件下水解的化学方程式:______。
③有机玻璃可由甲基丙烯酸甲酯通过加聚反应得到,有机玻璃的结构简式为______。
(3)水杨醛是一种天然香料的中间体,可通过下列方法合成:
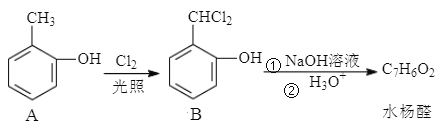
①B中官能团的名称为______和______。
②A→B的反应类型为______。
③水杨醛的结构简式为______。
④水杨醛的同分异构体X能发生水解反应,且1 mol X最多能与2 mol NaOH反应。写出符合上述条件X的结构简式:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下将3 mol CO2和2 mol H2混合于2 L的密闭容器中,发生如下反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g)
CO(g)+H2O(g)
(1)该反应的化学平衡常数表达式K=________。
(2)已知在700 ℃时,该反应的平衡常数K1=0.6,则该温度下反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)的平衡常数K2=________,反应1/2CO2(g)+1/2H2(g)
CO2(g)+H2(g)的平衡常数K2=________,反应1/2CO2(g)+1/2H2(g) ![]() 1/2CO(g)+1/2H2O(g)的平衡常数K3=________。
1/2CO(g)+1/2H2O(g)的平衡常数K3=________。
(3)已知在1 000 ℃时,该反应的平衡常数K4为1.0,则该反应为________反应(填“吸热”或“放热”)。
(4)能判断该反应达到化学平衡状态的依据是________。(填编号)
A.容器中压强不变
B.c(CO2)=c(CO)
C.生成a mol CO2的同时消耗a mol H2
D.混合气体的平均相对分子质量不变
(5)在1 000 ℃下,某时刻CO2的物质的量为2.0 mol,则此时v正________v逆(填“>”、“=”或“<”)。该温度下反应达到平衡时,CO2的转化率为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在25℃时,H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如下图所示,下列叙述错误的是
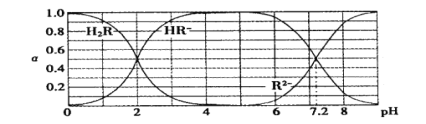
A.H2R是二元弱酸,其Ka1=1×10-2
B.当溶液恰好呈中性时,c( Na + )=2c ( R2- ) + c( HR- )
C.NaHR在溶液中水解倾向大于电离倾向
D.含Na2R与NaHR各0.1 mol的混合溶液的pH=7.2
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,再用待测溶液润洗后,注入待测溶液,然后调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;
③用蒸馏水将锥形瓶洗净后,从碱式滴定管中放入20.00mL待测溶液,滴入甲基橙作指示剂,然后用标准盐酸进行滴定。滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL;
④重复以上过程,测得所耗盐酸的体积为V2mL。
试回答下列问题:
(1)锥形瓶中溶液的颜色从_________色变为___________色时,停止滴定。
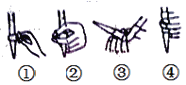
(2)下图中,第②步“调节滴定管的尖嘴部分充满溶液”方法正确的是_________,如果滴定前有气泡,滴定后气泡消失,由此对测定结果形成的影响是___________(填“偏高”、“偏低”或“无影响”)
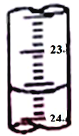
(3)图中是某次滴定时的滴定管中的液面,其读数为__________mL。
(4)根据下列数据:
滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 20.00 | 0.20 | 24.10 |
第二次 | 20.00 | 3.00 | 27.10 |
请计算待测烧碱溶液的浓度为____________mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随加入的c(HC2O4-)的变化趋势如图所示。下列说法正确的是( )
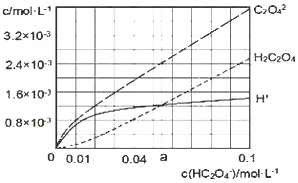
A.当c(HC2O4-)=0.1 mol/L时,c(H+)>c(C2O42-)-c(H2C2O4)
B.当c(HC2O4-)>a mol/L时,c(H+)<c(H2C2O4),HC2O4-的水解程度大于电离程度
C.HC2O4-![]() C2O42-+H+,Ka(HC2O4-)=a
C2O42-+H+,Ka(HC2O4-)=a
D.将0.08 mol/LH2C2O4溶液与等浓度NaOH溶液等体积混合后(忽略体积变化),c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】常温时,用0.1000mol/LNaOH溶液滴定25.00mL0.1000mol/L 某一元酸HX 溶液,滴定过程中pH变化曲线如图所示,下列说法不正确的是
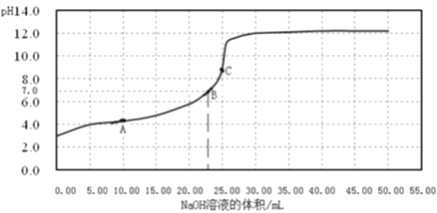
A. 在A点:c (HX)>c(Na+)>c(X-) B. 在B点,溶液中c(H+)=c(OH-)
C. 0.05mol/L NaX 溶液的pH≈9.0 D. C 点溶液中存在的主要平衡是X-+ H2O![]() HX+OH-
HX+OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,向一定体积0.1 mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示,则( )
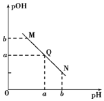
A.N点处pH>pOH,则N点处所示溶液呈酸性
B.该温度下水的离子积Kw=1×10-2a
C.Q点所示溶液呈中性,则M、N、Q三点中只有Q点溶液中水的电离出的c(H+)与水的电离c(OH-)相等
D.M点所示溶液的导电能力强于Q
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com