
科目: 来源: 题型:
【题目】毒重石的主要成分 BaCO3(含 Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备 BaCl2·2H2O 的流程如下:
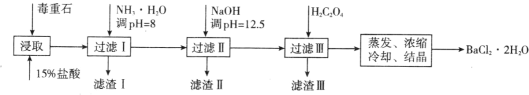
(1)毒重石用盐酸浸取前需充分研磨,目的是_______。实验室用 37%的盐酸配制 15%的盐酸,除量筒外还需使用下列仪器中的_______(填标号)。
a 烧杯 b 容量瓶 c 玻璃棒 d 滴定管
(2)
Ca2+ | Mg2 + | Fe3+ | |
开始沉淀时的 pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的 pH | 13.9 | 11.1 | 3.2 |
流程中,滤渣Ⅱ中含_______(填化学式)。加入 H2C2O4 时应避免过量,原因是_______。 [已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9]
(3)利用间接酸碱滴定法可测定 Ba2+的含量,实验分两步进行。已知:2CrO42-+2H+=Cr2O72-+H2O Ba2++CrO42-=BaCrO4↓
步骤Ⅰ:移取 xmL 一定浓度的 Na2CrO4 溶液与锥形瓶中,加入酸碱指示剂,用 b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为 V0 mL。
步骤Ⅱ:移取 y mLBaCl2 溶液于锥形瓶中,加入 x mL 与步骤Ⅰ相同浓度的 Na2CrO4 溶液,待 Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为 V1 mL。滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的_______(填“上方”或“下方”)。BaCl2 溶液的浓度为___________mol·L-1,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将_______(填“偏大”或“偏小”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下重水(D2O)的离子积常数为1.6×10-15,用定义pH一样来规定pD=-lg{c(D+)},则该温度下,下列叙述正确的是
A.纯净的重水(D2O)中,pD=7
B.1 L溶解有0.01 mol DCl的重水溶液,其pD=12.0
C.纯净的重水中,c(D+)=c(OD-)
D.1 L溶解有0.01 mol NaOD的重水溶液,其pD=12.0
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:C(s) + H2O(g) =CO(g) + H2(g) ΔH=a kJ·mol-1
2C(s) +O2(g) =2CO(g) ΔH=-220 kJ·mol-1
H-H、O=O和O-H键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则a为( )
A.+332B.+118C.+350D.+130
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图所示,![]() ,
,![]() ,下列说法正确的是
,下列说法正确的是
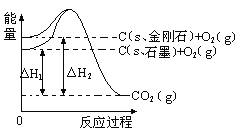
A.石墨和金刚石的转化是物理变化
B.金刚石的稳定性强于石墨
C.石墨的键能比金刚石的键能大1.9kJ/mol
D. C(s,石墨)=C(s,金刚石),该反应的H<0
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于焓变(ΔH)的叙述或判断中错误的是

A. 2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的 ΔH<0
B. 500 ℃、30 MPa下,0.5 mol N2和1.5 mol H2充分反应放出 19.3 kJ 热量,则反应“N2(g)+3H2(g) ![]() 2NH3(g)”的 ΔH=-38.6 kJ·mol-1
2NH3(g)”的 ΔH=-38.6 kJ·mol-1
C. 据下图1 知:ΔH1 = ΔH2+ΔH3
D. 据下图2 知:E的大小对该反应的ΔH 无影响
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A.乙醚和乙醇互为同分异构体
B.苯与苯乙烯具有相同最简式但不是同系物
C.![]() 分子中最多可以有20个原子共平面
分子中最多可以有20个原子共平面
D.CH3CH2CH2CH3和C(CH3)4互为同系物
查看答案和解析>>
科目: 来源: 题型:
【题目】气态烃A在催化剂作用下加压、加热与水反应制得B,B在一定条件下氧化可得C,C在催化剂作用下与氧气反应可得D,D和B与浓硫酸混合加热可得到有香味的无色油状液体E。它们的转化关系如下:

请回答下列问题:
(1)推断下列物质: A_________,B __________,C __________,D__________,E_________; (写结构简式)
(2)写出下列反应方程式并指出反应类型。
①A→B:___________________________________________;属_________反应;
②D+B→E:___________________________________________;属_________反应;
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。
(1)用双线桥表示出电子转移的方向和数目__,题干中反应改写成离子方程式是__。
(2)电解食盐水的过程中,被还原的元素是__,氧化产物是__。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示2套实验装置,分别回答下列问题。
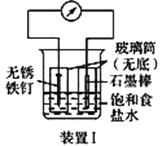
(1)装置Ⅰ为铁的吸氧腐蚀实验。一段时间后,铁被________(填“ 氧化”或“还原”); 向插入石墨棒的玻璃筒内滴入酚酞溶液,可观察到石墨附近的溶液变红,该电极反应为______________________________________。
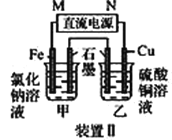
(2)装置Ⅱ中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞溶液,观察到铁片电极附近首先变红。电源的M端为________(填“正”或“负”)极,甲烧杯中铁电极的电极反应为____________,停止电解,乙中________电极质量增加。
查看答案和解析>>
科目: 来源: 题型:
【题目】在不同温度下,向V L密闭容器中加入0.5mol NO和0.5mol活性炭,发生反应:2NO(g)+C(s) ![]() N2(g)+CO2(g) ΔH=-Q kJ·mol-1(Q>0),达到平衡时的数据如下表:
N2(g)+CO2(g) ΔH=-Q kJ·mol-1(Q>0),达到平衡时的数据如下表:
温度/℃ | n(C)/mol | n(CO2)/mol |
T1 | 0.15 | |
T2 | 0.375 |
下列有关说法正确的是( )
A.由上述信息可推知:T1>T2
B.T2℃条件下,若反应达到平衡后再缩小容器的体积,c(N2):c(NO)增大
C.T1℃条件下,若开始时反应物的用量均减小一半, 平衡后NO的转化率增大
D.![]() ℃条件下,该反应的平衡常数
℃条件下,该反应的平衡常数![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com