
科目: 来源: 题型:
【题目】2molA与2molB混合于2L的密闭容器中,发生如下反应,2A(g)+3B(g) ![]() 2C(g)+2D(g),2s后A的转化率为50%,测得v(D)=0.25mol/(L·s)。下列推断不正确的是
2C(g)+2D(g),2s后A的转化率为50%,测得v(D)=0.25mol/(L·s)。下列推断不正确的是
A. z=2
B. 2s后,容器内的压强是初始的7/8倍
C. 2s时,C的体积分数为2/7
D. 2s后,B的浓度为0.5mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】甲烷是天然气的主要成分,是一种重要的清洁能源和化工原料。
(1)用煤制天然气时会发生多个反应,通过多种途径生成CH4。
已知:C(s)十2H2(g) ![]() CH4(g) △H=-73kJ/mol
CH4(g) △H=-73kJ/mol
2CO(g) ![]() C(s)+CO2(g) △H=-171kJ/mol
C(s)+CO2(g) △H=-171kJ/mol
CO(g)十3H2(g) ![]() CH4(g)+H2O(g) △H=-203kJ/mol。
CH4(g)+H2O(g) △H=-203kJ/mol。
写出CO(g) 与H2O(g) 反应生成H 2(g) 和CO2(g) 的热化学方程式____________。
(2)天然气中含有H2S杂质,某科研小组用氨水吸收得到NH4HS溶液,已知T℃k(NH3·H2O) =1.74×10-5; k1(H2S) =1.07×10-7, k2(H2S) =1.74×10-13,NH4HS溶液中所含粒子浓度大小关系正确的是____________。
A c(NH4+)>c(HS-)>c(OH-) >c(H+)
B c(HS-) > c(NH4+)> (S2-) >c(H+)
C c(NH4+)>c(HS-) >c(H2S) >c(H+)
D c(HS-) >c(S2-) >c(H+)>c(OH-)
(3)工业上常用CH4与水蒸气在一定条件下来制取H2,其原理为: CH4(g)+H2O(g) ![]() CO(g)+3H2(g)
CO(g)+3H2(g)
①一定温度时, 在一个体积为2L的恒容密闭容器中, 加入1molCH4和1.4mol水蒸气发生上述反应, 5min后达平衡, 生成0.2mol CO, 用H2表示该反应的速率为____________。此反应的平衡常数为____________(结果保留到小数点后三位)。
②下列说法中能说明此反应达到平衡状态的是____________。
A 体系的压强不再发生变化
B 生成1molCH4的同时消耗3molH2
C 各组分的物质的量浓度不再改变
D 体系的密度不再发生变化
E 反应速率V(CH4):V(H2O):u(CO):u(H2)=1:1:1:3
(4)甲醇水蒸气重整制氢反应:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49kJ/mol。某温度下, 将[n(H2O) :n(CH3OH) ] =1:1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】钛酸钡(BaTiO3)在工业上有重要用途,主要用于制作电子陶瓷、PTC热敏电阻、电容器等多种电子元件。以下是生产钛酸钡的一种工艺流程图:
![]()
已知:①草酸氧化钛钡晶体的化学式为BaTiO(C2O4)2·4H2O;
②25℃时,BaCO3的溶度积Ksp=2.58×10-9;
(1)BaTiO3中Ti元素的化合价为:__________。
(2)用盐酸酸浸时发生反应的离子方程式为: __________。
(3)流程中通过过滤得到草酸氧化钛钡晶体后,为提高产品质量需对晶体洗涤。
①过滤操作中使用的玻璃仪器有_____________________。
②如何证明晶体已洗净?_______________________。
(4)TiO2具有很好的散射性,是一种有重要用途的金属氧化物。工业上可用TiCl4水解来制备,制备时需加入大量的水,同时加热,其目的是:_______________。
(5)某兴趣小组取19.70gBaCO3模拟上述工艺流程制备BaTiO3,得产品13.98g,BaTiO3的产率为:________。
(6)流程中用盐酸酸浸,其实质是BaCO3溶解平衡的移动。若浸出液中c(Ba2+)=0.1mol/L,则c(CO32-)在浸出液中的最大浓度为__________ mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. FeCl3+3KSCN![]() Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体,溶液颜色加深
Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体,溶液颜色加深
B. 工业合成氨中,将氨气液化分离
C. A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B中试管中产生气泡快
D. 对于反应2NO2(g)![]() N2O4(g) △H<0,升高温度可使体系颜色变深
N2O4(g) △H<0,升高温度可使体系颜色变深
查看答案和解析>>
科目: 来源: 题型:
【题目】用标准NaOH溶液滴定未知浓度的盐酸(盐酸放在锥形瓶中,NaOH放在滴定管中),用酚酞作指示剂,下列操作中会导致实验结果偏低的是 ( )
①碱式滴定管用蒸馏水洗净后没有用标准液润洗
②用酸式滴定管加待测液时,刚用蒸馏水洗净后的滴定管未用待测液润洗
③锥形瓶用蒸馏水洗净后没有用待测液润洗
④滴定前滴定管尖端有气泡,滴定后气泡消失
⑤终点读数时俯视,其他读数方法正确.
A.①④B.②③⑤C.②⑤D.④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下, 用0.100mol·L-1NaOH溶液分别滴定20.00mL0.100mol·L-1的HA溶液和HB溶液的滴定曲线如图。下列说法错误的是(己知lg2≈0.3)
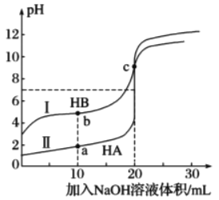
A.HB是弱酸,b点时溶液中c(B-)>c(Na+)>c(HB)
B.a、b、c三点水电离出的c(H+):a>b>c
C.滴定HB溶液时,应用酚酞作指示剂
D.滴定HA溶液时, 当V(NaOH)=19.98mL时溶液pH约为4.3
查看答案和解析>>
科目: 来源: 题型:
【题目】油酸甘油酯(相对分子质量884)是一种典型的脂肪,在体内代谢时可发生如下反应:C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)。已知要消耗1kg该化合物,常人需快走约200公里(每快走1公里按平均耗能190 kJ计)。则油酸甘油酯的燃烧热△H约为( )
A.3.8×104kJ·mol-1B.-3.8×104kJ·mol-1
C.3.4×104kJ·mol-1D.-3.4×104kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用Cs2CO3、XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为__________;第一电离能I1(Si) ____ I1(Ge)(填“>”或“<”)。
(2)基态Ge原子核外电子排布式为_____________;SiO2、GeO2具有类似的晶体结构,其中熔点较高的是________,原因是______。
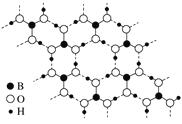
(3)如图为H3BO3晶体的片层结构,其中B的杂化方式为________;硼酸在热水中比在冷水中溶解度显著增大的主要原因是_____________。
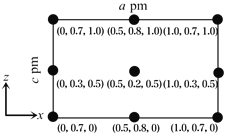
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属于正交晶系(长方体形),晶胞参数为a pm,b pm和c pm。如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为_______;CsSiB3O7的摩尔质量为M g·mol-1,设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为_____________g·cm-1(用代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe—Sm—As—F—O组成的化合物。回答下列问题:
(1)AsH3的沸点比NH3的________(填“高”或“低”),其判断理由是______。
(2)Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为________。
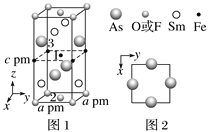
(3)一种四方结构的超导化合物的晶胞如图1所示。晶胞中Sm和As原子的投影位置如图2所示。图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学式表示为____________;通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=______________g·cm-3。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为(![]() ,
, ![]() ,
, ![]() ),则位于底面中心的原子2和铁原子3的坐标分别为___________、__________。
),则位于底面中心的原子2和铁原子3的坐标分别为___________、__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的轨道表示式为_________,基态S原子电子占据最高能级的电子云轮廓图为________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是____________。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为___________。
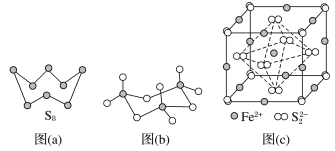
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为____________形,其中共价键的类型有________种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为__________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为______g·cm-3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com