
科目: 来源: 题型:
【题目】元素镍(Ni)、锰(Mn)及其化合物常用作工业生产的催化剂。已知Ni(OH)2(蓝绿色)、Mn(OH)2(紫色)均难溶于水,Ksp[Ni(OH)2]=6×1018,Ksp[Mn(OH)2]=2×1013,回答下列问题:
(1)某溶液中含有浓度较大的Ni2+和Mn2+,向其中滴加NaOH溶液,当Ni2+恰好沉淀完全(恰好完全沉淀时Ni2+浓度等于1.0×105mol·L1)时,溶液中的c(H+)=_______mol/L,此时溶液中c(Mn2+)=_______mol/L(提示:![]() )。
)。
(2)血红蛋白(Hb)与O2和CO存在如下平衡:Hb(aq)+O2(g)![]() HbO2(aq)K1,Hb(aq)+CO(g)
HbO2(aq)K1,Hb(aq)+CO(g)![]() HbCO(aq)K2,正常体温下血红蛋白与两种气体的结合度(α)(注:α
HbCO(aq)K2,正常体温下血红蛋白与两种气体的结合度(α)(注:α![]() =),随两气体平衡分压的变化关系如下图所示:
=),随两气体平衡分压的变化关系如下图所示:
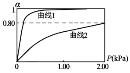
①若平衡常数K1远小于K2,则上图中曲线1代表的气体是_______;利用图中所给数据计算曲线2所代表平衡的平衡常数_______(用气体的平衡分压代替气体的平衡浓度)
②CO和Ni能发生反应生成四羰基镍:Ni+4CO![]() Ni(CO)4(四羰基镍),已知四羰基镍在温度高的条件下易分解,则该反应的正反应是_______(填“放热反应”或“吸热反应”),四羰基镍进入人体血液后更容易释放出金属镍,从而使人镍中毒,分析其中的原因_______。
Ni(CO)4(四羰基镍),已知四羰基镍在温度高的条件下易分解,则该反应的正反应是_______(填“放热反应”或“吸热反应”),四羰基镍进入人体血液后更容易释放出金属镍,从而使人镍中毒,分析其中的原因_______。
(3)已知Ni(OH)3难溶于水,它可由Ni(OH)2与NaClO溶液反应得到,试写出该反应的离子方程式_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ti及其化合物在航天工业上有重要的应用,回答下列问题:
(1)基态Ti原子的价电子排布式为_______,基态Ti原子核外存在_______对自旋相反的电子。
(2)TiCl4熔点为23℃,沸点为136℃,TiCl4晶体属于_______晶体。TiCl4可由TiO2与COCl2在一定条件下反应得到,反应的化学方程式为_______,COCl2中共价键类型为_______,C原子的杂化轨道类型是_______,与COCl2互为等电子体的分子为_______。C、O、Cl的电负性由小到大的顺序为_______。
(3)金红石型TiO2晶胞如图,如果晶胞的边长为apm,则它的密度为_______g/cm3(列出计算式即可)。
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】在25mL某浓度的氨水中逐滴加入0.01mol/L的盐酸溶液,曲线如图所示,有关粒子浓度关系正确的是()
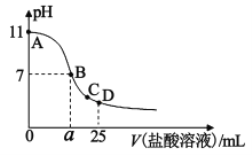
A.该氨水的浓度为0.001mol/L
B.在B点:a=12.5,且有c(NH4+)=c(Cl)=c(OH)=c(H+)
C.在C点:c(Cl)>c(NH4+)>c(H+)>c(OH)
D.在D点:c(NH4+)+c(NH3·H2O)=c(Cl)
查看答案和解析>>
科目: 来源: 题型:
【题目】现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1) m+n_________p(填“>”“=”“<”)。
(2)若加压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入A(体积不变),则B的转化率_________。
(4)若降低温度,则平衡时B、C的浓度之比![]() 将_________。
将_________。
(5)若加入催化剂,平衡时气体混合物的总物质的量___________。
(6)若B是有色物质,A、C均无色,维持容器内压强不变,充入氖气时,混合物颜色_______(填“变深”“变浅”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】咖啡是世界三大饮料之一,因其含有咖啡因(结构简式为![]() )使人神经兴奋,影响人的睡眠。最近科学家用超临界二氧化碳提取咖啡因,成功制得了无因咖啡。下列说法错误的是()
)使人神经兴奋,影响人的睡眠。最近科学家用超临界二氧化碳提取咖啡因,成功制得了无因咖啡。下列说法错误的是()
A.咖啡因的化学式为C8H10N4O2
B.咖啡因是可溶于水的高分子化合物
C.咖啡因在一定条件下可与氢气发生加成反应
D.超临界二氧化碳提取咖啡因的操作是萃取
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温恒容条件下,下列叙述中不是可逆反应2A(g)+3B(g)![]() 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等②单位时间生成amolA,同时消耗1.5molB;③各组分的浓度不再变化;④混合气体的密度不再变化;⑤混合气体的总压强不再变化;⑥混合气体的物质的量不再变化;⑦混合气体的平均摩尔质量不再变化;⑧A、B、C的分子数目比为2: 3: 2.
A. ⑤⑥⑧ B. ②⑤⑧ C. ①③④ D. ②④⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下的2L密闭容器,进行反应2X(g)+Y(g) ![]() 2Z(g),若起始时X、Y、Z物质的量分别为n1、n2、n3(均不为零)。达平衡时,X、Y、Z浓度分别为0.2mol/L、0.1 mol /L和0.08 mol/L,则下列判断合理的是( )
2Z(g),若起始时X、Y、Z物质的量分别为n1、n2、n3(均不为零)。达平衡时,X、Y、Z浓度分别为0.2mol/L、0.1 mol /L和0.08 mol/L,则下列判断合理的是( )
A. X和Y的转化率不一定相等
B. n1、n2=2:1
C. 平衡时,Y和Z的生成速率之比为2:1
D. n1的取值范围为0<n1<0.28
查看答案和解析>>
科目: 来源: 题型:
【题目】苯甲醛是一种重要的化工原料,某小组同学利用如图所示实验装置(夹持装置已略去)制备苯甲醛。
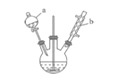
已知有机物的相关数据如下表所示:
有机物 | 沸点℃ | 密度为g/cm3 | 相对分子质量 | 溶解性 |
苯甲醛 | 178.1 | 1.04 | 106 | 微溶于水,易溶于乙醇、醚和卤代烃 |
苯甲醇 | 205.7 | 1.04 | 108 | 微溶于水,易溶于乙醇、醚和卤代烃 |
二氯甲烷 | 39.8 | 1.33 | 难溶于水,易溶于有机溶剂 |
实验步骤:
①向容积为500mL的三颈烧瓶加入90.0mL质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9-10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌。
②充分反应后,用二氯甲烷萃取水相3次,并将有机相合并。
③向所得有机相中加入无水硫酸镁,过滤,得到有机混合物。
④蒸馏有机混合物,得到2.08g苯甲醛产品。
请回答下列问题:
(1)仪器b的名称为______,搅拌器的作用是______。
(2)苯甲醇与NaClO反应的化学方程式为_______。
(3)步骤①中,投料时,次氯酸钠不能过量太多,原因是____;步骤③中加入无水硫酸镁,若省略该操作, 可能造成的后果是______。
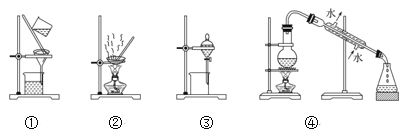
(4)步骤②中,应选用的实验装置是___(填序号),该操作中分离出有机相的具体操作方法是___。
(5)步骤④中,蒸馏温度应控制在_______左右。
(6)本实验中,苯甲醛的产率为________(保留到小数点后一位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】反应:H2(g)+ I2(g)![]() 2HI(g) △H ﹤0 达平衡后,下列说法正确的是
2HI(g) △H ﹤0 达平衡后,下列说法正确的是
A. 增加H2的量,反应放出的热量减小 B. 升高温度,反应放出的热量增加
C. 增大压强,反应放出的热量不变 D. 加入催化剂,反应的△H减小
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1
2NH3(g) ΔH=-92.4 kJ·mol-1
(1)已知:2H2(g)+O2(g)![]() 2H2O(g) ΔH=-483.6 kJ·mol-1。则4NH3(g)+3O2(g)
2H2O(g) ΔH=-483.6 kJ·mol-1。则4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) ΔH=______kJ·mol-1。
2N2(g)+6H2O(g) ΔH=______kJ·mol-1。
(2)如图所示,合成氨反应中未使用催化剂时,逆反应的活化能Ea(逆)=__kJ·mol-1;使用催化剂之后,正反应的活化能为___kJ·mol-1(已知:加入催化剂后,反应分两步进行,反应的活化能是两个过程中需要吸收能量较大的反应的活化能)。
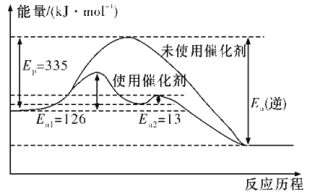
(3)从平衡视角考虑,工业合成氨应该选择常温条件,但实际工业生产却选择500 ℃左右的高温,试解释其原因: ____________________________。
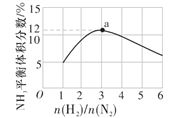
(4)如图表示500 ℃、60 MPa条件下,原料气投料比与平衡时NH3的体积分数的关系。根据图中a点数据计算N2的平衡体积分数为__。
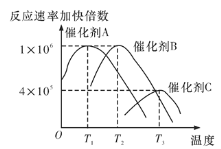
(5)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行实验,所得结果如图所示(其他条件相同),则实际生产中适宜选择的催化剂是__(填“A”“B”或“C”),理由是________。
(6)如图是当反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃反应达到平衡时,混合物中NH3的物质的量分数随总压强的变化曲线。
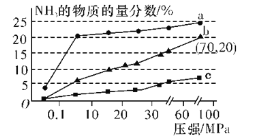
①曲线a、b对应温度较高的是___(填“a”或“b”)。
②列出b点平衡常数的计算式Kp=____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;不要求计算结果)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com