
【题目】现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1) m+n_________p(填“>”“=”“<”)。
(2)若加压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入A(体积不变),则B的转化率_________。
(4)若降低温度,则平衡时B、C的浓度之比![]() 将_________。
将_________。
(5)若加入催化剂,平衡时气体混合物的总物质的量___________。
(6)若B是有色物质,A、C均无色,维持容器内压强不变,充入氖气时,混合物颜色_______(填“变深”“变浅”或“不变”)。
【答案】> 减小 增大 增大 不变 变浅
【解析】
(1)当减小压强时,混合体系中C的质量分数也减小,说明压强减小平衡向逆反应方向移动,则方程式中反应物的气体的计量数之和大于生成物气体的化学计量数之和;
(2)反应物的气体的计量数之和大于生成物气体的化学计量数之和,加压平衡正向移动;
(3)加热A平衡正向移动,B的转化率增大;
(4)达到平衡后,当升高温度时,B的转化率变大,说明温度升高平衡向正反应方向移动,则正反应吸热,降温平衡逆向移动;
(5)催化剂不影响平衡移动;
(6)维持容器内压强不变,充入氖气时,容器的体积增大,所有反应物和生成物的浓度都会减小。
(1)达到平衡后,当减小压强时,混合体系中C的质量分数也减小,说明压强减小平衡向逆反应方向移动,则方程式中反应物的气体的计量数之和大于生成物气体的化学计量数之和,故m+n>p。
(2)增大压强时,平衡向着方程式中气体的计量数之和增大的反应方向移动,即向着正反应方向移动,则A的质量分数减小。
(3)若加入A(体积不变),平衡向着正反应方向移动,则B的转化率增大。
(4)正反应放热,若降低温度,平衡逆向移动,C的物质的量减少,B的物质的量增大,所以二者的浓度比值将增大。
(5)催化剂对化学平衡移动没有影响,所以若加入催化剂,该反应平衡时气体混合物的总物质的量不变。
(6)若B是有色物质,A、C均为无色物质,维持容器内压强不变,充入氖气时,反应体系气体的压强减小,B物质浓度减小,所以体系颜色变浅。


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】甲、乙同学用0.10mol/L H2C2O4草酸溶液、0.01mol/L KMnO4溶液、0.01mol/L H2SO4溶液、一定量的蒸馏水等试剂,进行探究实验,通过测定溶液褪色所需时间来探究浓度、温度对反应速率的影响。
(1)已知酸性KMnO4与H2C2O4反应后Mn元素以Mn2+形式存在溶液中,C元素转化为CO2气体逸出,请写出该反应的化学方程式____________。
(2)为探究反应物浓度、温度对化学反应速率的影响。甲同学设计的实验方案如下表:
实验序号 | 温度/℃ | 体积V/ mL | |||
H2C2O4溶液 | 水 | KMnO4溶液 | H2SO4溶液 | ||
1 | 25 | 10.0 | 0.0 | 4.0 | 2.0 |
2 | 25 | 8.0 | a | 4.0 | 2.0 |
3 | 50 | b | 0.0 | 4.0 | 2.0 |
①若以实验1为对照组,为了达到实验探究目的则a=____________,b=____________。
②若实验1测得溶液褪色所需时间为5s,则用高锰酸钾表示的反应速率为______________________。
(3)乙同学部分实验设计方案如下表:
编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
mol/L | mL | mol/L | mL | ||
① | 0.10 | 2.0 | 0.01 | 4.0 | 25 |
② | 0.10 | 2.0 | 0.02 | 4.0 | 25 |
…… | |||||
该同学想通过实验①和②探究反应物浓度对化学反应速率的影响,请你对该方案的合理性进行评价,并说明理由__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废镍催化剂中主要有Ni,还有Al、Fe、SiO2及其它不溶于酸、碱的杂质。现用废镍催化剂制备NiSO4·7H2O晶体,其流程如图:
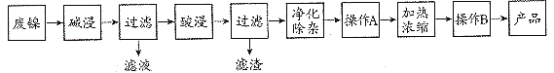
已知:Ksp[Fe(OH)3]=8.0×10-38,Ksp[Fe(OH)2]=8.0×10-16,Ksp[Al(OH)3]=3.2×10-34,Ksp[Ni(OH)2]=2.0×10-15,1g2=0.3,
回答下列问题
(1)“酸浸时发生的离子方程式为Fe+2H+=Fe2++H2↑、____。
(2)“净化除杂需要先加入H2O2溶液,发生反应的离子方程式为___。
(3)Ni2+在强碱性溶液中还可被NaClO氧化为NiOOH,该反应离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化钠(NaBH4)可用作还原剂和塑料发泡剂。它在催化剂作用下与水反应获取氢气的微观过程如图所示。下列说法不正确的是
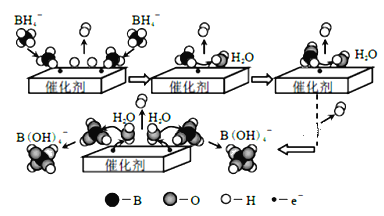
A.NaBH4中氢元素的化合价为+1价
B.若用D2O代替H2O,反应后生成的气体中含有H2、HD和D2
C.通过控制催化剂的用量和表面积,可以控制氢气的产生速率
D.NaBH4 与水反应的离子方程式为:BH4-+4H2O=B(OH)4-+4H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列说法正确的是( )
A. 用惰性电极电解NaH2PO2溶液,其阳极反应式为2H2O+4e-=O2↑+4H+
B. 将H3PO2溶液加入到酸性高锰酸钾溶液中,H3PO2的还原产物可能为H3PO4
C. H3PO2与过量NaOH溶液反应的离子方程式为H3PO2+3OH-= PO23-+3H2O
D. H3PO2溶于水的电离方程式为H3PO2![]() H++H2PO2-
H++H2PO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1200 ℃时,天然气脱硫工艺中会发生下列反应:H2S(g)+![]() O2(g)= SO2(g)+H2O(g) ΔH1,H2S(g)+
O2(g)= SO2(g)+H2O(g) ΔH1,H2S(g)+![]() O2(g)= S(g)+H2O(g) ΔH2,2H2S(g)+SO2(g)=
O2(g)= S(g)+H2O(g) ΔH2,2H2S(g)+SO2(g)= ![]() S2(g)+2H2O(g) ΔH3,2S(g)= S2(g) ΔH4 ,则ΔH4的正确表达式为( )
S2(g)+2H2O(g) ΔH3,2S(g)= S2(g) ΔH4 ,则ΔH4的正确表达式为( )
A.ΔH4=![]() (ΔH1+ΔH3-3ΔH2)B.ΔH4=
(ΔH1+ΔH3-3ΔH2)B.ΔH4=![]() (3ΔH2-ΔH1-ΔH3)
(3ΔH2-ΔH1-ΔH3)
C.ΔH4=![]() (ΔH1+ΔH3-3ΔH2)D.ΔH4=
(ΔH1+ΔH3-3ΔH2)D.ΔH4=![]() (ΔH1-ΔH3-3ΔH2)
(ΔH1-ΔH3-3ΔH2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物如NH3及铵盐、N2H4、N2O4等在中学化学、化工工业、国防等领域占有重要地位。
(1)已知反应NO2(g)+CO(g)=NO(g)+CO2(g)的能量变化如图所示,下列说法正确的是___。
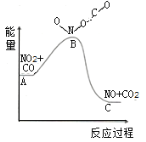
A.图中A→B的过程为放热过程
B.1molNO2和1molCO的键能总和大于1molNO和1molCO2的键能总和
C.该反应为氧化还原反应
D.1molNO2(g)和1molCO(g)的总能量低于1molNO(g)和1molCO2(g)的总能量
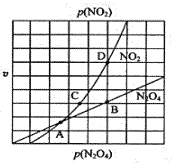
(2)N2O4与NO2之间存在反应N2O4(g)![]() 2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度的变化如图所示。
2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度的变化如图所示。
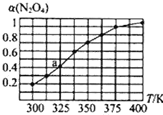
①由图推测该反应的△H___0(填“>”或“<”),理由为___。
②图中a点对应温度下,已知N2O4的起始压强为108kPa,则该温度下反应的平衡常数Kp=__kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系v(N2O4)=k1p(N2O4),v(NO2)=k2p2(NO2),其中k1、k2是与反应温度有关的常数。相应的速率压强关系如图所示,一定温度下,k1、k2与平衡常数Kp的关系是k1=__。
(3)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图所示。
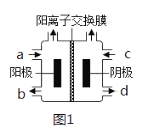
①收集到(CH3)4NOH的区域是___(填a、b、c或d)。
②写出电解池总反应(化学方程式)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.甲烷的燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)H=-890.3kJ/mol
B.同种金属作为原电池的正极比作为电解池的阳极腐蚀得更快
C.向稀硫酸与蔗糖共热后的溶液中滴加银氨溶液,水浴加热,未见银镜,不能说明蔗糖没有水解
D.![]() 的二氯代物有三种
的二氯代物有三种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A. 正戊烷、新戊烷、异戊烷互为同分异构体
B. 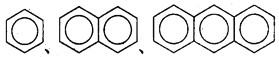 互为同系物
互为同系物
C. 四氯乙烯分子中所有原子都处于同一平面
D. 扁桃酸(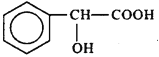 )属于甲酸酯且有羟基直接连在苯环上的同分异构体共有13种
)属于甲酸酯且有羟基直接连在苯环上的同分异构体共有13种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com