
科目: 来源: 题型:
【题目】钛白粉(TiO2)是重要的白色颜料,LiFePO4是锂离子电池的正极材料。一种利用钛铁矿( 主要成分为FeTiO3 和少量Fe2O3 )进行钛白粉和LiFePO4 的联合生产工艺如下图所示:

回答下列问题:
(1) LiFePO4中Fe的化合价是_______________________。
(2)钛铁矿“酸溶”前需要进行粉碎,粉碎的目的是__________________________________。
(3)用离子方程式表示操作I加入铁粉的目的:__________________________。操作II为一系列操作,名称是加热浓缩、冷却结晶、过滤,其中用到的陶瓷仪器的名称是___________。
(4)TiO2+易水解,则其水解的离子方程式为______________________;“转化”利用的是TiO2+的水解过程,需要对溶液加热,加热的目的是________________________________。
(5)“沉铁”的的是使Fe3+生成FePO4,当溶液中c(PO43-)= 1.0×10-17mol/L时可认为Fe3+ 沉淀完全,则溶液中Fe3+沉淀完全时的c(Fe3+)=_______mol/L[已知:该温度下,Ksp(FePO4)=1.0×10-22]。
(6)由“沉铁”到制备LiFePO4的过程中,所需17% H2O2溶液与草酸( H2C2O4)的质量比是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组的同学通过查阅资料获得两个信息:一是在CaO存在的条件下,干燥的NaOH与干燥的CH3COONa混合加热可得到CH4;二是在加热条件下CH4可还原CuO。他们设计如下装置(加热仪器省略)制备CH4、还原CuO并验证B中有CO2、H2O生成。
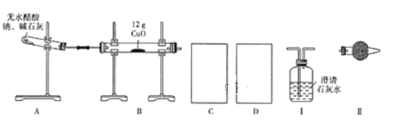
(1)为实现上述实验目的,C、D中的仪器应分别为_______________(填"Ⅰ、Ⅱ"或"Ⅱ、Ⅰ"),Ⅱ中的试剂是________________。
(2)A、B处均需要加热,实验中应先加热______处,表明B中有CO2生成的现象是_________。A中另一种生成物是常见的无机盐,A中反应的化学方程式为_________。
(3)实验表明,即使实验操作、使用试剂完全符合规范实验的要求,制备过程中试管仍会出现破裂情况,试分析其原因:________________。
(4)实验结束后,B中固体全部变成红色,甲同学通过查阅资料后认为,该固体可能是铜、氧化亚铜或者是二者的混合物,同时查得Cu2O在酸性条件下可转化为Cu、Cu2+。为确定红色固体的成分,他设计了如下两种方法。
①取少量红色固体于试管中,再向试管中加入足量的稀硫酸,判断含有Cu2O的现象是________,在常用的酸中,稀硫酸能不能换成稀硝酸_________(填“能”或“不能"),原因是_________。
②称量所得红色固体的质量,当固体质量(m)介于___________之间表明红色固体是Cu与Cu2O的混合物。
查看答案和解析>>
科目: 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl。利用如下反应,可实现氯的循环利用:
4HCl(g)+O2(g) ![]() 2Cl2(g)+2H2O(g) △H=-115.6 kJ·mol-1
2Cl2(g)+2H2O(g) △H=-115.6 kJ·mol-1
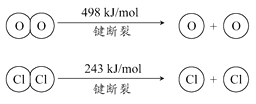
下列说法正确的是
A. 升高温度能提高HCl的转化率
B. 加入催化剂,能使该反应的焓变减小
C. 1molCl2转化为2molCl2原子放出243kJ热量
D. 断裂H2O(g)中1mol H-O键比断裂HCl(g)中1mol H-Cl键所需能量高
查看答案和解析>>
科目: 来源: 题型:
【题目】以芳香烃A和化合物F为原料合成除草剂双苯噁唑酸(I)的一种工艺流程如下:
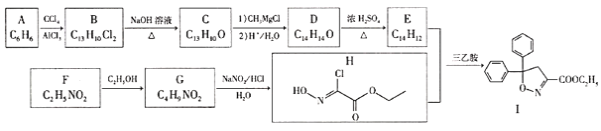
已知以下信息:
①B、C、D、E中均含有两个苯环。
②E能使Br2的CCl4溶液褪色,其核磁共振氢谱有4组峰,峰面积比为2:2:1:1;F中含有两种官能团且具有两性;G能发生水解反应。
③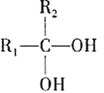 (不稳定)
(不稳定)![]()
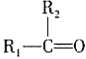
④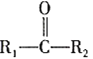
![]()
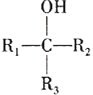 ;RCl
;RCl![]() RMgCl
RMgCl
回答下列问题:
(1)F的化学名称为_______。
(2)A生成B、D生成E的反应类型依次为______________、___________________。
(3)E、G的结构简式依次为__________________、________________。
(4)B生成C的化学方程式为_________。
(5)芳香化合物X是D的同分异构体,X的苯环上有3个取代基,能与![]() 溶液发生显色反应,能使
溶液发生显色反应,能使![]() 的
的![]() 溶液褪色,X的核磁共振氢谱有5组峰且峰面积比为6:4:2:1:1,写出两种符合要求的X的结构简式:______________。
溶液褪色,X的核磁共振氢谱有5组峰且峰面积比为6:4:2:1:1,写出两种符合要求的X的结构简式:______________。
(6)根据题给信息,写出以乙醛为原料制备2-丁醇的合成路线:________(其他试剂任用)。
查看答案和解析>>
科目: 来源: 题型:
【题目】铜和硫的化合物在化工、医药材料等领域具有广泛的用途。回答下列问题:
(1)原子轨道是指电子在原子核外的___________,基态S原子的原子轨道数是____个。
(2)基态Cu原子中,核外电子占据的原子轨道为球形的最高能级符号是______,占据该能级的电子数为__________。
(3)Cl、S、Se在元素周期表中处于相邻的位置,其第一电离能的大小顺序为_______。
(4)下图是含元素Cu、S的有机物的结构简式:

①该有机化合物结构中含有的化学键类型是_______(填“共价键““离子键”或“共价键、离子键”)、配位键,其中1个该有机物分子中配位键数为_____个,这些配位键中提供孤电子对的元素是__________。
②S原子的杂化方式为_______、带*N原子的杂化方式为_______。
(5)下图是Cu-Au合金的一种立方晶体结构:

已知该合金的密度分dg/cm3,阿伏加德罗常数的值为NA,若Au原子的半径为bpm(lpm=10-10cm),则铜原子的半径为______cm(写出计算表达式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】分析下列反应在任何温度下均能自发进行的是( )
A.2N2(g)+O2(g)═2N2O(g)△H=+163kJmol-1
B.Ag(s)+![]() Cl2(g)═AgCl(s)△H=-127kJmol-1
Cl2(g)═AgCl(s)△H=-127kJmol-1
C.HgO(s)═Hg(l)+![]() O2(g)△H=+91kJmol-1
O2(g)△H=+91kJmol-1
D.H2O2(l)═![]() O2(g)+H2O(l)△H=-98kJmol-1
O2(g)+H2O(l)△H=-98kJmol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列涉及化学学科观点的有关说法正确的是![]()
A. 微粒观:二氧化硫是由硫原子和氧原子构成的
B. 转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和
C. 守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g
D. 结构观:金刚石和石墨由于结构中碳原子的排列方式不同,性质存在着较大的差异
查看答案和解析>>
科目: 来源: 题型:
【题目】氮及其化合物在人们的日常生活、生产和环保事业中属于“明星物质”。回答下列问题:
(1)氨气是农业肥料和化工生产的重要原料,其电子式为____。
(2)叠氮化钠(NaN3)在药物制备、合成影像、化学分析、汽车制造等行业有着广泛的用途,但该物质极易爆炸,且有副毒。可用NaClO溶液对含有叠氮化钠的溶液进行处理,生成一种无污染的气体单质,反应的化学方程式为______________。
(3)“固氮”是农业科学家研究的永恒主题。在某特殊催化剂和光照条件下,N2与水反应可生成NH3。
已知:
(i)4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
(ii)H2O(g)=H2O(l) △H2= -44.0kJ/mol。
则2N2(g) +6H2O(l)![]() 4NH3(g)+3O2(g) △H3=______kJ/mol。
4NH3(g)+3O2(g) △H3=______kJ/mol。
(4)目前“人工固氮”最成功的应用就是工业合成氨:
N2(g) +3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。
2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。

①图甲是测得X、Y 的浓度随时间变化的曲线.其中Y 为_____(写化学式),反应达到平衡时的平均反应速率v(N2) =_________。
②在不同温度和压强下,平衡体系中NH3的体积分数与温度、压强关系如图乙,则压强p1_____p2(填“>”“<”“=”或“不确定”,下同),B、D 两点的平衡常数KB____KD,B 点N2 的转化率=_________(保留3位有效数字)。
(5)“绿水青山就是金山银山”,利用原电池原理(6NO2 +8NH3=7N2+12H2O)可以处理氮的氧化物和NH3 尾气,装置原理图如图丙:

负极反应式为__________,当有标准状况下4.48 L NO2被处理时,转移电子的物质的量为_____mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】某物质G可做香料,其结构简式为![]() ,工业合成路线如下:
,工业合成路线如下:

已知:
Ⅰ. 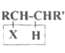
![]() RCH=CHR'
RCH=CHR'
Ⅱ.RCH2X+NaOH![]() RCH2OH+NaX
RCH2OH+NaX
(R、R'为烃基或H原子,X为卤素原子)
回答下列问题:
(1)A为芳香烃,相对分子质量为78。下列关于A的说法中,正确的是____(填序号)。
a.密度比水大
b.所有原子均在同一平面上
c.一氯代物只有一种
(2)反应①的反应类型为__________反应。
(3)C的核磁共振氢谱显示有4组峰,步骤②的化学方程式是__________。
(4)③的反应条件是__________。
(5)④为加成反应,E的核磁共振氢谱显示有6组峰,步骤④的化学方程式是_______。
(6)步骤⑤的化学方程式是__________。
(7)下列说法正确的是__________。
a.上述框图中方框内所有物质均为芳香族化合物
b.D存在顺反异构
c.反应②和⑤都是取代反应
(8)反应⑥中Cu是反应的催化剂,该反应的化学方程式是__________。
查看答案和解析>>
科目: 来源: 题型:
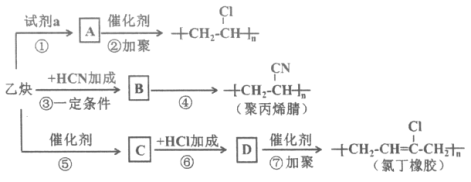
【题目】以乙炔为主要原料可以合成聚氯乙烯、聚丙烯腈和氯丁橡胶,有关合成路线图如下:
已知: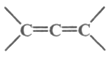 不稳定
不稳定
(1)乙炔中官能团的名称是__________。
(2)试剂a是__________。
(3)写出物质B的结构简式__________。
(4)④的反应类型是__________。
(5)写出下列反应的化学方程式:反应⑤_______;反应⑦_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com