
科目: 来源: 题型:
【题目】氧化石墨烯基水凝胶是一类新型复合材料,常用 Hummers 法制备氧化石墨烯,具体方法为:将石墨粉和无水 NaNO3 混合后置于浓硫酸中并用冰浴冷却,再用 KMnO4 溶液进行氧化处理,最后用 H2O2 处理即可得到氧化石墨烯。请回 答下列问题。
(1)锗(Ge)元素与碳元素同族,基态 Ge 原子的外围电子排布式是_____。与锗同周期且基态原子未成对 电子数与 Ge 原子相同的元素有_____(用元素符号表示)。
(2)对氧化石墨烯进行还原可得到还原氧化石墨烯,二者的结构如图所示:
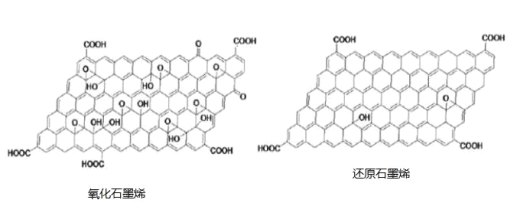
①还原石墨烯中碳原子的杂化形式是___________________ 。
②二者当中在水溶液中溶解度更大的是____________ (填物质名称),原因为__________________。
(3)NaNO3 中 NO3- 的空间构型为_____,写出两种与 NO3- 的互为等电子体的分子的分子式_____。
(4)金属钾晶体和金属锰晶体的三维空间堆积方式均为体心立方堆积。
①上述两种晶体原子在二维平面放置方式均为_____(填“密置层”或“非密置层”)。
②金属钾和金属锰的熔点分别为 63℃和 1244℃,金属锰的熔点高于金属钾熔点的原因为___________。
(5)中国科学家首次证明了二维冰的存在,二维冰是由两层六角冰无旋转堆垛而成,两层之间靠氢键连接,每个水分子与面内水分子形成三个氢键,与面外水分子形成一个氢键,二维冰结构的模型示意图的侧视图 如图 1 所示,厚度为 a pm,俯视图如图 2 所示,距离最近的两个水分子间的距离为 b pm,设阿伏加德罗常 数的值为 N,二维冰的密度是________________ g·cm3。
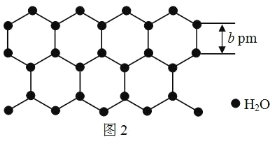

查看答案和解析>>
科目: 来源: 题型:
【题目】硒(Se)是第四周期第ⅥA族元素,是人体内不可或缺的微量元素,H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的重要原料。
(1)已知:①2H2Se(g)+O2(g)![]() 2Se(s)+2H2O(l) ΔH1=akJ·mol-1
2Se(s)+2H2O(l) ΔH1=akJ·mol-1
②2H2(g)+O2(g)![]() 2H2O(l) ΔH2=bkJ·mol-1
2H2O(l) ΔH2=bkJ·mol-1
反应H2(g)+Se(s)![]() H2Se(g)的ΔH3=__kJ·mol-1(用含a、b的代数式表示)。
H2Se(g)的ΔH3=__kJ·mol-1(用含a、b的代数式表示)。
(2)T℃时,向一恒容密闭容器中加入3molH2和1molSe,发生反应H2(g)+Se(s)![]() H2Se(g)。
H2Se(g)。
①下列情况可判断反应达到平衡状态的是__(填字母代号)。
a.气体的密度不变 b.v(H2)=v(H2Se)
c.气体的压强不变 d.气体的平均摩尔质量不变
②当反应达到平衡后,将平衡混合气体通入气体液化分离器使H2Se气体转化为H2Se液体,并将分离出的H2再次通入发生反应的密闭容器中继续与Se反应时,Se的转化率会提高。请用化学平衡理论解释:_。
③以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如图1、图2所示:
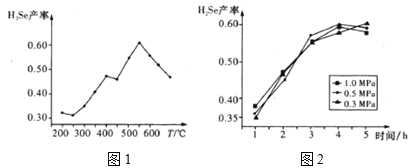
则制备H2Se的最佳温度和压强为__。
(3)已知常温下H2Se的电离平衡常数K1=1.3×10-4、K2=5.0×10-11,则NaHSe溶液呈__(填“酸性”或“碱性”),请通过计算数据说明__。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)化合物SOCl2是一种液态化合物,沸点为77℃,在盛有10mL水的锥形瓶中小心滴加8~10滴SOCl2,可观察到剧烈水解反应,液面有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色。轻轻振荡锥形瓶,等白雾消失后,往溶液中滴加AgNO3溶液,有不溶于HNO3的白色凝乳状沉淀析出。
①根据上述实验,写出SOCl2和水反应的化学方程式____。
②AlCl3溶液蒸干灼烧得不到无水AlCl3,而用SOCl2与AlCl3·6H2O混合共热,可得到无水AlCl3,其原因是____。
(2)25℃时,将amol/L氨水与0.01mol/L盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显__(填“酸”、“碱”或“中”)性。
(3)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中![]() __。
__。
[已知Ksp(BaCO3)=2.2×10–9,Ksp(BaSO4)=1.1×10–10]。
(4)次磷酸(H3PO2)是一种精细化工产品。常温下,K(H3PO2)=1×10–2,0.1mol/L的H3PO2溶液在加水稀释过程中,下列表达式的数据一定变小的是_。(填序号)
A.c(H+) B.![]() C.c(H+)·c(OH-) D.
C.c(H+)·c(OH-) D.![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20.00mL0.1mol·L-1氨水中滴入0.1mol·L-1盐酸,溶液中由水电离出的c(H+)的负对数[-1gc水(H+)]与所加盐酸体积的关系如图所示,下列说法不正确的是( )
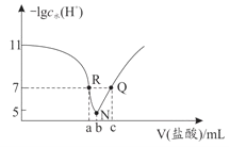
A.常温下,Kb(NH3·H2O)约为1×10-5
B.b=20.00
C.R、Q两点对应溶液均呈中性
D.R到N、N到Q所加盐酸体积不相等
查看答案和解析>>
科目: 来源: 题型:
【题目】一种特殊的热激活电池示意图如下。该电池总反应为:PbSO4(s)+2LiCl+Ca(s)= CaCl2(s)+ Li2SO4+Pb(s) ,下列说法不正确的是
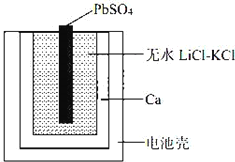
A. Ca电极发生氧化反应
B. 负极的电极反应:Ca(s)+2Cl﹣﹣2e﹣= CaCl2(s)
C. 可用 LiCl 和 KCl 水溶液代替无水 LiCl﹣KCl
D. 当无水LiCl﹣KCl混合物受热熔融后电池才能工作
查看答案和解析>>
科目: 来源: 题型:
【题目】电解法转化CO2实现CO2资源化利用。电解CO2制甲酸盐的装置如图所示。下列说法中正确的是( )
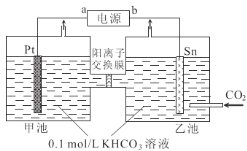
A.b是电源正极
B.K+由乙池向甲池迁移
C.甲池中KHCO3溶液浓度增大,乙池中KHCO3溶液浓度降低
D.乙池电极反应式为:CO2+HCO3-+2e-=HCOO-+CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】研究金属桥墩的腐蚀及防护是桥梁建设的重要课题。下列有关说法正确的是( )
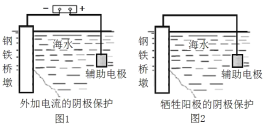
A.图1辅助电极的材料应为铜
B.图1通入的保护电流只与钢铁桥墩和辅助阳极的材料有关
C.图2钢铁桥墩上发生的反应是O2+2H2O+4e-=4OH-
D.钢铁桥墩在河水的腐蚀比海水中更快
查看答案和解析>>
科目: 来源: 题型:
【题目】乙烷是一种重要的化工原料,可用作制冷剂、燃料、制备乙烯的原料。请回答下列问题:
(1)已知:①C2H6 (g)![]() C2H4 (g)+H2(g)ΔH1 =+136.8kJ/mol
C2H4 (g)+H2(g)ΔH1 =+136.8kJ/mol
②H2 (g)+![]() O2(g)
O2(g)![]() H2O(l) ΔH2=-285.8 kJ/mol
H2O(l) ΔH2=-285.8 kJ/mol
③ C2H4(g)+3O2(g)![]() 2CO2(g)+2H2O(l); ΔH3= -1411.0 kJ/mol
2CO2(g)+2H2O(l); ΔH3= -1411.0 kJ/mol
则表征 C2H6 (g)燃烧热的热化学方程式为_____。
(2)1000℃时,在某刚性容器内充入一定量的 C2H6 ,只发生反应①,已知平衡时容器中总压为2.1×105Pa,乙 烷的平衡转化率为 40%。
①乙烷分解前容器压强为_____Pa ,1000℃时,反应①的平衡常数 Kp=_____Pa[气体分压(P 分)=气体 总压(Pa)×物质的量分数]。
②若其他条件不变,刚性容器改为体积可变的密闭容器,则达到平衡时乙烷的转化率_____40%(填“>”、“<” 或“=”)。
(3)乙烷催化氧化裂解法是一种新型的制备乙烯的方法:C2H6 (g)+![]() O2(g)
O2(g)![]() C2H4 (g)+H2O(g)ΔH =-149 kJ/mol,
C2H4 (g)+H2O(g)ΔH =-149 kJ/mol,
① 反应 C2H6 (g)+![]() O2(g)
O2(g)![]() C2H4 (g)+H2O(g)ΔH =-149 kJ/mol的正活化能和逆活化能中较大的是________。
C2H4 (g)+H2O(g)ΔH =-149 kJ/mol的正活化能和逆活化能中较大的是________。
② 800℃时,控制原料气的总物质的量一定,当 C2H6 和 O2 的物质的量之比为 2:1 时,乙烯的平衡产率最大,而当![]() 较小时,乙烯的平衡产率较低,可能的原因为_____。
较小时,乙烯的平衡产率较低,可能的原因为_____。
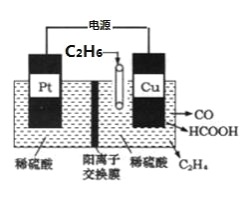
(4)利用电解法可将 C2H6 转化为多种燃料,原理如图所示。铜电极为_____极,该电极上生成 HCOOH 的电极反 应式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯乙烯是一种重要的有机化工原料,某化学小组利用如图装置制备氯乙烯,下列有关说法错误的是
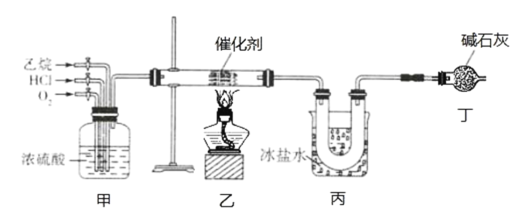
A.装置乙中发生反应的化学方程式为:CH3CH3+HCl+O2![]() CH2=CHCl+2H2O
CH2=CHCl+2H2O
B.装置甲可通过控制通入气体的速率来控制反应气体的物质的量之比
C.装置丙的主要作用为冷凝并分离出氯乙烯
D.装置丁可以完全吸收尾气,实现尾气零排放
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定量的X加入某密闭容器中,发生反应:2X(g)![]() 3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断不正确的是( )
3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断不正确的是( )

A.升高温度,该反应平衡常数K增大
B.压强大小有P3>P2>P1
C.反应过程中加入高效催化剂可以缩短达到平衡的时间
D.在该条件下M点X平衡转化率为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com