
科目: 来源: 题型:
【题目】一种浓差电池如图所示,阴、阳离子交换膜交替放置,中间的间隔交替充以河水和海水,选择性透过Cl和Na+,在两电极板形成电势差,进而在外部产生电流。下列关于该电池的说法正确的是( )
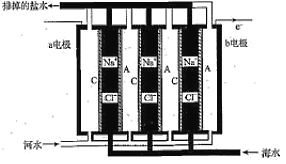
A.a电极为电池的正极,电极反应为2H++2e═H2↑
B.C为阴离子交换膜,A为阳离子交换膜
C.负极隔室的电中性溶液通过阳极表面的还原作用维持
D.该电池的缺点是离子交换膜价格昂贵,优点是电极产物有经济价值
查看答案和解析>>
科目: 来源: 题型:
【题目】柠檬烯是一种食用香料,其结构简式如图所示。下列有关柠檬烯的分析正确的是( )
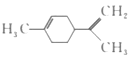
A.它的一氯代物有6种
B.它的分子中所有的碳原子一定在同一平面上
C.它和丁基苯(如图所示)互为同分异构体![]()
D.一定条件下,它分别可以发生加成、取代、氧化等反应
查看答案和解析>>
科目: 来源: 题型:
【题目】燃烧0.1 mol某有机物得0.2 mol CO2和0.3 mol H2O,由此得出的结论不正确的是( )
A. 该有机物分子的结构简式为CH3—CH3
B. 该有机物中碳、氢元素原子数目之比为1∶3
C. 该有机物分子中不可能含有![]() 双键
双键
D. 该有机物分子中可能含有氧原子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应的有机产物,肯定是一种的是( )
A. 异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B. 2—氯丁烷(![]() )与NaOH溶液共热发生反应
)与NaOH溶液共热发生反应
C. 甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D. 等物质的量的甲烷和氯气的混和气体长时间光照后的产物
查看答案和解析>>
科目: 来源: 题型:
【题目】磷酸铁锂是制作电池的材料,其制备过程可以简化成如图所示。下列说法错误的是( )
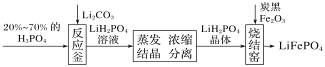
A.蒸发需要的硅酸盐材料仪器有:烧杯、酒精灯、玻璃棒、泥三角
B.反应釜中反应的化学方程式为2H3PO4+Li2CO3=2LiH2PO4+H2O+CO2↑
C.分离的操作是过滤
D.烧结窑中氧化铁与炭黑发生氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.相对分子质量为72的某烷烃,一氯代物有4种
B.四苯基乙烯![]() 中所有碳原子一定处于同一平面
中所有碳原子一定处于同一平面
C.在一定条件下,苯与液溴、浓硝酸生成溴苯、硝基苯的反应都属于取代反应
D.![]() 和
和![]() 分子组成相差一个“-CH2-”,因此是同系物
分子组成相差一个“-CH2-”,因此是同系物
查看答案和解析>>
科目: 来源: 题型:
【题目】在某温度(T℃)的水溶液中,c(H+)=10xmol/L,c(OH-)=10ymol/L,x与y关系如图所示。
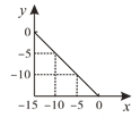
(1)该温度下,水的离子积为________,T℃_____25℃(填“大于”“小于”或“等于”)。
(2)将此温度下pH=11的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH约为________。(已知lg2=0.3)
(3)在此温度下,将pH=13的NaOH溶液VaL与pH=1的硫酸溶液VbL混合。若所得混合液的pH=2,则Va:Vb =_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】山豆根查尔酮具有清热解毒的作用。下列说法错误的是( )
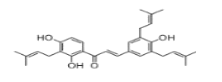
A.它的化学式为C30H34O4。
B.分子中所有的C原子可能共面。
C.1mol山豆根查尔酮最多消耗NaOH、H2的物质的量分别为3mol、11mol。
D.可以用浓溴水检验山豆根查尔酮的存在。
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组欲测定市售橙汁饮料中维生素C的含量。每100克鲜榨橙汁中含有大约37.5毫克的维生素C。实验室可用碘量法测定橙汁饮料中维生素C的含量,反应的方程式为C6H8O6+I2==C6H6O6+2HI(维生素C化学式为C6H8O6,相对分子质量为176),其实验步骤及相关数据如下:
①标准溶液的稀释:移取浓度为0.0080mol/L的碘标准溶液25.00mL于250mL容量瓶中,定容,摇匀备用。
②移取10.00mL饮料样品(设密度为1.0g/cm3)于250 mL锥形瓶中,加入50mL蒸馏水,2mL指示剂。
③在滴定管中装入稀释后的标准溶液,滴定至终点,读取并记录相关数据。
④重复测定3次,数据记录如下表。
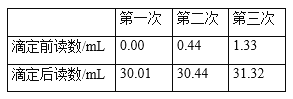
回答下列问题:
(1)实验中盛装标准溶液应选择______(填“酸式”或“碱式”)滴定管。
(2)步骤2中加入的指示剂是___________,判断滴定达到终点的现象是__________。
(3)实验中下列操作可能导致测定结果偏低的是_______(填标号)。
A.稀释标准溶液定容时俯视刻度线
B.滴定结束时俯视读
C.在锥形瓶中加入样品后放置较长时间才开始滴定
D.滴定管尖嘴部分有气泡,滴定后消失
(4)计算该饮料样品中维生素C含量为________mg/100 g。该含量______(填“高于”或“低于”)鲜榨橙汁。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学实验小组用酸性KMnO4溶液与草酸(H2C2O4)溶液反应,研究外界条件对反应速率的影响,实验操作及现象如下:
编号 | 实验操作 | 实验现象 |
I | 向一支试管中先加入1 mL 0.01 mol/L酸性KMnO4溶液,再加入1滴3 mol/L硫酸和9滴蒸馏水,最后加入1 mL 0.1 mol/L草酸溶液 | 前10 min内溶液紫色无明显变化,后颜色逐渐变浅,30 min后几乎变为无色 |
II | 向另一支试管中先加入1 mL 0.01 mol/L酸性KMnO4溶液,再加入10滴3 mol/L硫酸,最后加入1 mL 0.1 mol/L草酸溶液 | 80 s内溶液紫色无明显变化,后颜色迅速变浅,约150 s后几乎变为无色 |
(1)写出高锰酸钾与草酸反应的离子方程式:______________________________。
(2)由实验I、II可得出的结论是_______________________________。
(3)关于实验II中80 s后溶液颜色迅速变浅的原因,该小组提出猜想:反应中生成的Mn2+对该反应有催化作用。利用提供的试剂设计实验III,验证猜想。提供的试剂:0.01 mol/L酸性 KMnO4溶液,0.1 mol/L草酸溶液,3 mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水补全实验III的操作:向试管中先加入1 mL 0.01 mol/L酸性KMnO4溶液,_______,最后加入1 mL 0.1 mol/L草酸溶液。
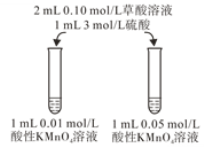
(4)该小组拟采用如图所示的实验方案继续探究KMnO4溶液浓度对反应速率的影响。你认为他们的实验方案______(填“合理”或“不合理”),理由是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com