
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| 催化剂、△ |
| KOH |






查看答案和解析>>
科目: 来源: 题型:



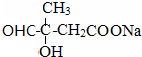
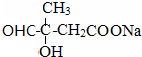


查看答案和解析>>
科目: 来源: 题型:
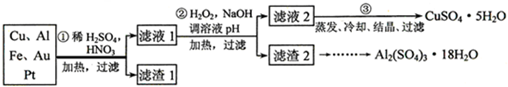
查看答案和解析>>
科目: 来源: 题型:
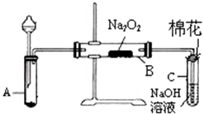 为了探究SO2与Na2O2的反应是否类似于CO2,甲同学设计了如图实验装置.
为了探究SO2与Na2O2的反应是否类似于CO2,甲同学设计了如图实验装置.查看答案和解析>>
科目: 来源: 题型:
 氮化硅(Si3N4)是一种新型陶瓷材料,它可在高温下的氮气流中由石英与焦炭通过以下反应制得:
氮化硅(Si3N4)是一种新型陶瓷材料,它可在高温下的氮气流中由石英与焦炭通过以下反应制得:| c6(CO) |
| c2(N2) |
| c6(CO) |
| c2(N2) |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com