
科目: 来源: 题型:
 (其中Ⅰ、Ⅱ为未知部分的结构),为推测X的分子结构,进行如下的转化示意图:
(其中Ⅰ、Ⅱ为未知部分的结构),为推测X的分子结构,进行如下的转化示意图:


| Cu |
| △ |
| Cu |
| △ |




查看答案和解析>>
科目: 来源: 题型:
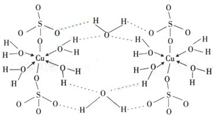 (2010?陕西模拟)由CO与H2催化合成甲醇是生物质能利用的方法之一.
(2010?陕西模拟)由CO与H2催化合成甲醇是生物质能利用的方法之一.查看答案和解析>>
科目: 来源: 题型:
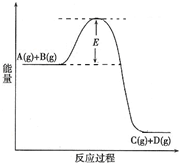 (2010?陕西模拟)已知A(g)+B(g)?C(g)+D(g) 反应过程中的能量变化如图所示,回答下列问题.
(2010?陕西模拟)已知A(g)+B(g)?C(g)+D(g) 反应过程中的能量变化如图所示,回答下列问题.查看答案和解析>>
科目: 来源: 题型:
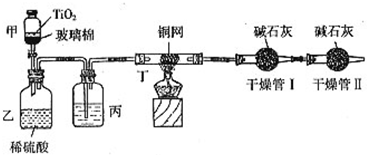 (2010?陕西模拟)根据环保要求,在处理有氰电镀废水时,剧毒的CN-在催化剂TiO2颗粒作用下,先用NaClO将CN-氧化成CNO-(CN-和CNO-中N元素均为-3价),再在酸性条件下继续与NaClO反应生成N2、CO2和Cl2.环保工作人员在密闭系统中用下图装置进行实验,测定CN-被处理的百分率.
(2010?陕西模拟)根据环保要求,在处理有氰电镀废水时,剧毒的CN-在催化剂TiO2颗粒作用下,先用NaClO将CN-氧化成CNO-(CN-和CNO-中N元素均为-3价),再在酸性条件下继续与NaClO反应生成N2、CO2和Cl2.环保工作人员在密闭系统中用下图装置进行实验,测定CN-被处理的百分率.查看答案和解析>>
科目: 来源: 题型:
(2010?陕西模拟)已知25℃时几种弱酸的电离平衡常数:
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com