
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| ||
查看答案和解析>>
科目: 来源: 题型:
下列物质的分类正确的是( )
|
查看答案和解析>>
科目: 来源: 题型:
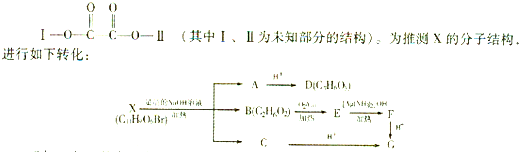
| △ |
| △ |




查看答案和解析>>
科目: 来源: 题型:
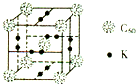 (2012?潍坊一模)[物质结构与性质]
(2012?潍坊一模)[物质结构与性质]查看答案和解析>>
科目: 来源: 题型:
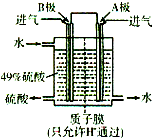 (2012?潍坊一模)黄铁矿(Fe2S,其中S为-1价)是工业生产硫酸的重要原料.FeS2在高温下与氧气反应:3FeS2+8O2
(2012?潍坊一模)黄铁矿(Fe2S,其中S为-1价)是工业生产硫酸的重要原料.FeS2在高温下与氧气反应:3FeS2+8O2
| ||
查看答案和解析>>
科目: 来源: 题型:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
| pH | 9.8 | 9.7 | 11.6 | 10.3 |
| 16 |
| 3 |
| 16 |
| 3 |
查看答案和解析>>
科目: 来源: 题型:
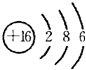

| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
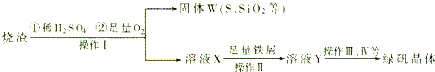

- 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com