
科目: 来源: 题型:
.[化学-有机化学基础](13分)
对二甲苯(英文名称p-xylene),缩写为PX)是化学工业的重要原料。
(1)写出PX的结构简式 。
(2)PX可发生的反应有 、 (填反应类型)。
(3)增塑剂(DEHP)存在如下图所示的转化关系,其中A是PA的一种同分异构体。

①B的苯环上存在2种不同化学环境的氢原子,则B的结构简式是 。
②D分子所含官能团是 (填名称)。
③C分子有一个碳原子连接乙基和正丁基,DEHP的结构简式是 。
(4)F是B的一种同分异构体,具有如下特征:
a.是苯的邻位二取代物;
b.遇FeCl3溶液显示特征颜色;
c.能与碳酸氢钠溶液反应。
写出F与NaHCO3溶液反应的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
[化学-物质结构与性质]13分
(1)元素的第一电离能:Al Si(填“>”或:“<”)
(2)基态Mn2+的核外电子排布式为 。
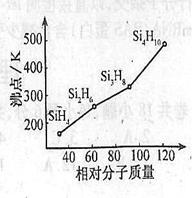
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如右图所示,呈现这种变化关系的原因是 。
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm—(含B、O、H三种元素)的球棍模型如右下图所示:
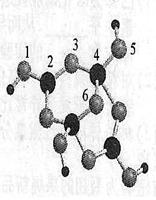
①在Xm—中,硼原子轨道的杂化类型有 ;配位键存在于 原子之间(填原子的数字标号);
m= (填数字)。
②硼砂晶体由Na+、Xm—和H2O构成,它们之间存在的作用力有 (填序号)。
A.离子键 B.共价键 C.金属键
D.范德华力 E.氢键
查看答案和解析>>
科目: 来源: 题型:
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如右图所示)。
 (1)制备实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)。
(1)制备实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)。
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加入浓盐酸
(2)制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出的下列实验方案:
甲方案:与足量AgNO3溶液反应,称量生成的AgCl质量。
乙方案:采用酸碱中和滴定法测定。
丙方案:与已知量CaCO3(过量)反应,称量剩余的CaCO3质量。
丁方案:与足量Zn反应,测量生成的H2体积。
继而进行下列判断和实验:
①判定甲方案不可行,理由是 。
②进行乙方案实验:准确量取残余清液稀释一定的倍数后作为试样。
a.量取试样20.00mL,用0.1000 mol·L—1NaOH标准溶液滴定,消耗22.00mL,该次滴定测的试样中盐酸浓度为 mol·L—1;
b.平行滴定后获得实验结果。
 ③判断丙方案的实验结果 (填“偏大”、“偏小”或“准确”)。
③判断丙方案的实验结果 (填“偏大”、“偏小”或“准确”)。
[已知:Ksp(CaCO3)=2.8×![]() 、Ksp(MnCO3)=2.3×
、Ksp(MnCO3)=2.3×![]() ]
]
④进行丁方案实验:装置如右图所示(夹持器具已略去)。
(i)使Y形管中的残余清液与锌粒反应的正确操作是将 转移到 中。
(ii)反应完毕,每间隔1分钟读取气体体积、气体体积逐渐减小,直至不变。气体体积逐次减小的原因
是 (排除仪器和实验操作的影响因素)。
查看答案和解析>>
科目: 来源: 题型:
(1)电镀是,镀件与电源的 极连接。
(2)化学镀的原理是利用化学反应生成金属单质沉淀在镀件表面形成的镀层。
①若用铜盐进行化学镀铜,应选
用 (填“氧化剂”或“还原剂”)与之反应。
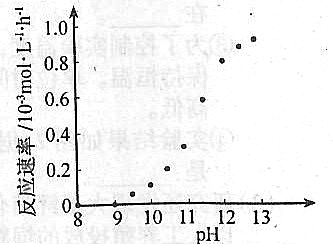
②某化学镀铜的反应速率随镀液pH变化如右图所示。该镀铜过程中,镀液pH控制在12.5左右。据图中信息,给出使反应停止的方法:
(3)酸浸法制取硫酸铜的流程示意图如下:
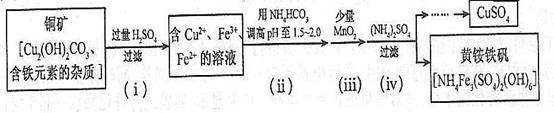
①步骤(i)中Cu2(OH)2CO3发生反应的化学方程式为 。
②步骤(ii)所加试剂起调节pH作用的离子是 (填离子符号)。
③在步骤(iii)发生的反应中,1molMnO2转移2个mol电子,该反应的离子方程式为 。
④步骤(iv)除去杂质的化学方程式可表示为
![]()
过滤后母液的pH=2.0,c(![]() )=a mol·L—1,c(
)=a mol·L—1,c(![]() )=b mol·L—1,c(
)=b mol·L—1,c(![]() )=d mol·L—1,该反应的平衡常数K= (用含a、b、d的代数式表示)。
)=d mol·L—1,该反应的平衡常数K= (用含a、b、d的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
(1)元素M的离子与NH4+所含电子数和质子数均相同,则M的原子结构示意图为
(2)硫酸铝溶液与过量氨水反应的离子方程式为 。
(3)能证明Na2SO3溶液中存在SO32—+H2O![]() HSO3—+OH—水解平衡的事实
HSO3—+OH—水解平衡的事实
是 (填序号)。
A. 滴入酚酞溶液变红,再加入H2SO4溶液红色退去
B. 滴入酚酞溶液变红,再加入氯水后红色退去
C. 滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色退去
(4)元素X、Y在周期表中位于同一主族,化合物Cu2X和Cu2Y可发生如下转化(其中D是纤维素水解的最终产物):
![]()
①非金属X Y(填“>”或“<”)
②Cu2Y与过量浓硝酸反应有红棕色气体生成,化学方程式为 。
(5)在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)![]() 2C(g)+D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高,简述该反应的平衡常数与温度的变化关系: 。
2C(g)+D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高,简述该反应的平衡常数与温度的变化关系: 。
| 物 质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
查看答案和解析>>
科目: 来源: 题型:
一定条件下,溶液的酸碱性对TiO2光催化燃料R降解反应的影响如右图所示。下列判断判断正确的是

A.在0-50min之间,pH=2和pH=7时R的降解百分率相等
B.溶液酸性越强,R的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在20-25min之间,pH=10时R的平均降解速率为0.04 mol·L—1·min—1
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.0.5molO3与11.2LO2所含的分子数一定相等
B.25℃与60℃时,水的pH相等
C.中和等体积、等物质的量的浓度的盐酸和醋酸所消耗的n(NaOH)相等
D.2SO2(g)+O2(g)=2SO3(g)和4SO2(g)+2O2(g)=4SO3(g)的△H相等
查看答案和解析>>
科目: 来源: 题型:
将右图所示实验装置的K闭合,下列判断正确的是

A.![]() 电极上发生还原反应
电极上发生还原反应
B.电子沿Zn![]() a
a![]() b
b![]() Cu路径流动
Cu路径流动
C.片刻后甲池中c(SO42—)增大
D.片刻后可观察到滤纸b点变红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com