
科目: 来源: 题型:解答题
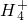 、Fe2+、Fe3+、C
、Fe2+、Fe3+、C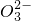 、S
、S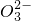 、S
、S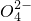 、Cl-、N
、Cl-、N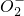 、N
、N 中的一种或几种,取该溶液进行连续实验,实验过程如下:
中的一种或几种,取该溶液进行连续实验,实验过程如下: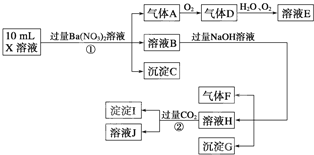
查看答案和解析>>
科目: 来源: 题型:解答题
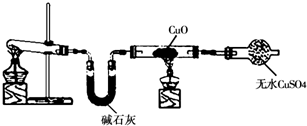
| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 稀硫酸中加入该单质a | 无明显变化 |
| Ⅱ | 硝酸钠溶液中加入该单质a | 无明显变化 |
| Ⅲ | 硫酸钠溶液中加入该单质a | 无明显变化 |
| Ⅳ | 稀硫酸中加入硝酸钠溶液 | 无明显变化 |
| 再加入该单质a | 有无色气泡;溶液变蓝 |
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
| 选项 | 实验内容 | 结论 |
| A | 某物质的水溶液使红色石蕊试纸变蓝 | 该物质一定是碱 |
| B | 某气体能使湿润淀粉碘化钾试纸变蓝 | 该气体一定是氯气 |
| C | 某物质的水溶液中加入盐酸产生无色无味气体 | 该溶液一定是碳酸根离子 |
| D | 0.84g铁和50.00mL 1.00mo l/L的稀硝酸反应 | 反应后溶液中一定有Fe3+和Fe2+ |
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
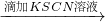 无明显现象
无明显现象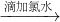 溶液变红
溶液变红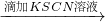 溶液变红
溶液变红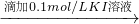 溶液红色未褪去
溶液红色未褪去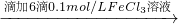 溶液明显变黄
溶液明显变黄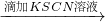 溶液变红
溶液变红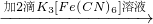 溶液变蓝
溶液变蓝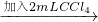 取上层溶液
取上层溶液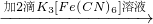 溶液变蓝(比试管2中溶液颜色深)
溶液变蓝(比试管2中溶液颜色深)查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
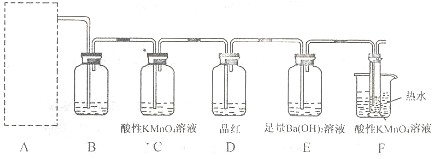
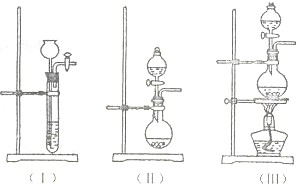
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com