
科目:gzhx 来源: 题型:
科目:gzhx 来源:2012-2013学年上海市普陀区高三下学期二模化学试卷(解析版) 题型:计算题
实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。
请回答:
(1)用软锰矿制备K2MnO4的化学方程式是 。
(2)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为 。生成0.1mol还原产物时转移电子 个。KMnO4、K2MnO4和MnO2的氧化性由强到弱的顺序是 。
(3)KMnO4能与热的Na2C2O4(aq,硫酸酸化)反应生成Mn2+和CO2。若取用软锰矿制得的KMnO4产品0.165g,能与0.335g Na2C2O4恰好完全反应(假设杂质均不能参与反应),该产品中KMnO4的纯度为 。
科目:gzhx 来源: 题型:解答题
科目:gzhx 来源: 题型:
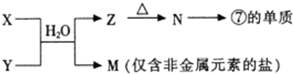
A.XY2 B.XY C.X2Y2 D.Y2
科目:gzhx 来源: 题型:
| 族 | ⅠA | 0 | ||||||
| 周期 | ||||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | |||||


| ||
| ||
科目:gzhx 来源: 题型:
| A、100mL的盐酸中HCl物质的量浓度为7.5mol/L | B、生成的H2S气体在标准状况下的体积为2.24L | C、该磁黄铁矿中FexS的x=0.85 | D、该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3:1 |
科目:gzhx 来源:2010-2011学年江西师大附中、临川一中高三12月联考化学试卷 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的组合是( )
① 2.3 g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA
②含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
③标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA。
④ 25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
⑤ 100 mL 1 mol·L-1 AlCl3溶液中含阳离子数大于0.1NA [来源:Z#xx#k.Com]
⑥ 50 mL 12 mol•L-1 浓盐酸与足量二氧化锰加热反应,转移电子数小于0.3 NA
⑦ 13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA
A.①②⑥ B.①⑤⑥⑦ C.②④⑥⑦ D.③⑤⑥
科目:gzhx 来源:2011届江苏省姜堰市二中高三上学期学情调查(三)化学试卷 题型:单选题
用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
| A.1molFeCl3和沸水完全反应转化为氢氧化铁胶体后,其中胶体粒子数目为NA |
| B.标准状况下,1L液态水中含有的H+ 数目10-7NA |
| C.CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等 |
| D.13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA |
科目:gzhx 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的组合是( )
① 2.3 g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA
②含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
③标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA。
④ 25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
⑤ 100 mL 1 mol·L-1 AlCl3溶液中含阳离子数大于0.1NA
⑥ 50 mL 12 mol??L-1 浓盐酸与足量二氧化锰加热反应,转移电子数小于0.3 NA
⑦ 13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA
A.①②⑥ B.①⑤⑥⑦ C.②④⑥⑦ D.③⑤⑥
科目:gzhx 来源:2010-2011学年云南省宣威市高三上学期期末考试理科化学部分 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的组合是( )
① 2.3 g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1 NA
② 含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
③ 标准状况下,2.24 L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1 NA。
④ 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH- 数目为0.2 NA
⑤ 100 mL 1 mol·L-1 AlCl3溶液中含阳离子数大于0.1 NA
⑥ 7.8 g Na2O2与足量CO2反应,转移电子数为0.1 NA
⑦ 13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2 NA
⑧ 标准状况下,2.24 L H2O含有的电子数为NA
A.①②⑥⑧ B.①⑤⑥⑦
C.②④⑥⑦ D.③⑤⑥⑧
科目:gzhx 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的组合是( )
① 2.3 g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1 NA
② 含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
③ 标准状况下,2.24 L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1 NA。
④ 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH- 数目为0.2 NA
⑤ 100 mL 1 mol·L-1 AlCl3溶液中含阳离子数大于0.1 NA
⑥ 7.8 g Na2O2与足量CO2反应,转移电子数为0.1 NA
⑦ 13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2 NA
⑧ 标准状况下,2.24 L H2O含有的电子数为NA
A.①②⑥⑧ B.①⑤⑥⑦
C.②④⑥⑦ D.③⑤⑥⑧
科目:gzhx 来源:2010-2011学年河南省辉县市高三上学期第四次月考理综化学卷 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的组合是( )
① 2.3 g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA
②含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
③标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA。
④ 25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
⑤ 100 mL 1 mol·L-1 AlCl3溶液中含阳离子数大于0.1NA
⑥ 50 mL 12 mol•L-1 浓盐酸与足量二氧化锰加热反应,转移电子数小于0.3 NA
⑦ 13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA
A.①②⑥ B.①⑤⑥⑦ C.②④⑥⑦ D.③⑤⑥
科目:gzhx 来源:2014届山东省文登市高三上学期期中统考理综化学试卷(B)(解析版) 题型:填空题
要准确掌握化学用语及常用计量方法。按要求回答下列问题:
(1)NA表示阿伏加德罗常数。28g乙烯和环丁烷(C4H8)的混合气体中含有____NA个碳原子;分子总数为NA个的NO2和CO2混合气体含______ NA个氧原子数;1mol37Cl中,中子数比质子数多_______ NA个;1L 1mol/LFe2(SO4)3溶液中含_____NA个SO42-离子。
(2)图中A、B分别是某微粒的结构示意图,回答下列问题:
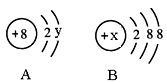
①若A表示某元素的原子,则y= 。
②若B表示某稀有气体元素的原子,则该元素的单质的化学式为 ,若B是阴离子的结构示意图,则x的取值范围是________________。
(3)RxO42-中R的化合价为___________(用含x 的式子表示),当0.3 mol RxO42-完全反应,生成RO2时,转移0.6 mol电子,则x=__________。
(4)将7.8 g镁铝合金与100mL 稀硫酸恰好完全反应,将反应后的溶液加热蒸干,得到无水硫酸盐46.2 g,则原硫酸的物质的量浓度为______________。
科目:gzhx 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.25℃时,pH=3的1.0LNaHSO3溶液中,含Na+数目为0.001 NA
B.常温下,1 molO2和O3的混合气体中所含氧原子数为2.5NA
C.标准状况下,11.2 L的乙烯中含有的共用电子对数为NA
D.13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA
科目:gzhx 来源:江苏省2010届高三年级第一次模拟考试化学试题 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.0.1mol/L的氯化铝溶液中含有的氯离子数为0.3NA
B.常温下,1 molO2和O3的混合气体中所含氧原子数为2.5NA
C.标准状况下,11.2 L的乙烯中含有的共用电子对数为NA
D.13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA
科目:gzhx 来源:2011-2012学年湖南师大附中高三第四次月考化学试卷 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.2.8g铁粉在1.12L(标准状态)氯气中充分燃烧,失去的电子数为0.15NA
B.常温下,0.1mol/L HCl溶液中所含的H+个数为0.1NA
C.26.0g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.4NA
D.11.2L 的CO气体与0.5molN2所含的电子数相等