
科目:gzhx 来源:浙江省浙南、浙北部分学校2012届高三12月联考化学试题 题型:058
含氮废水进入水体后而对环境造成的污染越来越严重,对含氮废水进行有效的检测和合理的处理是人们研究和关心的重要问题.
(1)环境专家认为可以用金属铝将水体中的NO3-还原为N2,从而消除污染.其反应的离子方程式是:
6NO3-+10Al+18H2O=3N2↑+10Al(OH)3+6OH-.又有人认为金属镁比铝能更快消除氮的污染,其反应原理和金属铝相同.写出镁和含NO3-的废水反应的离子方程式________.
(2)水中的NO2-是含氮有机物分解的产物,其浓度的大小是水源污染程度的标志之一.检测水中的NO2-可用目视比色法(比较溶液颜色深浅度以测定所含有色物质浓度的方法),检测步骤如下:
步骤一:配制标准溶液:称取0.69 g NaNO2,溶于水后在容量瓶中稀释至1 L得溶液A,移取5 mL溶液A,稀释至1 L,得溶液B.
步骤二:配制标准色阶:取6只规格为10 mL的比色管(即质地、大小、厚薄相同且具有塞的平底试管),分别加入体积不等的溶液B,并稀释至10 mL,再加入少许(约0.30 g)氨基苯磺酸粉末,实验结果如下表所示.
![]()
步骤三:取10 mL水样倒入比色管中,加少许氨基苯磺酸,显色后与标准色阶对比.
①利用步骤三在野外检测水样污染程度的优点是________.
②步骤二中设计色阶序号1的作用是________.
③如果水样显色后比6号还深,应采取的措施是________.
(3)现有含NH3为3.4 mg·L-1的废水150 m3(密度为1 g·cm-3),可采用如下方法进行处理:将甲醇加入含氨的废水中,在一种微生物作用下发生反应:
2O2+NH3 NO3-+H++H2O
NO3-+H++H2O
6NO3-+6H++5CH3OH→3N2↑+5CO2↑+13H2O
若用此方法处理,假设每步的转化率为100%,需要甲醇________g.
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
荷尔蒙胰岛素是一种蛋白质,含硫3.4%。
(1)胰岛素可能的最小相对分子质量是_________________。
(2)它的相对分子质量为5 734,每一个分子中可能有_____________个硫原子。
科目:gzhx 来源: 题型:
(1)胰岛素可能的最小相对分子质量是_________________。
(2)它的相对分子质量为5 734,每一个分子中可能有_____________个硫原子。
科目:gzhx 来源: 题型:
A、H2O2的电子式为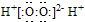 | ||||||
B、O2-、Na的结构示意图都可以用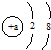 表示 表示 | ||||||
| C、H2O、NaOH、Na2O2中氧元素的化合价均为-2 | ||||||
D、
|
科目:gzhx 来源: 题型:
(08上海12校第二次联考)现有浓度为0.2摩尔/某升一元弱酸HX与浓度的0.1摩尔/升的氢氧化钠等体积混合后(忽略混合后溶液体积的变化),所得混合溶液中存在的下列关系可能正确的是( )
A.2c(Na+)=c(X―)+c(HX)=0.2mol・L―1
B.2CX―)>c(Na+)>c(H+)>c(OH―)
C.c(Na+)-c(X―)=c(H+)-c(HX)+c(OH―)
D.c(Na+)>c(X―)>c(OH―)>c(H+)
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
科目:gzhx 来源:2013-2014学年山东省滨州市高三3月模拟(一模)考试化学试卷(解析版) 题型:填空题
X、Y、Z均是由两种短周期元素组成的无机物,它们的每个分子中均含有l8个电子,相关信息如下表所示(“/”表示相应的信息略去):
化合物 | X | Y | Z |
分子中含有的原子个数 | / | 4 | / |
摩尔质量/g·mol-l | 32 | 34 | / |
回答下列问题:
(1)X常用作火箭推进剂,其分子的球棍模型为 ,则X的化学式为 .
,则X的化学式为 .
(2)Y的化学性质描述正确的是 。
a.不稳定性 b.弱碱性 c.氧化性 d.还原性
(3)Z的化学式可用H2A表示。将一定量的Z气体通入0.05mol·L-1CuSO4溶液中,二者恰好完全反应。已知Ksp(CuA)=6.0×10-36。若不考虑溶液体积的变化,则:
①反应后溶液的pH= 。
②若反应后溶液中c(A2-)=2.0×10-30mol·L-1,则溶液中c(Cu2+)= mol·L-1。
(4)将一定量的Z气体通人NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。

①O点溶液中所含溶质的化学式为 。
②已知a点溶液呈碱性,该溶液中离子的物质的量浓度由大到小的顺序是 。
科目:gzhx 来源: 题型:
(10分)
(1)标准状况下, CO2的密度为 (保留两位小数)。
(2)标准状况下,由等物质的量的A 和B 两种气体组成的混合气体5.6L,其质量为7.5g。已知A的相对分子质量是B 的2.75 倍,则A 的摩尔质量为 。
(3)12.4gNa2X中含Na+ 0.4 mol,则X的相对原子质量为 。
(4)在标准状况下,一个装满氯气的容器的质量为74.6克,若装满氮气则重66克,那么此容器的容积为 。
(5)在一定温度和压强下,7g氯气的体积为7.5L,在同样条件下,15L某未知气体的质量8.4 g,该未知气体的相对分子质量为 。
科目:gzhx 来源:2014届河南省高一上学期第一次月考化学试卷 题型:填空题
(10分)
(1)标准状况下, CO2的密度为 (保留两位小数)。
(2)标准状况下,由等物质的量的A 和B 两种气体组成的混合气体5.6L,其质量为7.5g。已知A的相对分子质量是B 的2.75 倍,则A 的摩尔质量为 。
(3)12.4gNa2X中含Na+ 0.4 mol,则X的相对原子质量为 。
(4)在标准状况下,一个装满氯气的容器的质量为74.6克,若装满氮气则重66克,那么此容器的容积为 。
(5)在一定温度和压强下,7g氯气的体积为7.5L,在同样条件下,15L某未知气体的质量8.4 g,该未知气体的相对分子质量为 。
科目:gzhx 来源:2009年普通高等学校招生统一考试化学试题(上海卷) 题型:填空题
如果我们规定12C的相对原子质量为24,且0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),那么下列几种物理量会有变化吗?若有,请说明变化结果。
(1)一个12C原子的质量 (2)阿伏加德罗常数(NA) (3)摩尔质量
 (4)O2的相对分子质量 (5)气体摩尔体积
(4)O2的相对分子质量 (5)气体摩尔体积
(6)98%(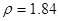 )硫酸的物质的量浓度 (7)44gCO2所含的分子个数
)硫酸的物质的量浓度 (7)44gCO2所含的分子个数
科目:gzhx 来源: 题型:
如果我们规定12C的相对原子质量为24,且0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),那么下列几种物理量会有变化吗?若有,请说明变化结果。
![]() (1)一个12C原子的质量 (2)阿伏加德罗常数(NA) (3)摩尔质量
(1)一个12C原子的质量 (2)阿伏加德罗常数(NA) (3)摩尔质量
![]() (4)O2的相对分子质量 (5)气体摩尔体积
(4)O2的相对分子质量 (5)气体摩尔体积
![]() (6)98%(
(6)98%(![]() )硫酸的物质的量浓度 (7)44gCO2所含的分子个数
)硫酸的物质的量浓度 (7)44gCO2所含的分子个数
科目:gzhx 来源: 题型:
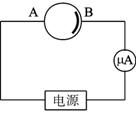
图1-6-4
制造太阳能电池需要高纯度的硅,工业上由粗硅制高纯度硅常通过以下反应实现:
①Si(s)+3HCl(g)![]() SiHCl3(g)+H2(g);ΔH=-381 kJ
SiHCl3(g)+H2(g);ΔH=-381 kJ
②SiHCl3(g)+H2(g) ![]() Si(s)+3HCl(g)
Si(s)+3HCl(g)
(1)元素硅在周期表中位于__________;晶体硅属于__________晶体,是__________ (填“导体”“半导体”或“绝缘体”);晶体硅有类似金刚石的结构,每摩尔晶体硅的共价键数目为____________________,键角为__________。
(2)关于上述条件下的两个反应的叙述不正确的是( )
A.两个反应都是置换反应 B.反应②是放热反应
C.上述反应是可逆反应 D.两个反应都是氧化还原反应
(3)反应②的热效应为____________________。
科目:gzhx 来源:2011-2012学年河南省南阳一中高一上学期第一次月考化学试卷 题型:填空题
(10分)
(1)标准状况下, CO2 的密度为 (保留两位小数)。
的密度为 (保留两位小数)。
(2)标准状况 下,由等物质的量的A 和B 两种气体组成的混合气体5.6L,其质量为7.5g。已知A的相对分子质量是B 的2.75 倍,则A 的摩尔质量为 。
下,由等物质的量的A 和B 两种气体组成的混合气体5.6L,其质量为7.5g。已知A的相对分子质量是B 的2.75 倍,则A 的摩尔质量为 。
(3)12.4gNa2X中含Na+ 0.4 mol,则X的相对原子质量为 。
(4)在标准状况下,一个装满氯气的容器 的质量为74.6克,若装满氮气则重66克,那么此容器的容积为 。
的质量为74.6克,若装满氮气则重66克,那么此容器的容积为 。
(5)在一定温度和压强下,7g氯气的体积为7.5L,在同样条件下,15L某未知气体的质量8.4 g,该未知气体的相对分子质量为 。
科目:gzhx 来源:2011-2012学年浙江省高三10月份月考化学试卷 题型:选择题
如果我们规定12C的相对原子质量为24,且0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),那么下列几种物理量没有变化的是
(1)一个12C原子的质量 (2)阿伏加德罗常数(NA) (3)摩尔质量 (4)O2的相对分子质量 (5)气体摩尔体积 (6)ag C2H5OH的物质的量
(7)98%浓硫酸的物质的量浓度 (8)44gCO2所含的分子个数
A.⑴ B.⑴⑹⑺⑻ C.⑵⑶⑷⑸ D.⑴⑻
科目:gzhx 来源:2012届浙江省金华一中高三10月份月考化学试卷 题型:单选题
如果我们规定12C的相对原子质量为24,且0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),那么下列几种物理量没有变化的是
(1)一个12C原子的质量 (2)阿伏加德罗常数(NA) (3)摩尔质量 (4)O2的相对分子质量 (5)气体摩尔体积(6)ag C2H5OH的物质的量
(7)98%浓硫酸的物质的量浓度(8)44gCO2所含的分子个数
| A.⑴ | B.⑴⑹⑺⑻ | C.⑵⑶⑷⑸ | D.⑴⑻ |
科目:gzhx 来源: 题型:
如果我们规定12C的相对原子质量为24,且0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),那么下列几种物理量会有变化吗?若有,请说明变化结果。
(1)一个12C原子的质量 (2)阿伏加德罗常数(NA)(3)摩尔质量
(4)O2的相对分子质量 (5)气体摩尔体积
(6)98%(![]() )硫酸的物质的量浓度 (7)44gCO2所含的分子个数
)硫酸的物质的量浓度 (7)44gCO2所含的分子个数
科目:gzhx 来源:2009年上海市松江区高考化学二模试卷(解析版) 题型:解答题
科目:gzhx 来源: 题型:解答题