
科目:gzhx 来源: 题型:
(1)胰岛素可能的最小相对分子质量是_________________。
(2)它的相对分子质量为5 734,每一个分子中可能有_____________个硫原子。
科目:gzhx 来源: 题型:
荷尔蒙胰岛素是一种蛋白质,含硫3.4%。
(1)胰岛素可能的最小相对分子质量是_________________。
(2)它的相对分子质量为5 734,每一个分子中可能有_____________个硫原子。
科目:gzhx 来源: 题型:
(1)胰岛素可能的最小相对分子质量为__________________________________。
(2)它的确定相对分子质量为5 734,则每一分子中可能含有____________________个硫原子。
科目:gzhx 来源: 题型:
现有100 g 3.4%的氨水,欲使其质量分数增大1倍,可采用的正确方法是( )
A.使溶液再溶解0.1 mol NH3 B.加入20.4%的浓氨水25 g
C.加热蒸发掉一半水 D.加热蒸发掉50 g H2O
科目:gzhx 来源: 题型:022
胰岛素是一种蛋白质,含硫3.4%.
(1)胰岛素可能的最小相对分子质量是____________.
(2)它的相对分子质量为5734,每一分子中可能有____________硫原子.
科目:gzhx 来源:必修二训练化学苏教版 苏教版 题型:022
荷尔蒙胰岛素是一种蛋白质,含硫3.4%.
(1)胰岛素可能的最小相对分子质量为________.
(2)它的确定相对分子质量为5734,则每一分子中可能含有________个硫原子.
科目:gzhx 来源:高考三人行 化学 题型:022
荷尔蒙胰岛素是一种蛋白质,含硫3.4%.
(1)胰岛素可能的最小相对分子质量是________.
(2)它的相对分子质量为5734,每一分子中可能有________硫原子.
科目:gzhx 来源:物理教研室 题型:022
胰岛素是一种蛋白质,含硫3.4%.
(1)胰岛素可能的最小相对分子质量是____________.
(2)它的相对分子质量为5734,每一分子中可能有____________硫原子.
科目:gzhx 来源: 题型:
(1)胰岛素可能的最小相对分子质量是_____________。
(2)它的相对分子质量为5734,每个分子中可能有____________个硫原子。
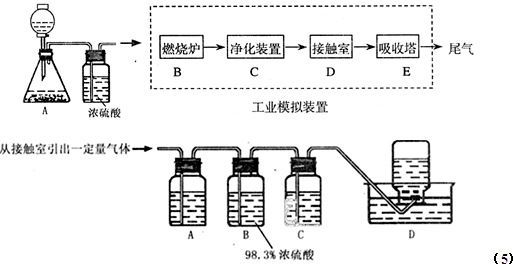
科目:gzhx 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
| 压强/Mpa 转化率 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
科目:gzhx 来源: 题型:
科目:gzhx 来源:2013-2014学年浙江省高三上学期第二次月考化学试卷(解析版) 题型:选择题
工业废气中氮的氧化物是重要的污染源,有一种治理污染的方法是通入适量氨气将其还原为无毒物质N2和H2O,现有含氮氧化物NO和NO2的混合气体3L,用相同条件下的NH3 3L恰好反应完全,则混合气中NO与NO2的体积分数比
A.l:4 B.1:3 C.l:2 D.l:l
科目:gzhx 来源: 题型:解答题

| 压强/Mpa 转化率 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
科目:gzhx 来源: 题型:
工业上用氨气与空气的混合气在一定条件下制硝酸,发生的反应是:
① 4NH3+5O2 →4NO+6H2O
![]() ② 4NO+3O2+2H2O→4HNO3
② 4NO+3O2+2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空及计算:
(1)为使氨气恰好完全氧化为一氧化氮,氨气与空气的混合气中氨的体积分数(用小数表示)为________(保留2位小数)。
(2)现将1 mol的氨气与12 mol的空气混合反应,可得到硝酸 mol;
(3)向上述溶液中加入 mL 20%的硝酸(密度为1.11g/mL),才能得到69%的硝酸溶液。
(4)现有100mol的原料气,其中含氨气为xmol,反应后生成的硝酸ymol。在得到硝酸的条件下,写出x与y的关系式。(写出解题过程)
科目:gzhx 来源:松江区二模 题型:问答题
科目:gzhx 来源:2009年上海市松江区高考化学二模试卷(解析版) 题型:解答题
科目:gzhx 来源:2009年上海市松江区高考化学模拟试卷(解析版) 题型:解答题
科目:gzhx 来源:名卷汇编(化学) 题型:013
工业废气中氮的氧化物是重要的污染源,有一种治理污染的方法是通入适量氨气将其还原为无毒物质![]() 和
和![]() ,现有含氮氧化物NO和
,现有含氮氧化物NO和![]() 的混合气体3L,用同条件下的
的混合气体3L,用同条件下的![]() 3.5L恰好反应完全,则混合气体中NO与
3.5L恰好反应完全,则混合气体中NO与![]() 的体积分数比是
的体积分数比是
[ ]
科目:gzhx 来源: 题型:解答题
科目:gzhx 来源: 题型:013
工业废气和汽车尾气排出的氮的氧化物,是空气的重要污染源,为了消除 的污染,可通入适量氨气将
的污染,可通入适量氨气将 还原为无毒物质
还原为无毒物质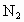 和
和 ,即:
,即:
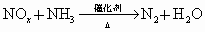
现有含氮氧化物NO与 的混合气体3.0L,用同温同压下的3.5L
的混合气体3.0L,用同温同压下的3.5L 恰好使该混合气体完全反应转化为
恰好使该混合气体完全反应转化为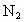 ,则混合气中NO与
,则混合气中NO与 的体积比是
的体积比是
[ ]
|
A.1:4 |
B.1:3 |
|
C.1:2 |
D.1:1 |