
科目:gzhx 来源:2011-2012学年江苏省新海高级中学高一下学期期中考试化学试卷(带解析) 题型:填空题
(12分)化学反应速率与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 50 | 120 | 232 | 288 | 310 |

科目:gzhx 来源:2011-2012学年重庆市高三9月月考理科综合试题(化学部分) 题型:填空题
(16分)(1)已知:还原性HSO3->I-,氧化性IO3->I2。在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O
①配平上述反应的化学方程式(将化学计量数填在方框内);并写出其氧化产物____________。
②在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为____________ (填化学式);
(2)向某密闭容器中加人0.15 mol/L A、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c(B)未画出,t1时增大到0.05 mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。

①若t4时改变的条件为减小压强,则B的起始物质的量浓度为________mol/L;
②若t1=15 s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=_______mol/(L·s)。
③t3时改变的某一反应条件可能是_______(选填序号)。
a使用催化剂 b增大压强 c增大反应物浓度
④有甲、乙两个容积均为2L的密闭容器,在控制两容器温度相同且恒定情况下,向甲中通入3mol A,达到平衡时,B的体积分数为20%,则向乙容器中充入1 mol C和0.5mol B,达到平衡时,C的浓度c(C)=________
科目:gzhx 来源: 题型:
(12分)化学反应速率与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 50 | 120 | 232 | 288 | 310 |
① 哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最小 ,
原因是 。
② 哪一时间段的反应速率最大 ,原因是 。
③ 求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率 。
(设溶液体积不变)
④ 如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他可采取的措施是 :
A.加蒸馏水 B.加Na2CO3溶液 C.加NaCl溶液 D.加NaNO3溶液
(2)已知某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。该反应的化学方程式为: 。
科目:gzhx 来源:2011-2012学年河北省保定市高三上学期期末调研考试理科综合化学试卷(解析版) 题型:填空题
(1分)W、X、Y、Z、L、M为元索周期表中原子序数依次增大的短周期元素。
已知:①X的单质在Z2中燃烧可生成XZ和XZ2两种气体;
②L是一种金屑单质,该金属与Z2反应可生成L2Z和L2Z2两种固体;
③M的单质在Z2中燃烧的产物可使品红溶液褪色,加热后恢复原色;
请回答下列问题:
(1) 写出L2Z的电子式________
(2) 写出L2Z2与XZ2气体反应的化学方程式________________________________
(3) X、Y、Z分别与W可形成10电子化合物,这三种化合物中沸点最髙的是(填化学式)________________, W、Y、Z可形成离子化合物W4Y2Z3,其水溶液中各离子浓度由大到小的顺序为________________________, W2Z2与FeSO4混合溶于稀硫酸中,反应的离子方程式为________________________________________;
(4) 在容积为2L的密闭容器中加人0.48mol MZ2和0.22mol Z2, —定温度下反应达到平衡时得到0. 24 mol MZ3,则反应的化学平衡常数K=________,若温度不变,再加人0.50 mol Z2后重新达到平衡,则Z2的转化率________ (填“升高”、“不变”或“降低”),MZ3的体积分数________ (填“增大”、“不变”或“减小”)。
科目:gzhx 来源: 题型:
(1分)W、X、Y、Z、L、M为元索周期表中原子序数依次增大的短周期元素。
已知:①X的单质在Z2中燃烧可生成XZ和XZ2两种气体;
②L是一种金屑单质,该金属与Z2反应可生成L2Z和L2Z2两种固体;
③M的单质在Z2中燃烧的产物可使品红溶液褪色,加热后恢复原色;
请回答下列问题:
(1) 写出L2Z的电子式________
(2) 写出L2Z2与XZ2气体反应的化学方程式________________________________
(3) X、Y、Z分别与W可形成10电子化合物,这三种化合物中沸点最髙的是(填化学式)________________, W、Y、Z可形成离子化合物W4Y2Z3,其水溶液中各离子浓度由大到小的顺序为________________________, W2Z2与FeSO4混合溶于稀硫酸中,反应的离子方程式为________________________________________;
(4) 在容积为2L的密闭容器中加人0.48molMZ2和0.22mol Z2,—定温度下反应达到平衡时得到0. 24 mol MZ3,则反应的化学平衡常数K=________,若温度不变,再加人0.50 mol Z2后重新达到平衡,则Z2的转化率________ (填“升高”、“不变”或“降低”),MZ3的体积分数________ (填“增大”、“不变”或“减小”)。
科目:gzhx 来源:2012届河北省保定市高三上学期期末调研考试理科综合化学试卷(解析版) 题型:填空题
(1分)W、X、Y、Z、L、M为元索周期表中原子序数依次增大的短周期元素。
已知:①X的单质在Z2中燃烧可生成XZ和XZ2两种气体;
②L是一种金屑单质,该金属与Z2反应可生成L2Z和L2Z2两种固体;
③M的单质在Z2中燃烧的产物可使品红溶液褪色,加热后恢复原色;
请回答下列问题:
(1) 写出L2Z的电子式________
(2) 写出L2Z2与XZ2气体反应的化学方程式________________________________
(3) X、Y、Z分别与W可形成10电子化合物,这三种化合物中沸点最髙的是(填化学式)________________, W、Y、Z可形成离子化合物W4Y2Z3,其水溶液中各离子浓度由大到小的顺序为________________________, W2Z2与FeSO4混合溶于稀硫酸中,反应的离子方程式为________________________________________;
(4) 在容积为2L的密闭容器中加人0.48mol MZ2和0.22mol Z2, —定温度下反应达到平衡时得到0. 24 mol MZ3,则反应的化学平衡常数K=________,若温度不变,再加人0.50 mol Z2后重新达到平衡,则Z2的转化率________ (填“升高”、“不变”或“降低”),MZ3的体积分数________ (填“增大”、“不变”或“减小”)。
科目:gzhx 来源:2014届江苏省高一下学期期中考试化学试卷(解析版) 题型:填空题
(12分)化学反应速率与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
|
时间(min) |
1 |
2 |
3 |
4 |
5 |
|
氢气体积(mL)(标准状况) |
50 |
120 |
232 |
288 |
310 |
① 哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最小 ,
原因是 。
② 哪一时间段的反应速率最大 ,原因是 。
③ 求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率 。
(设溶液体积不变)
④ 如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他可采取的措施是 :
A.加蒸馏水 B.加Na2CO3溶液 C.加NaCl溶液 D.加NaNO3溶液
(2)已知某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。该反应的化学方程式为: 。

科目:gzhx 来源: 题型:
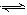
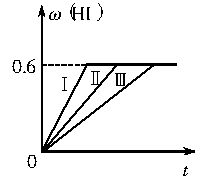 2HI(g)(正反应方向为放热反应),并达到平衡。HI的体积分数ω(HI)随时间的变化关系如曲线Ⅱ所示。试回答:
2HI(g)(正反应方向为放热反应),并达到平衡。HI的体积分数ω(HI)随时间的变化关系如曲线Ⅱ所示。试回答:科目:gzhx 来源:海门市2007学年第一学期高三第一次诊断考试、化学试卷 题型:022
| |||||||||||||||
科目:gzhx 来源:东莞市塘厦中学2007届高三月考(二)、九月月考化学试题(人教) 人教 题型:022
| |||||||||||||
科目:gzhx 来源:2012届重庆市南开中学高三9月月考理科综合试题(化学部分) 题型:填空题
(16分)(1)已知:还原性HSO3->I-,氧化性IO3->I2。在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O
①配平上述反应的化学方程式(将化学计量数填在方框内);并写出其氧化产物____________。
②在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为____________ (填化学式);
(2)向某密闭容器中加人0.15 mol/L A、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c(B)未画出,t1时增大到0.05 mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
①若t4时改变的条件为减小压强,则B的起始物质的量浓度为________mol/L;
②若t1="15" s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=_______mol/(L·s)。
③t3时改变的某一反应条件可能是_______(选填序号)。
a使用 催化剂 b增大压强 c增大反应物浓度
催化剂 b增大压强 c增大反应物浓度
④有甲、乙两个容积均为2L的密闭容器,在控制两容器温度相同且恒定情况下,向甲中通入3mol A,达到平衡时,B的体积分数为20%,则向乙容器中充入1 mol C和0.5mol B,达到平衡时,C的浓度c(C)=________
科目:gzhx 来源: 题型:
(16分)(1)已知:还原性HSO3->I-,氧化性IO3->I2。在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O
①配平上述反应的化学方程式(将化学计量数填在方框内);并写出其氧化产物____________。
②在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为____________ (填化学式);
(2)向某密闭容器中加人0.15 mol/L A、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c(B)未画出,t1时增大到0.05mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
①若t4时改变的条件为减小压强,则B的起始物质的量浓度为________mol/L;
②若t1=15 s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=_______mol/(L·s)。
③t3时改变的某一反应条件可能是_______(选填序号)。
a使用催化剂 b增大压强 c增大反应物浓度
④有甲、乙两个容积均为2L的密闭容器,在控制两容器温度相同且恒定情况下,向甲中通入3mol A,达到平衡时,B的体积分数为20%,则向乙容器中充入1 mol C和0.5mol B,达到平衡时,C的浓度c(C)=________
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
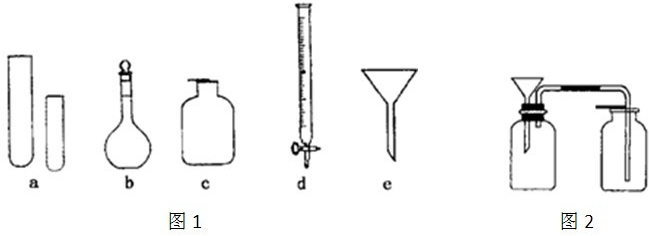
| 仪器编号 | a | b | c | d | e |
| 名称 | 试管 | 溶量瓶 | 集气瓶 | 碱式滴定管 | 普通漏斗 |
| 改正的名称 | 无 无 |
容量瓶 容量瓶 |
无 无 |
酸式滴定管 酸式滴定管 |
无 无 |
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
 某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示.由图中数据分析:
某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示.由图中数据分析: 2Z
2Z 2Z
2Z科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
 2L容器中,分别将物质的量均为2.00mol的SO2、O2混合,在不同温度(T)下发生如下反应:2SO2(g)+O2(g)⇌2SO3(g).并在第10s时分别测定其中SO3的物质的量分数(SO3%)并绘成如图所示曲线:
2L容器中,分别将物质的量均为2.00mol的SO2、O2混合,在不同温度(T)下发生如下反应:2SO2(g)+O2(g)⇌2SO3(g).并在第10s时分别测定其中SO3的物质的量分数(SO3%)并绘成如图所示曲线:. | v |
科目:gzhx 来源: 题型:
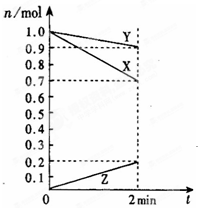 (1)某温度时,在2L容器中,X、Y、Z三种物质的物质的 量随时间变化曲线如图所示.由图中数据分析,该反应的 化学方程式为:
(1)某温度时,在2L容器中,X、Y、Z三种物质的物质的 量随时间变化曲线如图所示.由图中数据分析,该反应的 化学方程式为: