科目:czhx 来源: 题型:
| ||
| ||
科目:gzhx 来源:2016届西藏日喀则一中高三下学期二模考试理综化学试卷(解析版) 题型:实验题
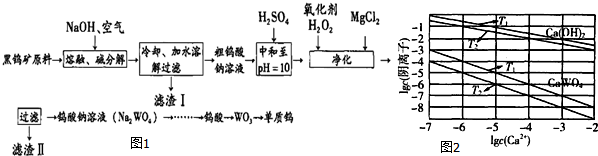
钨是熔点最高的金属,是重要的战略物资.自然界中钨矿石的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含少量Si、P、As的化合物.由黑钨矿冶炼钨的工艺流程如图:

已知:①滤渣I的主要成份是Fe2O3、MnO2.
②上述流程中,除最后一步外,其余步骤钨的化合价未变.
③常温下钨酸难溶于水.
回答下列问题:
(1)钨酸盐(FeWO4、MnWO4)中钨元素的化合价为__________,请写出MnWO4在熔融条件下发生碱分解反应生成MnO2的化学方程式__________。
(2)上述流程中向粗钨酸钠溶液中加硫酸调pH=10后,溶液中的杂质阴离子确SiO32-、HAsO32-、HAsO42-、HPO42-等,则“净化”过程中,加入H2O2时发生反应的离子方程式为__________,滤渣Ⅱ的主要成分是__________。
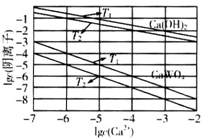
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小.图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线,则T1时Ksp(CaWO4)=__________mol•L-1.将钨酸钠溶液加入石灰乳得到大量钨酸钙,发生反应的离子方程式为__________,T2时该反应的平衡常数为__________mol•L-1。
(4)硬质合金刀具中含碳化钨(WC),利用电解法可以从碳化钨废料中回收钨.电解时,用碳化钨做阳极,不锈钢做阴极,HCl溶液为电解液,阳极析出钨酸并放出CO2.该阳极反应式为__________。

科目:gzhx 来源: 题型:解答题

科目:gzhx 来源: 题型:解答题
科目:czhx 来源: 题型:

科目:czhx 来源:2014-2015学年江苏省南通市崇川区九年级3月月考化学试卷(解析版) 题型:探究题
(16分)发酵粉的主要成分中含有碳酸氢钠。某化学兴趣小组的同学对碳酸氢钠的性质进行了探究。
Ⅰ.定性探究
实验一:探究碳酸氢钠溶液的酸碱性
用pH试纸测得碳酸氢钠溶液的pH约为8,可知碳酸氢钠溶液呈 性。
实验二:探究碳酸氢钠的热稳定性
【查阅资料】碳酸氢钠受热容易分解,生成水、一种气体和一种常见的固体物质。
【实验1】取一定质量的碳酸氢钠放到铜片上加热,如图所示。

(1)加热一段时间后,观察到烧杯内壁有水珠。
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊,说明该气体是 。
(3)欲通过进一步的实验探究来确定充分加热后的固体产物的成分。
【提出假设】①可能是Na2CO3
②可能是NaOH
③可能是 。
【实验2】
实验操作 | 实验现象 | 实验结论 |
A.将该固体溶于蒸馏水配制成溶液,取少量溶液于试 管中,滴加足量稀盐酸 | 有气体产生 | 假设 (填序号)不成立 |
B.另取少量溶液于试管中,滴加 溶液 | 固体产物中有 Na2CO3 | |
C.取上述B步骤静置后所得上层清液,滴入少量 溶液 | 无明显现象 | 假设①成立 |
【实验结论】NaHCO3受热分解的化学方程式为 。
【延伸拓展】实验室有两瓶失去标签的固体药品,已知它们是碳酸钠和碳酸氢钠,你能否设计一个实验进行鉴别,请简述你的实验方案及现象和结论 。。
Ⅱ.定量探究
为测定某发酵粉中碳酸氢钠的质量分数,设计了如下实验,其主要实验步骤如下:
①按下图组装仪器,取50g样品放入锥形瓶中,关闭活塞b,打开活塞a,从导管A处缓缓鼓入一定量的空气;

②关闭活塞a,打开活塞b,加入足量稀硫酸溶液,直至锥形瓶内不再产生气泡;
③关闭活塞b,打开活塞a,从导管A处缓缓鼓入一定量的空气;
④测量干燥管内碱石灰(氧化钙和氢氧化钠固体的混合物)增加的质量(见上图曲线);
⑤重复步骤③和④的操作,直至干燥管内物质质量不再增加。
(1)步骤①加入样品前还应 。
(2)装置甲的作用是 ,装置乙的作用是 ;
(3)请利用相关数据计算样品中碳酸氢钠的质量分数。(写出计算过程)
科目:czhx 来源: 题型:

科目:czhx 来源: 题型:
水在实验室和日常生活中有很多用途。
I、溶液是日常生活中的常见物质,水是最常用的溶剂。
20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图 2,甲、乙两种物质的溶解度曲线如图3。请结合图示回答下列问题:
2,甲、乙两种物质的溶解度曲线如图3。请结合图示回答下列问题:
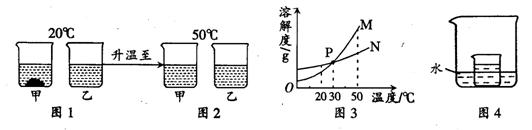
(1)图1中一定为饱和溶液的是 ▲
(2)图3中表示乙的溶解度曲线是 ▲ ;P点表示的含义是 ▲ 。
(3)在图4所示的实验中,小烧杯内盛放的是20℃时甲物质的饱和溶液。某同学要使小烧杯内有固体析出时,他应向大烧杯的水中加入下列物质中的 ▲ (填字母)。
A.氧化钙 B.氯化钠 C.氢氧化钠 D.硝酸铵
Ⅱ、水在工业生产中也很重要。
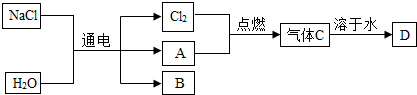
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。电解饱和食盐水可以得到多种化工产品,主要过程如下:
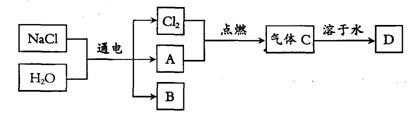
[资料 卡:石灰水中的溶质是一种碱——Ca(OH)2]
卡:石灰水中的溶质是一种碱——Ca(OH)2]
(4)已知气体A是密度最小的气体,B是一种碱,D是一种酸。写出金属铝和酸D反应生成气体A的化学方程式: ▲ 。
(5)B的化学式为 ▲ 。
(6)工业上电解食盐水是在立式隔膜电解槽中进行,产生的Cl2和气体A在两处逸出并分别收集、储存。
①已知20℃,S(NaCl)=36g,则室温下,68 kg饱和食盐水中溶质的质量为 ▲ 。
②电解一段时间,当收集到氯气的质量为0.71 kg时,列式计算生成的B的质量。
▲ 。
③0.71 kg氯气和A完全反应生成气体C,溶于一定量的水中形成酸D。若酸D中的溶质质量分数为36.5%,则其中水的质量为 ▲ 。
科目:czhx 来源: 题型:
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 名 称 | 食 醋 | 白 酒 | 白糖水 | 石灰水 | 纯碱溶液 |
| 主要成分 | CH3COOH | C2H5OH | C12H22O11 | Ca(OH)2 | Na2CO3 |
| 溶液pH | 3 | 7 | 7 | 11 | 8 |

科目:czhx 来源:2013届天津市红桥区九年级上学期期末考试化学试卷 题型:填空题
化学来源于生活又服务于生活。下表是生活中常用物质溶液的pH及主要成分化学式:
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 名 称 | 食 醋 | 白 酒 | 白糖水 | 石灰水 | 纯碱溶液 |
| 主要成分 | CH3COOH | C2H5OH | C12H22O11 | Ca(OH)2 | Na2CO3 |
| 溶液pH | 3 | 7 | 7 | 11 | 8 |
科目:czhx 来源:2012-2013学年天津市红桥区九年级上学期期末考试化学试卷(解析版)(解析版) 题型:填空题
化学来源于生活又服务于生活。下表是生活中常用物质溶液的pH及主要成分化学式:
|
序号 |
① |
② |
③ |
④ |
⑤ |
|
名 称 |
食 醋 |
白 酒 |
白糖水 |
石灰水 |
纯碱溶液 |
|
主要成分 |
CH3COOH |
C2H5OH |
C12H22O11 |
Ca(OH)2 |
Na2CO3 |
|
溶液pH |
3 |
7 |
7 |
11 |
8 |
(1)上述物质中,碱性最强的是 (填序号);
(2)当你被蚊虫叮咬(释放一种酸性物质)后,为减轻疼痛,可在叮咬处涂 (填序号);
(3)水垢的主要成分是碳酸钙和氢氧化镁,可用醋酸(食醋的主要成分)溶解除去。已知醋酸与氢氧化镁反应的化学方程式为:2CH3COOH + Mg(OH)2 = (CH3COO)2Mg +2H2O ,则醋酸与碳酸钙反应的化学方程式是 。
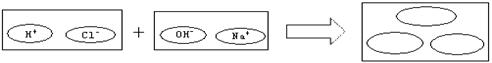
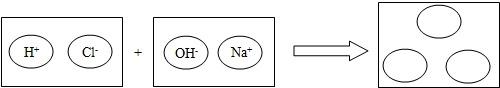
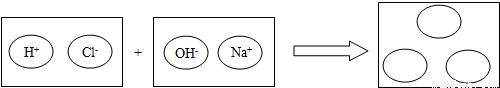
(4)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了下图。请你在右边的圆圈中填入适当的化学式或离子符号:
科目:czhx 来源: 题型:解答题
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 名 称 | 食 醋 | 白 酒 | 白糖水 | 石灰水 | 纯碱溶液 |
| 主要成分 | CH3COOH | C2H5OH | C12H22O11 | Ca(OH)2 | Na2CO3 |
| 溶液pH | 3 | 7 | 7 | 11 | 8 |
科目:czhx 来源:2011-2012学年重庆一中九年级(下)期中化学试卷(解析版) 题型:填空题
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 名 称 | 食 醋 | 白 酒 | 白糖水 | 石灰水 | 纯碱溶液 |
| 主要成分 | CH3COOH | C2H5OH | C12H22O11 | Ca(OH)2 | Na2CO3 |
| 溶液pH | 3 | 7 | 7 | 11 | 8 |

科目:czhx 来源:2012-2013学年天津市红桥区九年级(上)期末化学试卷(解析版) 题型:填空题
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 名 称 | 食 醋 | 白 酒 | 白糖水 | 石灰水 | 纯碱溶液 |
| 主要成分 | CH3COOH | C2H5OH | C12H22O11 | Ca(OH)2 | Na2CO3 |
| 溶液pH | 3 | 7 | 7 | 11 | 8 |

科目:czhx 来源:2011-2012学年重庆市岩口复兴学校九年级(下)月考化学试卷(4月份)(解析版) 题型:填空题
| 序号 | ① | ② | ③ | ④ | ⑤ |
| 名 称 | 食 醋 | 白 酒 | 白糖水 | 石灰水 | 纯碱溶液 |
| 主要成分 | CH3COOH | C2H5OH | C12H22O11 | Ca(OH)2 | Na2CO3 |
| 溶液pH | 3 | 7 | 7 | 11 | 8 |
科目:czhx 来源: 题型:

科目:czhx 来源: 题型:解答题
科目:czhx 来源: 题型:阅读理解
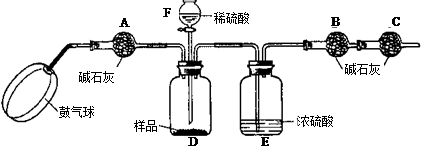
节约资源和保护环境已经成为我们的基本国策。节能减排、环境保护和生态市建设是市政府近些年的工作重点。硫酸厂生产硫酸的流程是:把含硫矿物燃烧,生成二氧化硫,二氧化硫和氧气在高温和催化剂的作用生成三氧化硫,最后三氧化硫和水化合生成硫酸。写出三氧化硫和水化合生成硫酸的化学方程式
某纯碱样品中含有少量硫酸钠,现欲测定其碳酸钠的质量分数,利用含有少量硫酸的澄清废水进行如下实验:
《实验原理》Na2CO3+H2SO4= Na2SO4 + H2O + CO2↑通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》

《实验步骤》
①如图连接装置(除B、C外)并加入所需药品。
②称量并记录B的质量(m1)。(称量时注意封闭B的两端。)
③按动鼓气球,持续鼓入空气约1分钟。
④连接上B、C。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)
⑧计算。
⑴已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是: ,以免使测定结果偏大。
(2) (能或不能)用稀盐酸代替稀硫酸,因为盐酸具有 性,会使测得碳酸钠的质量分数 (填偏大、偏小或不变,下同);若去除干燥管C,则测得碳酸钠的质量分数将会
(3)E装置的作用是
(4)本实验能否省略③、⑥两个步骤? (填能或不能),原因分别是 、
(5)若所取样品的质量为6g,分液漏斗F中盛放5%只含硫酸一种溶质的澄清废水,称得m1为51.20g,m2为53.40g,(计算结果保留两位小数)
求:(1)样品中碳酸钠的质量分数为多少?
(2)D装置中正好反应后,所得溶液的溶质质量分数是多少?
科目:czhx 来源: 题型:阅读理解
节约资源和保护环境已经成为我们的基本国策。节能减排、环境保护和生态市建设是市政府近些年的工作重点。硫酸厂生产硫酸的流程是:把含硫矿物燃烧,生成二氧化硫,二氧化硫和氧气在高温和催化剂的作用生成三氧化硫,最后三氧化硫和水化合生成硫酸。写出三氧化硫和水化合生成硫酸的化学方程式
某纯碱样品中含有少量硫酸钠,现欲测定其碳酸钠的质量分数,利用含有少量硫酸的澄清废水进行如下实验:
《实验原理》Na2CO3+H2SO4= Na2SO4 + H2O + CO2↑通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》
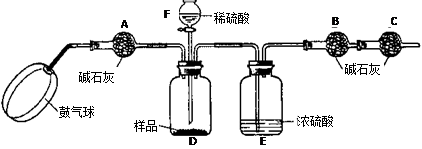
《实验步骤》
①如图连接装置(除B、C外)并加入所需药品。
②称量并记录B的质量(m1)。(称量时注意封闭B的两端。)
③按动鼓气球,持续鼓入空气约1分钟。
④连接上B、C。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)
⑧计算。
⑴已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是: ,以免使测定结果偏大。
(2) (能或不能)用稀盐酸代替稀硫酸,因为盐酸具有 性,会使测得碳酸钠的质量分数 (填偏大、偏小或不变,下同);若去除干燥管C,则测得碳酸钠的质量分数将会
(3)E装置的作用是
(4)本实验能否省略③、⑥两个步骤? (填能或不能),原因分别是 、
(5)若所取样品的质量为6g,分液漏斗F中盛放5%只含硫酸一种溶质的澄清废水,称得m1为51.20g,m2为53.40g,(计算结果保留两位小数)
求:(1)样品中碳酸钠的质量分数为多少?
(2)D装置中正好反应后,所得溶液的溶质质量分数是多少?
科目:czhx 来源: 题型:阅读理解