
科目:gzhx 来源:浙江省模拟题 题型:填空题
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)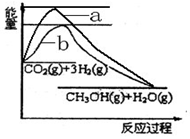
科目:czhx 来源: 题型:
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 | ||
| 实验2 | a | MnO2 0.5 |
| ||
| △ |
| ||
| ||
科目:czhx 来源: 题型:
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 | ||
| 实验2 | a | MnO2 0.5 |
| ||
| ||
| ||
科目:gzhx 来源: 题型:
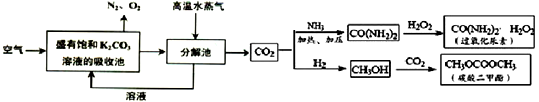
 原子序数之和为16的三种短周期元素的单质X、Y、Z,常温常压下均为无色气体,在适当条件下X、Y、Z之间可以发生如右图所示的变化.
原子序数之和为16的三种短周期元素的单质X、Y、Z,常温常压下均为无色气体,在适当条件下X、Y、Z之间可以发生如右图所示的变化.

| ||
| △ |
| ||
| △ |
科目:gzhx 来源: 题型:
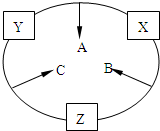 原子序数之和为16的三种短周期元素的单质X、Y、Z,常温常压下均为无色气体,在适当条件下X、Y、Z之间可以发生如右图所示的变化.已知B分子组成中Z原子
原子序数之和为16的三种短周期元素的单质X、Y、Z,常温常压下均为无色气体,在适当条件下X、Y、Z之间可以发生如右图所示的变化.已知B分子组成中Z原子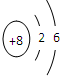
| ||
| △ |
| ||
| △ |
 NH4++OH-
NH4++OH- NH4++OH-
NH4++OH-
| ||
| ||
科目:czhx 来源:2013-2014学年江苏省淮安市金湖县九年级上学期期中考试化学试卷(解析版) 题型:选择题
催化转化器可将汽车尾气中的有毒气体转化为无毒气体,发生反应的微观示意图为:

下列从图示所获得的信息中,正确的是( )
A.图中有三种不同的氧化物
B.该反应中分子和原子的种类都发生了改变
C.反应过程中没有单质生成
D.反应前后各元素化合价不变
科目:czhx 来源: 题型:解答题
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 | ||
| 实验2 | a | MnO2 0.5 |
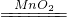 2KCl+3O2↑.已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空.
2KCl+3O2↑.已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空. 2KMnO4+Cl2↑+O2↑;
2KMnO4+Cl2↑+O2↑; 2KCl+MnO2+O2↑.
2KCl+MnO2+O2↑.
科目:czhx 来源:不详 题型:问答题
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 | ||
| 实验2 | a | MnO2 0.5 |
| ||
| ||
| ||
科目:czhx 来源: 题型:
催化剂在科研、医药生产和电子工业等前沿领域有着广泛应用。
(1)为探究二氧化锰对氯酸钾分解的催化作用。在相同条件下,同学们按下表进行实验并记录相关数据。(其他影响实验的因素均相同)
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 |
| |
| 实验2 | a | MnO2 0.5 |
① 表中a的数值应是 。
② 表中的待测数据指 (填字母序号)。
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
 ③ 设计“实验1”的目的是 。
③ 设计“实验1”的目的是 。
(2)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应。
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3====2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
![]() (I) 2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(I) 2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(II) (用化学方程式表示);
![]() (III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
(III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应。
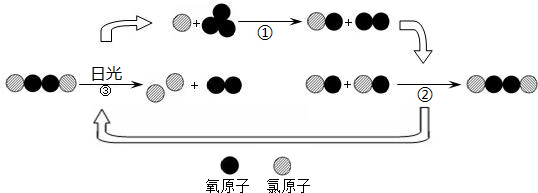
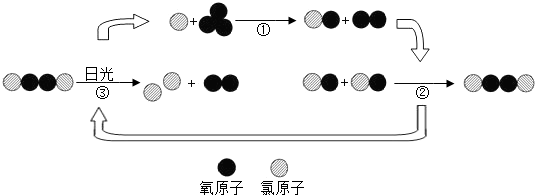
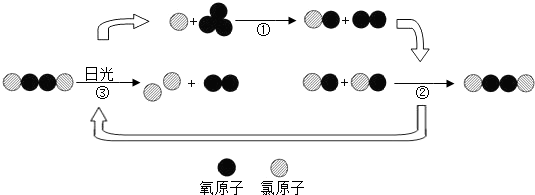
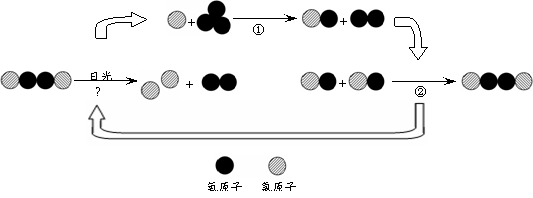
【拓展】氟利昂释放出的氯原子参与了臭氧层的破坏,其微观示意图如下:
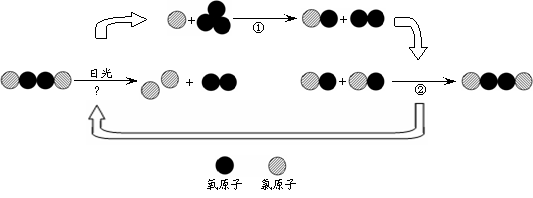 |
综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式 。
科目:czhx 来源: 题型:
催化剂在科研、医药生产和电子工业等前沿领域有着广泛应用。
(1)为探究二氧化锰对氯酸钾分解的催化作用。在相同条件下,同学们按下表进行实验并记录相关数据。(其他影响实验的因素均相同)
编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
实验1 | 2.0 |
| |
实验2 | a | MnO2 0.5 |
① 表中a的数值应是 。
② 表中的待测数据指 (填字母序号)。
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
③ 设计“实验1”的目的是 。
(2)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应。
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3== ==2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
==2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
![]() (I) 2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(I) 2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(II) (用化学方程式表示);
![]() (III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
(III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应。
【拓展】氟利昂释放出的氯原子参与了臭氧层的破坏,其微观示意图如下:
 |
综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式 。
科目:czhx 来源: 题型:
催化剂在科研、医药生产和电子工业等前沿领域有着广泛应用。
(1)为探究二氧化锰对氯酸钾分解的催化作用。在相同条件下,同学们按下表进行实验并记录相关数据。(其他影响实验的因素均相同)
编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
实验1 | 2.0 |
| |
实验2 | a | MnO2 0.5 |
① 表中a的数值应是 。
② 表中的待测数据指 (填字母序号)。
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
③ 设计“实验1”的目的是 。
(2)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应。
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3= ===2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
===2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
(I) 2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(II) (用化学方程式表示);
(III)K2MnO4 + Cl2==![]() =2KCl + MnO2 + O2↑。
=2KCl + MnO2 + O2↑。
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应。
【拓展】氟利昂释放出的氯原子参与了臭氧层的破坏,其微观示意图如下:
 |
综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式 。
科目:czhx 来源:2012-2013学年新人教版九年级(上)期末化学模拟试卷(8)(解析版) 题型:填空题
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 | ||
| 实验2 | a | MnO2 0.5 |
 2KCl+3O2↑.
2KCl+3O2↑. 2KMnO4+Cl2↑+O2↑;
2KMnO4+Cl2↑+O2↑; 2KCl+MnO2+O2↑.
2KCl+MnO2+O2↑.
科目:czhx 来源:2011年安徽省中考化学导向预测模拟试卷(一)(解析版) 题型:填空题
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 | ||
| 实验2 | a | MnO2 0.5 |
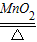 2KCl+3O2↑.
2KCl+3O2↑.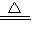 2KMnO4+Cl2↑+O2↑;
2KMnO4+Cl2↑+O2↑;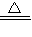 2KCl+MnO2+O2↑.
2KCl+MnO2+O2↑.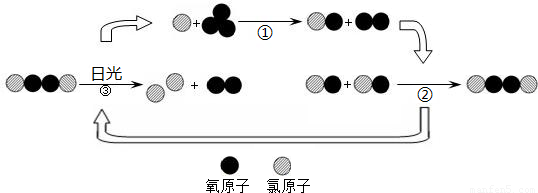
科目:czhx 来源:不详 题型:单选题

| A.图中有三种不同的氧化物 |
| B.该反应中分子和原子的种类都发生了改变 |
| C.反应过程中没有单质生成 |
| D.反应前后各元素化合价不变 |
科目:czhx 来源: 题型:
催化剂在生产、生活和科研中有重要作用。实验室用过氧化氢分解制氧气,常用MnO2作催化剂。
【提出问题】其他物质能代替MnO2作过氧化氢分解的催化剂吗?
【猜 想】甲同学认为CuO或Fe2O3可以代替MnO2,因为按 物质的简单分类MnO2、CuO、 Fe2O3都属于 。
物质的简单分类MnO2、CuO、 Fe2O3都属于 。
【设计实验】甲同 学按下面步骤进行实验:
学按下面步骤进行实验:
①在试管中加入5 mL 5%的过氧化氢溶液,把带火星的木条伸入试管;
②用精密的天平准确称量0.5 g Fe2O3红色粉末,并将其加入另一试管中;
③在步骤②的试管中加入5 mL 5%的过氧化氢溶液,把带火星的木条伸入试管;
④待步骤③的试管中没有气泡后,进行“某一操作”,得到红色固体,将固体洗净、干燥、称量,得红色固体的质量仍为0.5 g。
【现 象】甲同学观察到步骤①中的现象为 ,步骤③中带火星的木条复燃。
【反 思】步骤④中进行的“某一操作 ”是 。乙同学认为在步骤④后必需增加一个实验,请你写出增加这个实验的目的
”是 。乙同学认为在步骤④后必需增加一个实验,请你写出增加这个实验的目的  。
。
【结 论】通过以上实验步骤得出的结论是Fe2O3红色粉末是过氧化氢分解的催化剂 。
。
请根据三氧化二铁的化学式进行计算;(相对原子质量:Fe-56 O-16)
(1)Fe2O3的相对分子质量为 ;
(2)Fe2O3中铁元素和氧元素的质量比为 ;
(3)160gFe2O3中含有 g铁元素。
科目:czhx 来源: 题型:
科目:czhx 来源: 题型:

汽车安装使用催化净化装置是减少汽车尾气对空气污染有效方法之一。其主要发生的化学方程式为: 2NO+2CO 2CO2+N2。下列对该化学反应的说法不正确的是
A.反应物都属于氧化物
B.该反应使有害气体转化为无害物质
C.反应前后元素的种类、原子和分子个数都不变
D.化学方程式所表示的反应物和生成物中只有一种物质是单质
科目:gzhx 来源: 题型:
| ||
| △ |

| ||
科目:gzhx 来源: 题型:

 ”表示),原子分布如图二所示,该物质的化学式为
”表示),原子分布如图二所示,该物质的化学式为科目:gzhx 来源: 题型: