
科目:gzdl 来源: 题型:
我国已将控制酸雨和二氧化硫污染纳入《中华人民共和国大气污染防治法》,并提出了两控区(酸雨控制区和二氧化
硫污染控制区)酸雨和二氧化硫污染控制目标。根据下述资料,结合所学知识,回答⑴~⑷。
资料一:煤炭、石油以及金属冶炼等过程中产生的二氧化硫、氮氧化物,溶解在大气水中,以雨水、冻雨、雪、雹、
露等形式降到地面即成为酸雨,其pH值小于5.6,主要分硫酸型和硝酸型两类。
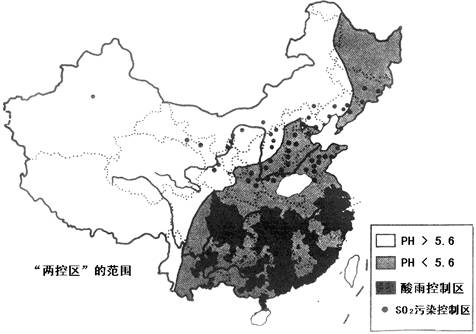
资料二:“两控区”的范围分布图
资料三:各种二氧化硫减排费用的比较表
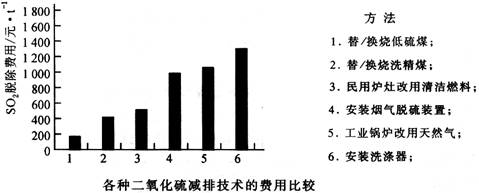
⑴ 我国各地环境问题表现同中有异,图中非控区主要表现为 ,而“两控区”又表现出比较严重的 。
⑵ 有关我国“两控区”对象的说法,正确的有 (填正确项字母)。
A.二氧化硫污染多集中于城市
B.二氧化硫只污染于北部,酸雨只影响到东部
C.我国酸雨主要属硫酸型
D.酸雨会酸化河湖,腐蚀建筑
E.大量工业锅炉改用天然气比较适合我国国情
F.酸雨区与酸性气体排源地一致
⑶ 我国南方酸雨强度比北方 ,其主要原因是 。
⑷ 防治酸雨可采取哪些措施?
科目:gzdl 来源: 题型:
我国已将控制酸雨和二氧化硫污染纳入《中华人民共和国大气污染防治法》,并提出了两控区(酸雨控制区和二氧化硫污染控制区)酸雨和二氧化硫污染控制目标。根据下述资料,结合所学知识,回答⑴~⑷。
资料一:煤炭、石油以及金属冶炼等过程中产生的二氧化硫、氮氧化物,溶解在大气水中,以雨水、冻雨、雪、雹、露等形式降到地面即成为酸雨,其pH值小于5.6,主要分硫酸型和硝酸型两类。
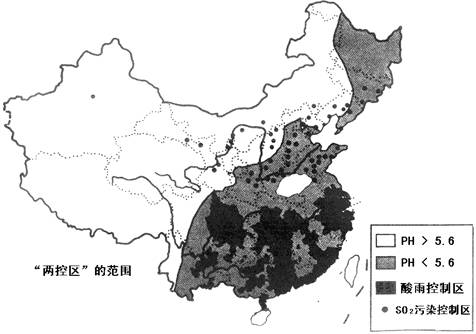
资料二:“两控区”的范围分布图
资料三:各种二氧化硫减排费用的比较表
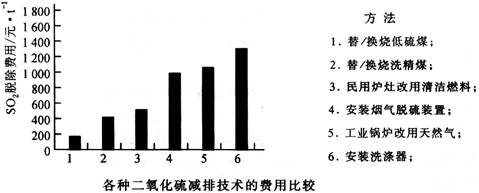
⑴ 我国各地环境问题表现同中有异,图中非控区主要表现为 ,而“两控区”又表现出比较严重的 。
⑵ 有关我国“两控区”对象的说法,正确的有 (填正确项字母)。
A.二氧化硫污染多集中于城市
B.二氧化硫只污染于北部,酸雨只影响到东部
C.我国酸雨主要属硫酸型
D.酸雨会酸化河湖,腐蚀建筑
E.大量工业锅炉改用天然气比较适合我国国情
F.酸雨区与酸性气体排源地一致
⑶ 我国南方酸雨强度比北方 ,其主要原因是
⑷ 防治酸雨可采取哪些措施?
科目:gzhx 来源:上海市长宁区2011届高三上学期期末质量调研化学试题 题型:058
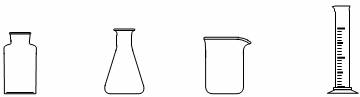
印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.测得某废腐蚀液中含CuCl2 1.5 mol/L、FeCl2 3.0 mol/L、FeCl3 1.0 mol/L、HCl 3.0 mol/L.取废腐蚀液200 mL按如下流程在实验室进行实验:

回答下列问题:
(1)操作1的名称是________,上述方法获得的铜粉中含有杂质,除杂所需试剂是________(填化学式).
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为________.
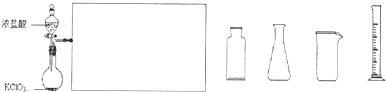
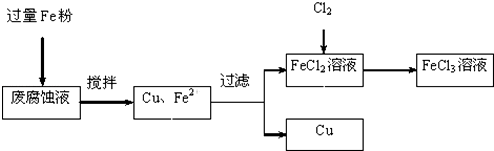
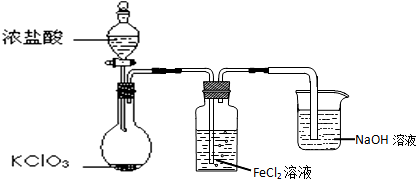
(3)下图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置.

从下图挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管.固定装置不用画),并标明容器中所装试剂.

(4)实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收.控制生成氯气速度的操作是:________________.
(5)按上述流程操作,需称取Fe粉的质量应不少于________g(精确到0.1 g),需通入Cl2的物质的量不少于________mol,加入烧瓶中的KClO3的质量应不少于________g(精确到0.1 g).
科目:gzhx 来源: 题型:解答题
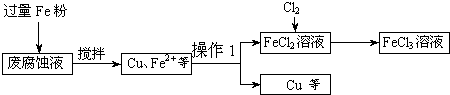
科目:gzhx 来源: 题型:
印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费。可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。测得某废腐蚀液中含CuCl2 1.5mol/L,含FeCl2 3.0mol/L,含FeCl3 1.0mol/L,含HCl 3.0mol/L。取废腐蚀液200mL按如下流程在实验室进行实验:
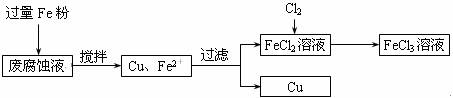
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂所需试剂是 (填化学式)。
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物。反应的化学方程式为 。
(3)下图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置。
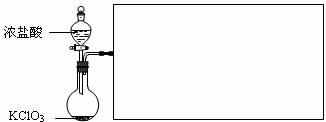
从下图挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管。固定装置不用画),并标明容器中所装试剂。
(4)实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收。控制生成氯气速度的操作是: 。
(5)按上述流程操作,需称取Fe粉的质量应不少于 g(精确到0.1g),需通入Cl2的物质的量不少于 mol,加入烧瓶中的KClO3的质量应不少于 g(精确到0.1g)。
科目:gzhx 来源: 题型:解答题
科目:gzhx 来源: 题型:
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是 。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3 。
①若酸性FeCl2 废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式:
| |
 ClO3-+
ClO3-+ | |
 Fe2++
Fe2++ | |
 =
= | |
 Cl-+
Cl-+ | |
 Fe3++
Fe3++ | |
 .
. (3)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
 欲使平衡正向移动可采用的方法是(填序号) 。
欲使平衡正向移动可采用的方法是(填序号) 。
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
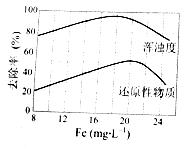
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约
为 mg·L-1。
科目:gzhx 来源: 题型:
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是 。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3 。
①若酸性FeCl2 废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式:
| |
 ClO3-+
ClO3-+
|
 Fe2++
Fe2++ | |
 =
= | |
 Cl-+
Cl-+ | |
 Fe3++
Fe3++ | |
 .
. (3)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
 欲使平衡正向移动可采用的方法是(填序号) 。
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。
科目:gzhx 来源: 题型:
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeC l3 高效,且腐蚀性小。请回答下列问题:
l3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是 。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3 。
①若酸性FeCl2 废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式:
| |
 ClO3-+
ClO3-+
|
 Fe2++
Fe2++ | |
 =
= | |
 Cl-+
Cl-+ | |
 Fe3++
Fe3++ | |

 .
. (3)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
 xFe3++yH2O
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释
c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。
科目:gzhx 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:填空题
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。(已知25℃Ksp[Fe(OH)3]=4.0×10﹣38 lg2=0.3)
请回答下列问题:
(1)FeCl3 净水的原理是____________ 。(用离子方程式表示),Fe3+水解生成的Fe(OH)3胶体粒子能吸附水中的悬浮杂质,常温下此反应的平衡常数为_________________(填写数值)。
(2)将FeCl3 溶液与NaHCO3 溶液混合,其离子方程式为 _______________。
(3)25℃时pH=3的溶液中,c(Fe3+)= mol•L﹣1要使Fe3+ 沉淀完全,pH应大于________。
(4)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+ 欲使平衡正向移动可采用的方法是(填序号) 。
Fex(OH)y(3x-y)++yH+ 欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
(5) FeCl3溶液可腐蚀印刷电路板,其反应为Cu +2FeCl3=CuCl2+2FeCl2 要将此反应设计在原电池中进行,则正极反应式为__________。
科目:gzhx 来源:2016届山西省高三第二轮训练三化学试卷(解析版) 题型:填空题
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)FeCl3净水的原理是 。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1,c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式: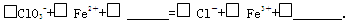
(3)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释
c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。

科目:gzhx 来源:2015-2016学年福建省高二下期末化学试卷(解析版) 题型:填空题
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)FeCl3净水的原理是__________________________,FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)_________________________;
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3.
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol•L-1,c(Fe3+)=1.0×10-3mol•L-1,c(Cl-)=5.3×10-2mol•L-1,则该溶液的pH约为_______;
②完成NaClO3氧化FeCl2的离子方程式:
____ClO3-+____Fe2++____= _____Cl-+____Fe3++______;
(3)FeCl3在溶液中分三步水【解析】
Fe3++H2O Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)2++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是_____________________________;
通过控制条件,以上水解产物聚合,生成聚合氯化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是(填序号)__________;
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是____________________;
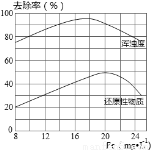
(4)天津某污水处理厂用聚合氯化铁净化污水的结果如图所示,由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg•L-1)表示]的最佳范围约为__________mg•L-1。
科目:gzhx 来源:2015-2016学年福建省厦门市高二下学期期末化学试卷(解析版) 题型:填空题
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小,请回答下列问题:
(1)FeCl3净水的原理是_________________;
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol•L-1,c(Fe3+)=1.0×10-3mol•L-1,c(Cl-)=5.3×10-2mol•L-1,则该溶液的pH约为_________________;
(3)FeCl3在溶液中分三步水【解析】
Fe3++H2O Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)2++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是_________________;
(4)通过控制条件,以上水解产物聚合,生成聚合氯化铁,离子方程式为:xFe3++yH2O⇌Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是(填序号)_________________
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
(5)室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条是_________________。
科目:gzhx 来源:2017届广西省高三上学期10月月考化学试卷(解析版) 题型:填空题
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)检验FeCl3溶液中阳离子的方法是
(2)FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)
FeCl3溶液也常用于腐蚀印刷电路板,反应的离子方程式为
(3)通过控制条件,将FeCl3水解产物聚合,生成聚合氧化铁,离子方程式为:xFe3++yH2O  Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是 (填序号)。
Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是 (填序号)。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
(4)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3。完成NaClO3 氧化FeCl2 的离子方程式 。
(5)处理废水时,发现FeCl3并不能使酸性废水中的悬浮物沉降除去,其原因是______________。
科目:gzhx 来源:2016届湖南省高三上学期入学考试化学试卷(解析版) 题型:填空题
(16分)FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:(16分)
(1)FeCl3 净水的原理是 。FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3 。
①若酸性FeCl2 废液中各离子浓度如下:则该溶液的pH约为 。
c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,
②NaClO3 能在酸性条件下氧化FeCl2 ,写出离子方程式:
(3)FeCl3 在溶液中分三步水【解析】
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为: xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
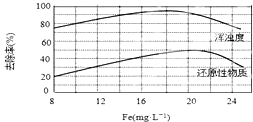
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。

由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。
科目:gzhx 来源: 题型:填空题
科目:gzhx 来源: 题型:解答题
科目:gzhx 来源: 题型:解答题
科目:gzhx 来源: 题型:解答题
科目:gzhx 来源: 题型:解答题