
科目:gzhx 来源:2013届安徽怀远县包集中学高二下学期期中考试化学试卷(解析版) 题型:填空题
(6分)一定温度下,向一固定容积的密闭容器中充入氢气和溴蒸气发生反应:H2(g)+Br2(g) 2HBr(g)。达到平衡状态后,下列说法中一定正确的是 ;能说明此反应达到平衡状态的是 。
2HBr(g)。达到平衡状态后,下列说法中一定正确的是 ;能说明此反应达到平衡状态的是 。
A.单位时间内生成n mol H2的同时生成2n mol HBr
B.单位时间内生成n mol H2的同时生成n molBr2
C.一个H-H键断裂的同时有两个H-Br键断裂
D.[HBr]∶[H2]∶[Br2]=2∶2∶1
E.温度和体积一定时,某一生成物的浓度不再变化
F.温度和体积一定时,容器内压强不再变化
科目:gzhx 来源: 题型:
(6分)一定温度下,向一固定容积的密闭容器中充入氢气和溴蒸气发生反应:H2(g)+Br2(g)2HBr(g)。达到平衡状态后,下列说法中一定正确的是 ;能说明此反应达到平衡状态的是 。
A.单位时间内生成n mol H2的同时生成2nmol HBr
B.单位时间内生成n mol H2的同时生成n molBr2
C.一个H-H键断裂的同时有两个H-Br键断裂
D.[HBr]∶[H2]∶[Br2]=2∶2∶1
E.温度和体积一定时,某一生成物的浓度不再变化
F.温度和体积一定时,容器内压强不再变化
科目:gzhx 来源:2011-2012学年安徽怀远县包集中学高二下学期期中考试化学试卷(带解析) 题型:填空题
(6分)一定温度下,向一固定容积的密闭容器中充入氢气和溴蒸气发生反应:H2(g)+Br2(g) 2HBr(g)。达到平衡状态后,下列说法中一定正确的是 ;能说明此反应达到平衡状态的是 。
2HBr(g)。达到平衡状态后,下列说法中一定正确的是 ;能说明此反应达到平衡状态的是 。
| A.单位时间内生成n mol H2的同时生成2n mol HBr |
| B.单位时间内生成n mol H2的同时生成n molBr2 |
| C.一个H-H键断裂的同时有两个H-Br键断裂 |
| D.[HBr]∶[H2]∶[Br2]=2∶2∶1 |
科目:gzhx 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高二化学(上) 题型:021
在一定温度下,向一固定体积的密闭容器中充入1mol N2和3mol H2,发生反应:N2(g)+3H2(g)![]() 2NH3(g),达到平衡后,又充入1mol N2和3mol H2,下列判断正确的是
2NH3(g),达到平衡后,又充入1mol N2和3mol H2,下列判断正确的是
[ ]
A.刚充入时,体系压强增大,后逐渐减小
B.达到新平衡时,N2和H2的转化率均降低
C.达到新平衡时,NH3的体积分数增大
D.达到新平衡时,c(N2)∶c(H2)∶c(NH3)=1∶3∶2
科目:gzhx 来源: 题型:
科目:gzhx 来源:期末题 题型:填空题
 2SO3。平衡后,SO2的转化率为а1,SO2浓度为c1moL/L,SO2体积分数为a1%;若此时再加入2moLSO2与1moLO2,达到新平衡后,SO2的转化率为а2,SO2浓度为c2moL/L,SO2体积分数为
2SO3。平衡后,SO2的转化率为а1,SO2浓度为c1moL/L,SO2体积分数为a1%;若此时再加入2moLSO2与1moLO2,达到新平衡后,SO2的转化率为а2,SO2浓度为c2moL/L,SO2体积分数为科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
科目:gzhx 来源:2010年河南省高一下学期期中考试化学试题 题型:选择题
273K时,反应N2(g)+3H2(g)
 2NH3(g) 生成2 molNH3(g)时放出92.2kJ的热量。在该温度下,向一固定容积的密闭容器内通入1mol N2和3mol H2,达到平衡时,放出热量为Q1;向另一容积相同的密闭容器中通入0.5mol N2和1.5mol H2,达到平衡时放出热量为Q2。则下列判断不正确的是:
2NH3(g) 生成2 molNH3(g)时放出92.2kJ的热量。在该温度下,向一固定容积的密闭容器内通入1mol N2和3mol H2,达到平衡时,放出热量为Q1;向另一容积相同的密闭容器中通入0.5mol N2和1.5mol H2,达到平衡时放出热量为Q2。则下列判断不正确的是:
A.同时进行时,用N2表示的反应速率:情况1>情况2
B.平衡时,情况1:Q1= 92.2kJ
C.达到平衡时,混合气体的密度:情况1>情况2
D.平衡时,情况2:Q2<46.1kJ
科目:gzhx 来源:2009-2010学年河南省郑州一中高一(下)期中化学试卷(解析版) 题型:选择题
科目:gzhx 来源:模拟题 题型:填空题
 H2(g) +CO(g)。 在一定温度下,向体积为2L的密闭容器中加入1 mol C和1 mol H2O,发生上述反应。
H2(g) +CO(g)。 在一定温度下,向体积为2L的密闭容器中加入1 mol C和1 mol H2O,发生上述反应。  2NH3(g) △H= -92.2 kJ.mol-1。反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示,其中t2、t7时刻改变的实验条件分别是:t2_____;t7____
2NH3(g) △H= -92.2 kJ.mol-1。反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示,其中t2、t7时刻改变的实验条件分别是:t2_____;t7____ 
科目:gzhx 来源:不详 题型:单选题
| A.同时进行时,用N2表示的反应速率:情况1>情况2 |
| B.平衡时,情况1:Q1=92.2kJ |
| C.达到平衡时,混合气体的密度:情况1>情况2 |
| D.平衡时,情况2:Q2<46.1kJ |
科目:gzhx 来源: 题型:
273K时,反应N2(g)+3H2(g) ![]() 2NH3(g) 生成2 molNH3(g)时放出92.2kJ的热量。在该温度下,向一固定容积的密闭容器内通入1mol N2和3mol H2,达到平衡时,放出热量为Q1;向另一容积相同的密闭容器中通入0.5mol N2和1.5mol H2,达到平衡时放出热量为Q2。则下列判断不正确的是:
2NH3(g) 生成2 molNH3(g)时放出92.2kJ的热量。在该温度下,向一固定容积的密闭容器内通入1mol N2和3mol H2,达到平衡时,放出热量为Q1;向另一容积相同的密闭容器中通入0.5mol N2和1.5mol H2,达到平衡时放出热量为Q2。则下列判断不正确的是:
A.同时进行时,用N2表示的反应速率:情况1>情况2
B.平衡时,情况1:Q1= 92.2kJ
C.达到平衡时,混合气体的密度:情况1>情况2
D.平衡时,情况2:Q2<46.1kJ
科目:gzhx 来源: 题型:
273K时,反应N2(g)+3H2(g)2NH3(g) 生成2 molNH3(g)时放出92.2kJ的热量。在该温度下,向一固定容积的密闭容器内通入1mol N2和3mol H2,达到平衡时,放出热量为Q1;向另一容积相同的密闭容器中通入0.5mol N2和1.5mol H2,达到平衡时放出热量为Q2。则下列判断不正确的是:
A.同时进行时,用N2表示的反应速率:情况1>情况2
B.平衡时,情况1:Q1= 92.2kJ
C.达到平衡时,混合气体的密度:情况1>情况2
D.平衡时,情况2:Q2<46.1kJ
科目:gzhx 来源:2010年河南省实验中学高一下学期期中考试化学试题 题型:单选题
273K时,反应N2(g)+3H2(g)  2NH3(g) 生成2 molNH3(g)时放出92.2kJ的热量。在该温度下,向一固定容积的密闭容器内通入1mol N2和3mol H2,达到平衡时,放出热量为Q1;向另一容积相同的密闭容器中通入0.5mol N2和1.5mol H2,达到平衡时放出热量为Q2。则下列判断不正确的是:
2NH3(g) 生成2 molNH3(g)时放出92.2kJ的热量。在该温度下,向一固定容积的密闭容器内通入1mol N2和3mol H2,达到平衡时,放出热量为Q1;向另一容积相同的密闭容器中通入0.5mol N2和1.5mol H2,达到平衡时放出热量为Q2。则下列判断不正确的是:
| A.同时进行时,用N2表示的反应速率:情况1>情况2 |
| B.平衡时,情况1:Q1= 92.2kJ |
| C.达到平衡时,混合气体的密度:情况1>情况2 |
| D.平衡时,情况2:Q2<46.1kJ |
科目:gzhx 来源: 题型:
| A、此时Y的浓度为0.6mol/L | B、5min 内v(X)=0.06mol/(L•min) | C、容器内X、Y、Z的浓度之比为1:2:2,则该反应达到平衡状态 | D、单位时间消耗0.1 molX同时生成0.2molZ,则该反应达到平衡状态 |
科目:gzhx 来源: 题型:
某温度下,向2L固定容积的密闭容器中加入2mol的SO2(g) 和1mol的O2(g)发生反应:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH﹤0,达平衡时,平衡常数K1=16。同温下,若向该密闭容器中加入1mol的SO3(g) 发生反应:SO3(g)
2SO3(g) ΔH﹤0,达平衡时,平衡常数K1=16。同温下,若向该密闭容器中加入1mol的SO3(g) 发生反应:SO3(g) ![]() SO2(g) + 1/2O2(g),达到平衡时,其平衡常数K2=________,再升高温度K2值将 (填“增大”“不变”或“减小”)。
SO2(g) + 1/2O2(g),达到平衡时,其平衡常数K2=________,再升高温度K2值将 (填“增大”“不变”或“减小”)。
科目:gzhx 来源: 题型:阅读理解
| 1 |
| 2 |
| 10 |
| 3 |
| 10 |
| 3 |
 |
0.1 | 0.5 | 1.0 | 10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
科目:gzhx 来源: 题型:阅读理解
(12分)(1)有科学家提出“绿色自由”的构想:将CO2变为燃料或有机化学品。其构想分成3个步骤:
① 利用浓碳酸钾溶液吸收空气中的CO2;
② 将第①步吸收液电解产生H2和O2,同时分离出CO2;
③ 将第②步产生的H2和CO2在一定条件下转化成CH4和水蒸气。
已知:H2(g)+0.5O2(g)=H2O(l) △H1= —285.8 kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H2=—889.6 kJ/mol
H2O(l)=H2O(g) △H3=+44.0 kJ/mol
第③步反应的热化学方程式为 。
(2)使用合适的催化剂和电极材料,以N2、H2为原料,以HCl-NH4Cl为电解质溶液构成新型燃料电池,同时达到固氮作用。该电池的正极反应式为 ,溶液中H+向 极移动(选择填写“正”或“负”)。
(3)某催化剂的主要成分是FeO、Fe2O3,当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化活性最高。以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉,发生如下反应:
2Fe2O3+C4FeO+CO2。为制得这种活性最高的催化剂,应向480 g Fe2O3粉末中加入炭粉的质量为_____g。
(4)在T℃时,向2L固定体积的密闭容器中加入4mol A和2 mol B,发生如下反应:
2A(g) + B(g) C(g) + D(g) △H = Q kJ·mol-1
当反应达到平衡时,A的转化率为50﹪。
(ⅰ)在一定条件下,反应可以自发向右进行,可知Q __________0 (填“﹤”、“﹥”或“﹦”)。
(ⅱ)维持温度不变,若向该容器中加入的物质及量如下,使起始时v(正)>v(逆)且达到平衡时C的百分含量为20﹪。下列符合要求的是
A.2 mol A、1 molB B.1 mol He、3 mol A、1.5 mol B、0.5molC、0.5mol D
C.2 mol C、2 molD D.2 molA、1mol B、1 mol C、1 mol D
科目:gzhx 来源: 题型:阅读理解
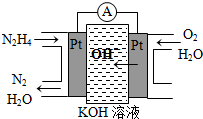 Ⅰ.肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂.试回答下列问题
Ⅰ.肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂.试回答下列问题| 物质 | CO | H2 | CH3OH |
| 浓度(mol•L-1) | 0.9 | 1.0 | 0.6 |
| 2 |
| 3 |
| 2 |
| 3 |