
科目:czhx 来源: 题型:
| 实验过程 | 实验现象 | 结论 |
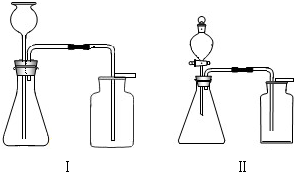
取少量黑色样品于试管,加入足量的稀硫酸,充分振荡 取少量黑色样品于试管,加入足量的稀硫酸,充分振荡 |
黑色固体不溶解 黑色固体不溶解 |
残余固体是碳 |
科目:czhx 来源: 题型:
科目:czhx 来源: 题型:
科目:czhx 来源: 题型:阅读理解
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | X |
| 3 | 7.30% | 8.00% | 1 4 |
科目:czhx 来源: 题型:阅读理解
科目:czhx 来源: 题型:阅读理解
科目:czhx 来源: 题型:
 13、在化学晚会上,小林同学表演了一个化学小魔术“空瓶生烟”(如图所示),A瓶中充满氯化氢气体B瓶中充满氨气抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题:
13、在化学晚会上,小林同学表演了一个化学小魔术“空瓶生烟”(如图所示),A瓶中充满氯化氢气体B瓶中充满氨气抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题: ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“○”表示氯原子,
”表示氮原子,用“○”表示氯原子,
科目:czhx 来源: 题型:
 ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用下图表示为:
”表示氯原子,上述反应过程可用下图表示为: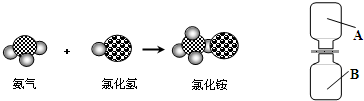
科目:czhx 来源: 题型:阅读理解
| 金属材料 | 无机非金属材料 | 合成材料 |
|
铁锅(铁勺、菜刀)
|
瓷碗(瓷盆等)
|
塑料篮
|
科目:czhx 来源: 题型:
 在化学晚会上,小林同学表演了一个化学小魔术“空瓶生烟”(如图所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题:
在化学晚会上,小林同学表演了一个化学小魔术“空瓶生烟”(如图所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题: ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用如图:
”表示氯原子,上述反应过程可用如图: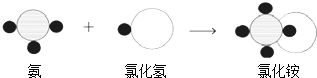
科目:czhx 来源: 题型:阅读理解
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
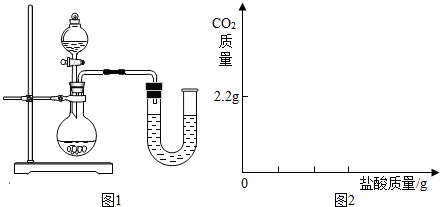
科目:czhx 来源: 题型:阅读理解
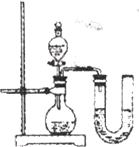
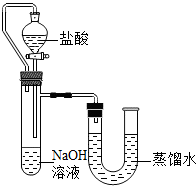 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应.科目:czhx 来源: 题型:阅读理解
科目:czhx 来源: 题型:阅读理解
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |

科目:czhx 来源: 题型:阅读理解
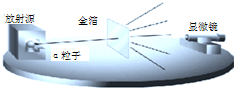 (2011•玉溪)探究原子结构的奥秘.
(2011•玉溪)探究原子结构的奥秘.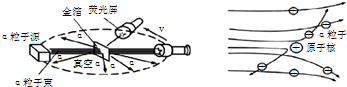

科目:czhx 来源: 题型:

科目:czhx 来源: 题型:
科目:czhx 来源: 题型:阅读理解
 23、物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
23、物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
科目:czhx 来源: 题型:阅读理解
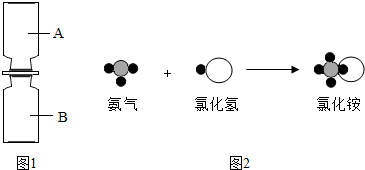 (2012•连云港一模)在化学晚会上,小军同学表演了一个化学小魔术“空瓶生烟”(如图1所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题:若用“
(2012•连云港一模)在化学晚会上,小军同学表演了一个化学小魔术“空瓶生烟”(如图1所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题:若用“ ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用图2表示.
”表示氯原子,上述反应过程可用图2表示.
| ||
科目:czhx 来源: 题型:阅读理解