
科目:gzhx 来源: 题型:阅读理解
科目:gzhx 来源:2010-2011学年广东省高三下学期二轮复习综合测试(4)理综化学部分 题型:填空题
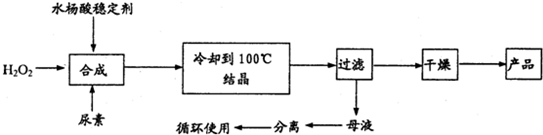
过氧化尿素[CO(NH2)2·H2O2 ]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域。其合成如下:

试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25—30℃,其主要原因是___________________________________。
(2)从母液中分离出H2O2和尿素,采用的操作是___________。
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000 mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应)。
①KMnO4溶液应盛放在________式(选填:“酸”、“碱”)滴定管中。
②完成并配平方程式:__MnO4-+ ___H2O2+___H+=___Mn2++ ____H2O+___ _____
③根据滴定结果,可确定产品中活性氧的质量分数为:___________。
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”)。
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为_________。
科目:gzhx 来源: 题型:
过氧化尿素[CO(NH2)2·H2O2 ]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域。其合成如下:
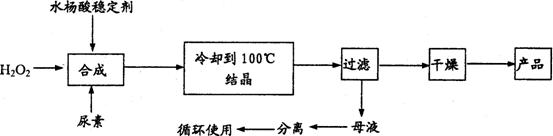
试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25—30℃,其主要原因是___________________________________。
(2)从母液中分离出H2O2和尿素,采用的操作是___________。
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000 mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应)。
①KMnO4溶液应盛放在________式(选填:“酸”、“碱”)滴定管中。
②完成并配平方程式:__MnO4-+ ___H2O2+___H+=___Mn2++ ____H2O+___ _____
③根据滴定结果,可确定产品中活性氧的质量分数为:___________。
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”)。
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为_________。
科目:gzhx 来源: 题型:
过氧化尿素[CO(NH2)2·H2O2 ]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域。其合成如下:
试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25—30℃,其主要原因是___________________________________。
(2)从母液中分离出H2O2和尿素,采用的操作是___________。
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000 mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应)。
①KMnO4溶液应盛放在________式(选填:“酸”、“碱”)滴定管中。
②完成并配平方程式:__MnO4-+___H2O2+___H+=___Mn2++ ____H2O+___ _____
③根据滴定结果,可确定产品中活性氧的质量分数为:___________。
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”)。
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为_________。
科目:gzhx 来源:2011届广东省电白一中高三下学期二轮复习综合测试(4)理综化学部分 题型:填空题
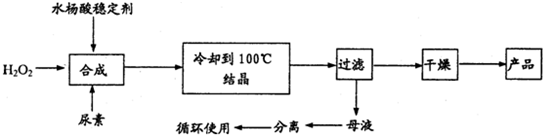
过氧化尿素[CO(NH2)2·H2O2 ]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域。其合成如下:
试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25—30℃,其主要原因是___________________________________。
(2)从母液中分离出H2O2和尿素,采用的操作是___________。
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000 mol/L KMnO4标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应)。
①KMnO4溶液应盛放在________式(选填:“酸”、“碱”)滴定管中。
②完成并配平方程式:__MnO4-+ ___H2O2+___H+=___Mn2++ ____H2O+___ _____
③根据滴定结果,可确定产品中活性氧的质量分数为:___________。
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”)。
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为_________。
科目:gzhx 来源:2010-2011学年浙江省绍兴市高三教学质量调测(理综)化学部分 题型:填空题
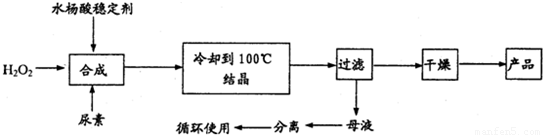
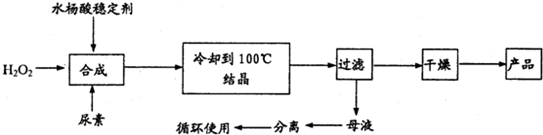
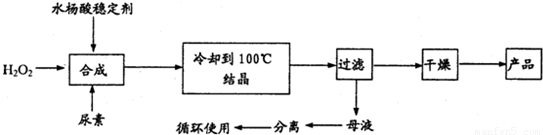
过氧化尿素是一种无毒无味的白色粉末,是一种新型的漂白剂与消毒剂。它的合成方式如下:

请回答下列问题:
(1)根据反应原理,CO(NH2)2·H2O2分子内存在的作用力
是 。
A.共价键 B.离子键
C.金属键 D.氢键
(2)流程图中反应器的装置如图所示,推测该反应的加热方式是 ;回流管中冷水流从 口流入;搅拌器选用的材质是玻璃而不是铁质或铝质材料的原因是 。

(3)母液处理方案1可以是 (用文字表达)。若欲从母液中离出H2O2和尿素,可采用的操作是 (选填序号)
A.盐析、过滤 B.减压蒸馏、结晶
C.分液、过滤 D.常压蒸馏、萃取
(4)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品2.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol·L-1的硫酸,然后用0.1000mol·L-1 KMnO4标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液8.00mL(KMnO4溶液与尿素不反应)。
①完成并配平方程式: MnO4-+ H2O2+ H+= MnO2++ H2O+
②若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量 。(“偏高”、“偏低”或“不变”)。
③根据滴定结果,可确定产品中活性氧的质量分数为 。
科目:gzhx 来源:浙江省模拟题 题型:填空题
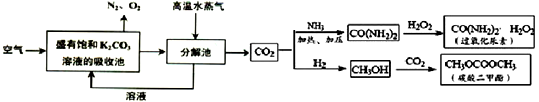
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)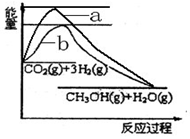
科目:gzhx 来源:不详 题型:问答题
科目:gzhx 来源:2011年广东省茂名市电白一中高考化学二轮复习卷(四)(解析版) 题型:解答题
科目:gzhx 来源:模拟题 题型:填空题
过氧化物在日常生活与工农业生产中应用广泛。如:过氧化氢是一种常见的绿色氧化剂,过氧碳酸钠、过氧化尿素则是多功能、高效、广谱的固体消毒剂。
资料显示:过氧化氢是一种无色液体,属于二元弱酸,能与水、乙醇、乙醚以任意比混溶,易分解,且重金属离子 对其分解过程具有促进催化作用。
(1)写出过氧化氢在Fe3+存在条件下分解的化学反应方程式:____________________;过氧化氢可作为绿
色氧化剂的理由是_______________。
(2)某同学为验证H2O2具有弱酸性,在滴加有酚酞的NaOH稀溶液中,加入适量的H2O2,结果发现溶液的红色褪去。你认为能否通过该实验证明H2O2具有酸性,并说明理由________________。如何通过实验进一步证明褪色的真正原因?请写出具体的实验方法:________________。
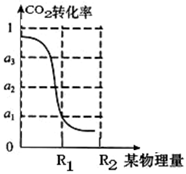
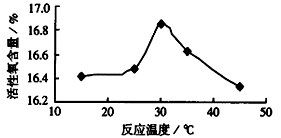
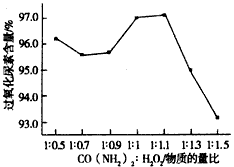
(3)过氧化尿素是一种新型的氧化剂与消毒剂,由H2O2与尿素在30℃反应制得。如图是30℃时过氧化尿素合成过程中原料的物质的量配比对产品含量的影响;你认为实际生产中应将n(H2O2):n[CO(NH2)2]控制在
____________,出现这一实验结果的主要原因是___________________。
科目:gzhx 来源: 题型:解答题
科目:gzhx 来源:2009-2010学年江苏省盐城市高三(上)期中化学试卷(解析版) 题型:解答题
科目:gzhx 来源: 题型:单选题
科目:gzhx 来源: 题型:
过氧化尿素是一种无毒无味的白色粉末,是一种新型的漂白剂与消毒剂。它的合成方式如下:
请回答下列问题:
(1)根据反应原理,CO(NH2)2·H2O2分子内存在的作用力
是 。
A.共价键 B.离子键
C.金属键 D.氢键
(2)流程图中反应器的装置如图所示,推测该反应的加热方式是 ;回流管中冷水流从 口流入;搅拌器选用的材质是玻璃而不是铁质或铝质材料的原因是 。
(3)母液处理方案1可以是 (用文字表达)。若欲从母液中离出H2O2和尿素,可采用的操作是 (选填序号)
A.盐析、过滤 B.减压蒸馏、结晶
C.分液、过滤 D.常压蒸馏、萃取
(4)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品2.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol·L-1的硫酸,然后用0.1000mol·L-1 KMnO4标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液8.00mL(KMnO4溶液与尿素不反应)。
①完成并配平方程式: MnO4-+ H2O2+ H+= MnO2++ H2O+
②若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量 。(“偏高”、“偏低”或“不变”)。
③根据滴定结果,可确定产品中活性氧的质量分数为 。
科目:gzhx 来源: 题型:
 (实验化学)某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积.如图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水.甲管有刻度(0~50mL),供量气用;乙管可上下移动,以调节液面高低.
(实验化学)某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积.如图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水.甲管有刻度(0~50mL),供量气用;乙管可上下移动,以调节液面高低.科目:gzhx 来源: 题型:阅读理解
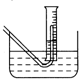 Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:①称取过氧化钠固体2.00g;②把这些过氧化钠固体放入气密性良好的气体发生装置中;③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平;④将烧瓶中的液体转移到250mL的容量瓶中,洗涤并将洗涤液也转入容量瓶,然后加入蒸馏水,定容,使液面恰好与刻度相切;⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLKMnO4溶液(此时锰全部以Mn2+存在)
Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:①称取过氧化钠固体2.00g;②把这些过氧化钠固体放入气密性良好的气体发生装置中;③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平;④将烧瓶中的液体转移到250mL的容量瓶中,洗涤并将洗涤液也转入容量瓶,然后加入蒸馏水,定容,使液面恰好与刻度相切;⑤用移液管移取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4溶液去滴定,至终点时用去了24.20mLKMnO4溶液(此时锰全部以Mn2+存在)科目:gzhx 来源: 题型:

| ||
| ||
科目:gzhx 来源: 题型:
| ||
| ||