
题目列表(包括答案和解析)
探究影响化学反应速率的因素。
(1)发现和提出问题:
化学反应有的很快,如爆炸,有的相当慢,如铁生锈。决定物质之间能否反应以及化学反应速率快慢的内因是反应物的结构和性质。除此以外,催化剂也能改变化学反应速率。
同学们都有这样的生活经验,木炭在氧气中燃烧比在空气中燃烧的旺;这说明反应物的浓度对化学反应速率有影响。夏天,将食品放在冰箱里不容易腐烂;这说明温度对化学反应速率也有影响。那么,温度和浓度是如何影响化学反应速率?
(2)猜想与假设:![]() .浓度越大,化学反应的速率越快。
.浓度越大,化学反应的速率越快。
![]() .温度越高,化学反应的速率越快。
.温度越高,化学反应的速率越快。
(3)收集证据:
实验仪器和试剂:试管、试管夹、酒精灯、药匙、量筒;锌粒、5%盐酸、20%盐酸。
利用上述实验仪器和试剂进行探究,如果假设是![]() ,你认为需要控制的变量有 。
,你认为需要控制的变量有 。
如果假设是![]() ,你认为需要控制的变量有 。
,你认为需要控制的变量有 。
在实验中,通过观测 来判断反应的快慢。
(4)结论与解释:实验证明,条件相同,盐酸的溶质质量分数越大,与金属的反应速率越快。其它条件相同,温度越高,化学反应的速率越快。从反应物的微观粒子相互作用的角度,你认为其原因分别是________________________________
和__________________
(5)交流与反思:通过实验探究我们知道,我们可以通过控制反应条件来控制化学反应的快慢。请你再举出一个通过控制化学反应条件来控制化学反应快慢的事例。
__________________
课外小组研究“影响H2O2生成O2反应速率的因素”的课题。通过查阅资料,他们提出如下猜想。
【提出猜想】催化剂和反应物浓度都会影响H2O2生成O2 的反应速率
【实验过程】实验装置如图: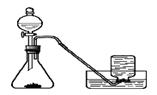
实验操作:检查装置的气密性良好。将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体。
实验记录:
| 实验编号 | ① | ② | ③ |
| 反应物 | 5%H2O2 50 mL | 5%H2O2 | 3%H2O250 mL |
| 加入固体 | 0.5gCuO | 0.5gMnO2 | 0.5gMnO2 |
| 收集等体积O2所需时间 | 105 s | 45s | 78 s |
课外小组研究“影响H2O2生成O2反应速率的因素”的课题。通过查阅资料,他们提出如下猜想。
【提出猜想】催化剂和反应物浓度都会影响H2O2生成O2 的反应速率
【实验过程】实验装置如图:
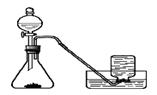
实验操作:检查装置的气密性良好。将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体。
实验记录:
|
实验编号 |
① |
② |
③ |
|
反应物 |
5%H2O2 50 mL |
5%H2O2 |
3%H2O250 mL |
|
加入固体 |
0.5gCuO |
0.5gMnO2 |
0.5gMnO2 |
|
收集等体积O2所需时间 |
105 s |
45s |
78 s |
(1)实验②中加入H2O2溶液的体积为 mL;
(2)充分反应后,将实验②中剩余物质里的MnO2提取的方法是 ;
【结论】该探究过程得出的结论是 ;
【反思】 H2O2在常温加入MnO2 后反应速率加快。小敏提出,为了更好的证明二氧化锰是否对H2O2生成O2的反应速率有影响,还应该增加一组对比实验。该实验选用的药品和用量为 ;
【实验拓展】小敏用收集的气体进行氧气的性质实验。
(1)铁丝在氧气中燃烧,其反应的化学方程式为 ;
(2)小敏发现用收集的气体进行铁丝燃烧实验时,没有产生明显的火星四射现象。造成这种结果的可能原因是 。

| 实验编号 | ① | ② | ③ |
| 反应物 | 5%H2O2 50 mL | 5%H2O2 | 3%H2O250 mL |
| 加入固体 | 0.5gCuO | 0.5gMnO2 | 0.5gMnO2 |
| 收集等体积O2所需时间 | 105 s | 45s | 78 s |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com