
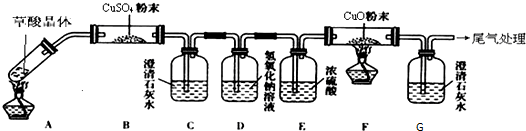
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
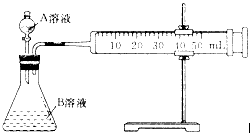

 H2C2O4»ή“ΚΘ§Νμ»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ
H2C2O4»ή“ΚΘ§Νμ»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ KMnO4»ή“ΚΓΘΫΪΥΡ÷ß ‘ΙήΖ÷≥…ΝΫΉι(Ης”–“Μ÷ß Δ”–H2C2O4»ή“ΚΚΆKMnO4»ή“ΚΒΡ ‘Ιή)Θ§“ΜΉιΖ≈»κάδΥ°÷–Θ§Νμ“ΜΉιΖ≈»κ»»Υ°÷–Θ§Ψ≠Ιΐ“ΜΕΈ ±ΦδΚσΘ§Ζ÷±πΜλΚœ≤Δ’ώΒ¥Θ§Φ«¬Φ»ή“ΚΆ …ΪΥυ–η ±ΦδΓΘΗΟ Β―ι ‘ΆΦΧΫΨΩ__________Ε‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΘ§ΒΪΗΟΉιΆ§―ß Φ÷’ΟΜ”–Ω¥ΒΫ»ή“ΚΆ …ΪΘ§Τδ‘≠“ρ «_____________________________________ΓΘ
KMnO4»ή“ΚΓΘΫΪΥΡ÷ß ‘ΙήΖ÷≥…ΝΫΉι(Ης”–“Μ÷ß Δ”–H2C2O4»ή“ΚΚΆKMnO4»ή“ΚΒΡ ‘Ιή)Θ§“ΜΉιΖ≈»κάδΥ°÷–Θ§Νμ“ΜΉιΖ≈»κ»»Υ°÷–Θ§Ψ≠Ιΐ“ΜΕΈ ±ΦδΚσΘ§Ζ÷±πΜλΚœ≤Δ’ώΒ¥Θ§Φ«¬Φ»ή“ΚΆ …ΪΥυ–η ±ΦδΓΘΗΟ Β―ι ‘ΆΦΧΫΨΩ__________Ε‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΘ§ΒΪΗΟΉιΆ§―ß Φ÷’ΟΜ”–Ω¥ΒΫ»ή“ΚΆ …ΪΘ§Τδ‘≠“ρ «_____________________________________ΓΘ “―÷ΣKMnO4ΚΆH2C2O4‘ΎΥα–‘»ή“Κ÷–ΖΔ…ζΖ¥”ΠΘΚ
KMnO4+ H2C2O4+ H2SO4 ΓΣ K2SO4+ MnSO4+ CO2Γϋ+ H2OΘ®«κ≈δΤΫΘ©ΓΘ
ΦΉΓΔ““ΝΫΗω Β―ι–ΓΉι”ϊΧΫΨΩ”ΑœλΜ·―ßΖ¥”ΠΥΌ¬ ΒΡ“ρΥΊΘ§…ηΦΤ Β―ιΖΫΑΗ»γœ¬ΘΚ
(1)ΦΉΉιΘΚΆ®Ιΐ≤βΕ®ΒΞΈΜ ±ΦδΡΎ…ζ≥…CO2ΤχΧεΧεΜΐΒΡ¥σ–Γά¥±»ΫœΜ·―ßΖ¥”ΠΥΌ¬ ΒΡ¥σ–ΓΘ§ Β―ιΉΑ÷Ο»γΆΦΥυ ΨΓΘ
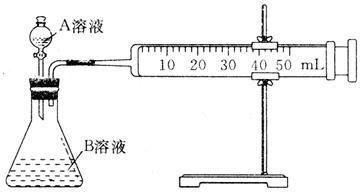
Β―ι ±A»ή“Κ“Μ¥Έ–‘Ζ≈œ¬Θ§AΘ§BΒΡ≥…Ζ÷Φϊœ¬±μΘΚ
| –ρΚ≈ | A»ή“Κ | B»ή“Κ |
| ΔΌ | 2mL 0.1 molΓΛLΘ≠1 H2C2O4»ή“Κ | 4mL 0.01 molΓΛLΘ≠1 KMnO4»ή“Κ |
| ΔΎ | 2mL 0.2 molΓΛLΘ≠1 H2C2O4»ή“Κ | 4mL 0.01 molΓΛLΘ≠1 KMnO4»ή“Κ |
| Δέ | 2mL 0.2 molΓΛLΘ≠1L H2C2O4»ή“Κ | 4mL 0.01 molΓΛLΘ≠1 KMnO4»ή“ΚΓΔ…ΌΝΩ¥ΏΜ·ΦΝ |
ΗΟ Β―ιΧΫΨΩΒΡ « Ε‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΓΘ‘ΎΖ¥”ΠΆΘ÷Ι÷°«ΑΘ§œύΆ§ ±ΦδΡΎ’κΆ≤÷–ΥυΒΟCO2ΒΡΧεΜΐ”…¥σΒΫ–ΓΒΡΥ≥–ρ « (”Ο Β―ι–ρΚ≈ΧνΩ’)ΓΘ
(2)““ΉιΘΚΆ®Ιΐ≤βΕ®KMnO4»ή“ΚΆ …ΪΥυ–η ±ΦδΒΡΕύ…Όά¥±»ΫœΜ·―ßΖ¥”ΠΥΌ¬ ΒΡ¥σ–ΓΓΘ»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ2![]() 0.1
0.1![]() H2C2O4»ή“ΚΘ§Νμ»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ4
H2C2O4»ή“ΚΘ§Νμ»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ4![]() 0.1
0.1![]() KMnO4»ή“ΚΓΘΫΪΥΡ÷ß ‘ΙήΖ÷≥…ΝΫΉι(Ης”–“Μ÷ß Δ”–H2C2O4»ή“ΚΚΆKMnO4»ή“ΚΒΡ ‘Ιή)Θ§“ΜΉιΖ≈»κάδΥ°÷–Θ§Νμ“ΜΉιΖ≈»κ»»Υ°÷–Θ§Ψ≠Ιΐ“ΜΕΈ ±ΦδΚσΘ§Ζ÷±πΜλΚœ≤Δ’ώΒ¥Θ§Φ«¬Φ»ή“ΚΆ …ΪΥυ–η ±ΦδΓΘΗΟ Β―ι ‘ΆΦΧΫΨΩ Ε‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”Αœλ,ΒΪΗΟΉιΆ§―ß Φ÷’ΟΜ”–Ω¥ΒΫ»ή“ΚΆ …ΪΘ§Τδ‘≠“ρ « ΓΘ
KMnO4»ή“ΚΓΘΫΪΥΡ÷ß ‘ΙήΖ÷≥…ΝΫΉι(Ης”–“Μ÷ß Δ”–H2C2O4»ή“ΚΚΆKMnO4»ή“ΚΒΡ ‘Ιή)Θ§“ΜΉιΖ≈»κάδΥ°÷–Θ§Νμ“ΜΉιΖ≈»κ»»Υ°÷–Θ§Ψ≠Ιΐ“ΜΕΈ ±ΦδΚσΘ§Ζ÷±πΜλΚœ≤Δ’ώΒ¥Θ§Φ«¬Φ»ή“ΚΆ …ΪΥυ–η ±ΦδΓΘΗΟ Β―ι ‘ΆΦΧΫΨΩ Ε‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”Αœλ,ΒΪΗΟΉιΆ§―ß Φ÷’ΟΜ”–Ω¥ΒΫ»ή“ΚΆ …ΪΘ§Τδ‘≠“ρ « ΓΘ
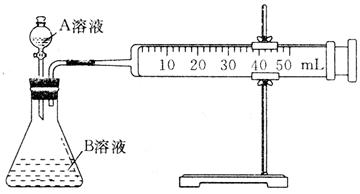
| –ρΚ≈ | A»ή“Κ | B»ή“Κ |
| ΔΌ | 2mL 0.1 molΓΛLΘ≠1 H2C2O4»ή“Κ | 4mL 0.01 molΓΛLΘ≠1 KMnO4»ή“Κ |
| ΔΎ | 2mL 0.2 molΓΛLΘ≠1 H2C2O4»ή“Κ | 4mL 0.01 molΓΛLΘ≠1 KMnO4»ή“Κ |
| Δέ | 2mL 0.2 molΓΛLΘ≠1L H2C2O4»ή“Κ | 4mL 0.01 molΓΛLΘ≠1 KMnO4»ή“ΚΓΔ…ΌΝΩ¥ΏΜ·ΦΝ |
 ¬ ΒΡ¥σ–ΓΓΘ»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ2
¬ ΒΡ¥σ–ΓΓΘ»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ2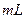 0.1
0.1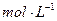 H2C2O4»ή“ΚΘ§Νμ»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ4
H2C2O4»ή“ΚΘ§Νμ»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ4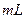 0.1
0.1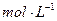 KMnO4»ή“ΚΓΘΫΪΥΡ÷ß ‘ΙήΖ÷≥…ΝΫΉι(Ης”–“Μ÷ß Δ”–H2C2O4»ή“ΚΚΆKMnO4»ή“ΚΒΡ ‘Ιή)Θ§“ΜΉιΖ≈»κάδΥ°÷–Θ§Νμ“ΜΉιΖ≈»κ»»Υ°÷–Θ§Ψ≠Ιΐ“ΜΕΈ ±ΦδΚσΘ§Ζ÷±πΜλΚœ≤Δ’ώΒ¥Θ§Φ«¬Φ»ή“ΚΆ …ΪΥυ–η ±ΦδΓΘΗΟ Β―ι ‘ΆΦΧΫΨΩ Ε‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”Αœλ,ΒΪΗΟΉιΆ§―ß Φ÷’ΟΜ”–Ω¥ΒΫ»ή“ΚΆ …ΪΘ§Τδ‘≠“ρ « ΓΘ
KMnO4»ή“ΚΓΘΫΪΥΡ÷ß ‘ΙήΖ÷≥…ΝΫΉι(Ης”–“Μ÷ß Δ”–H2C2O4»ή“ΚΚΆKMnO4»ή“ΚΒΡ ‘Ιή)Θ§“ΜΉιΖ≈»κάδΥ°÷–Θ§Νμ“ΜΉιΖ≈»κ»»Υ°÷–Θ§Ψ≠Ιΐ“ΜΕΈ ±ΦδΚσΘ§Ζ÷±πΜλΚœ≤Δ’ώΒ¥Θ§Φ«¬Φ»ή“ΚΆ …ΪΥυ–η ±ΦδΓΘΗΟ Β―ι ‘ΆΦΧΫΨΩ Ε‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”Αœλ,ΒΪΗΟΉιΆ§―ß Φ÷’ΟΜ”–Ω¥ΒΫ»ή“ΚΆ …ΪΘ§Τδ‘≠“ρ « ΓΘ(8Ζ÷)“―÷ΣKMnO4ΚΆH2C2O4(≤ίΥα)‘ΎΥα–‘»ή“Κ÷–ΜαΖΔ…ζ»γœ¬Ζ¥”ΠΘΚ
2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2Γϋ+8H2O
 ΦΉΓΔ““ΝΫΗω Β―ι–ΓΉι”ϊΧΫΨΩ”ΑœλΜ·―ßΖ¥”ΠΥΌ¬ ΒΡ“ρΥΊΘ§…ηΦΤ
ΦΉΓΔ““ΝΫΗω Β―ι–ΓΉι”ϊΧΫΨΩ”ΑœλΜ·―ßΖ¥”ΠΥΌ¬ ΒΡ“ρΥΊΘ§…ηΦΤ
Β―ιΖΫΑΗ»γœ¬( Β―ι÷–Υυ”ΟKMnO4»ή“ΚΨυ“―ΥαΜ·)ΘΚ
Θ®1Θ©ΦΉΉιΘΚΆ®Ιΐ≤βΕ®ΒΞΈΜ ±ΦδΡΎ…ζ≥…CO2ΤχΧεΧεΜΐΒΡΝΩά¥±»
ΫœΜ·―ßΖ¥”ΠΥΌ¬ Θ§ Β―ιΉΑ÷Ο»γΆΦΘ§ Β―ι ±Ζ÷“Κ¬©ΕΖ÷–A»ή
“Κ“Μ¥Έ–‘Φ”»κΘ§AΓΔBΒΡ≥…Ζ÷Φϊœ¬±μΘΚ
| –ρΚ≈ | A»ή“Κ | B»ή“Κ |
| ΔΌ | 2mL 0.1 molΓΛLΘ≠1H2C2O4»ή“Κ | 4mL 0.01 molΓΛLΘ≠1KMnO4»ή“Κ |
| ΔΎ | 2mL 0.2 molΓΛLΘ≠1 H2C2O4»ή“Κ | 4mL 0.01 molΓΛLΘ≠1 KMnO4»ή“Κ |
| Δέ | 2mL 0.2 molΓΛLΘ≠1 H2C2O4»ή“Κ | 4mL 0.01 molΓΛLΘ≠1 KMnO4»ή“Κ …ΌΝΩMnSO4(¥ΏΜ·ΦΝ) |
ΗΟ Β―ιΧΫΨΩΒΡ « “ρΥΊΕ‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΓΘ‘ΎΖ¥”ΠΆΘ÷Ι÷°«ΑΘ§œύΆ§ ±ΦδΡΎ’κΆ≤÷–ΥυΒΟCO2ΒΡΧεΜΐ”…¥σΒΫ–ΓΒΡΥ≥–ρ « (Χν Β―ι–ρΚ≈)ΓΘ
Θ®2Θ©““ΉιΘΚΆ®Ιΐ≤βΕ®KMnO4»ή“ΚΆ …ΪΥυ–η ±ΦδΒΡΕύ…Όά¥±»ΫœΜ·―ßΖ¥”ΠΥΌ¬ ΓΘ
»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ2 mL 0.1 molΓΛLΘ≠1H2C2O4»ή“ΚΘ§Νμ»ΓΝΫ÷ß ‘ΙήΗςΦ”»κ4 mL 0.1 molΓΛLΘ≠1 KMnO4»ή“ΚΓΘΫΪΥΡ÷ß ‘ΙήΖ÷≥…ΝΫΉι(ΟΩΉιΗς”–“Μ÷ß Δ”–H2C2O4»ή“ΚΚΆKMnO4»ή“Κ)Θ§“ΜΉιΖ≈»κάδΥ°÷–Θ§Νμ“ΜΉιΖ≈»κ»»Υ°÷–Θ§“ΜΕΈ ±ΦδΚσΘ§Ζ÷±πΜλΚœ≤Δ’ώΒ¥Θ§Φ«¬Φ»ή“ΚΆ …ΪΥυ–η ±ΦδΓΘΗΟ Β―ι ‘ΆΦΧΫΨΩ
“ρΥΊΕ‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΘ§ΒΪΗΟΉιΆ§―ß Φ÷’ΟΜ”–Ω¥ΒΫ»ή“ΚΆξ»ΪΆ …ΪΘ§Τδ‘≠“ρ « ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com