
题目列表(包括答案和解析)
普通食盐的主要成份是NaCl和杂质,假设杂质不溶于水、受热不分解、与AgNO3不反应。王华同学测定普通食盐样品中氯化钠的质量分数时所进行的实验操作流程和实验数据如下图所示。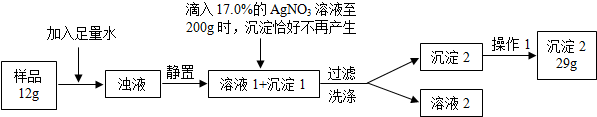
(实验中发生的化学反应方程式为:AgNO3+NaCl=AgCl↓+NaNO3)
请你完成空格和计算:
(1)王华进行操作1的目的是 _;
(2)求算样品中氯化钠的质量分数。(结果保留小数点后1位)
某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品,反应的化学方程式为:
2NaCl+2H2O 2NaOH+H2↑+Cl2↑。某研究性学习兴趣小组对该厂生产的烧碱样品进行如下探究。
2NaOH+H2↑+Cl2↑。某研究性学习兴趣小组对该厂生产的烧碱样品进行如下探究。
[提出问题]:烧碱样品中含有哪些杂质?
[猜想]:
(1)可能含有NaCl,作出此猜想的依据是电解的过程中氯化钠没有完全反应。
(2)可能含有碳酸钠,做出此猜想的理由是 (用化学方程式表示)。
[实验设计]
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量的烧碱样品置于试管中加水溶解,用手触摸试管外壁。 | 试管外壁发热。 | 原因是 |
| ②向①所得的溶液中加入盐酸至过量。 | 开始时无明显现象,过一段时间后有气泡产生。 | 说明样品中含有杂质 |
| ③向②所得的溶液中加入硝酸银溶液。 | 有白色沉淀产生。 | AgNO3+NaCl=AgCl↓+NaNO3 说明样品中含有杂质氯化钠 |

普通食盐的主要成份是NaCl和杂质,假设杂质不溶于水、受热不分解、与AgNO3不反应。王华同学测定普通食盐样品中氯化钠的质量分数时所进行的实验操作流程和实验数据如下图所示。
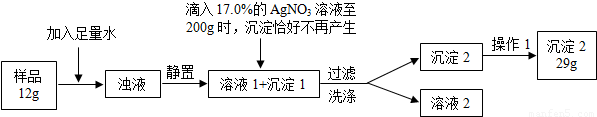
(实验中发生的化学反应方程式为:AgNO3+NaCl=AgCl↓+NaNO3)
请你完成空格和计算:
(1)王华进行操作1的目的是 _;
(2)求算样品中氯化钠的质量分数。(结果保留小数点后1位)
某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品,反应的化学方程式为:
2NaCl+2H2O 2NaOH+H2↑+Cl2↑。某研究性学习兴趣小组对该厂生产的烧碱样品进行如下探究。
2NaOH+H2↑+Cl2↑。某研究性学习兴趣小组对该厂生产的烧碱样品进行如下探究。
[提出问题]:烧碱样品中含有哪些杂质?
[猜想]:
(1)可能含有NaCl,作出此猜想的依据是电解的过程中氯化钠没有完全反应。
(2)可能含有碳酸钠,做出此猜想的理由是 (用化学方程式表示)。
[实验设计]
|
实验步骤 |
实验现象 |
解释或结论 |
|
①取适量的烧碱样品置于试管中加水溶解,用手触摸试管外壁。 |
试管外壁发热。 |
原因是 |
|
②向①所得的溶液中加入盐酸至过量。 |
开始时无明显现象,过一段时间后有气泡产生。 |
说明样品中含有杂质 |
|
③向②所得的溶液中加入硝酸银溶液。 |
有白色沉淀产生。 |
AgNO3+NaCl=AgCl↓+NaNO3 说明样品中含有杂质氯化钠 |
[反思]:小明认为上述实验不能说明样品中含有氯化钠,理由是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com