
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯.回答下列问题:
(1)写出制取用CH3COOH与C2H5
18OH发生反应制取乙酸乙酯的化学反应方程式
CH
3COOH+H
18OCH
2CH
3
CH
3CO
18OCH
2CH
3+H
2O
CH
3COOH+H
18OCH
2CH
3
CH
3CO
18OCH
2CH
3+H
2O
(2)浓硫酸的作用是:①
催化作用
催化作用
;②
吸水作用
吸水作用
.
(3)实验中饱和Na
2CO
3溶液的作用是(填字母序号)
BC
BC
.
A、中和乙酸和乙醇
B、中和乙酸并吸收部分乙醇
C、乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的小,有利于分层析出
D、加速酯的生成,提高其产率
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,为了防止
倒吸
倒吸
.
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是
分液
分液
.
(6)在该实验中,若用1mol乙醇和1mol乙酸在浓硫酸作用下加热,充分反应,能否生成1mol乙酸乙酯?为什么?
不能;该反应是可逆反应,反应不能进行到底;
不能;该反应是可逆反应,反应不能进行到底;
(7)下列描述能说明酯化反应已达到化学平衡状态的有(填序号)
②④⑤
②④⑤
.
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化.

 “酒是陈的香”,就是因为酒在储存过程中生成了有香 味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.
“酒是陈的香”,就是因为酒在储存过程中生成了有香 味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯. “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯.回答下列问题: CH3CO18OCH2CH3+H2O
CH3CO18OCH2CH3+H2O CH3CO18OCH2CH3+H2O
CH3CO18OCH2CH3+H2O (2009?江苏)下列有关试验操作的叙述正确的是( )
(2009?江苏)下列有关试验操作的叙述正确的是( )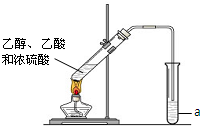 红酒密封储存时间越长,质量越好,其原因之一是储存过程中生成了具有香味的酯.在实验室可以用右图所示的装置制取乙酸乙酯.请回答:
红酒密封储存时间越长,质量越好,其原因之一是储存过程中生成了具有香味的酯.在实验室可以用右图所示的装置制取乙酸乙酯.请回答: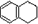 ,分子式是C10H12.常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2→C10H8Br4+4HBr.生成的四溴化萘常温下为固态,不溶于水,有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:
,分子式是C10H12.常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2→C10H8Br4+4HBr.生成的四溴化萘常温下为固态,不溶于水,有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下: