
题目列表(包括答案和解析)
A、B、C、D、E均为中学化学中的常见物质,它们之间的反应关系如图所示:
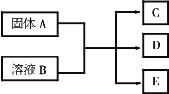
(1)若A为Na2CO3,C为温室气体,E为一种常用调味品.固体A与少量溶液B反应的化学方程式为________.
(2)若A为MnO2,C为黄绿色的有毒气体,则C与澄清石灰水反应的离子方程式为________________.
(3)若C为O2,D、E的焰色反应均显黄色,B、E可以相互转化,E与盐酸反应生成的气体能使澄清石灰水变浑浊.现有只含a mol B的溶液,欲使其变成只含amol E的溶液,可采取下列方法,试写出有关物质的化学式.
①只加入0.5a mol X,则X可能是________;
②只加入a mol Y,则Y可能是________.
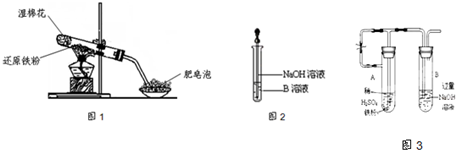
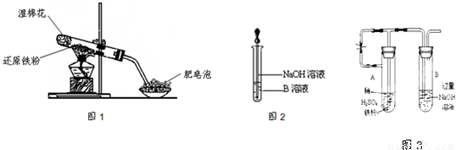
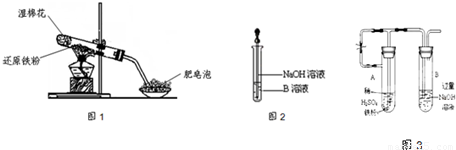
(17分)某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。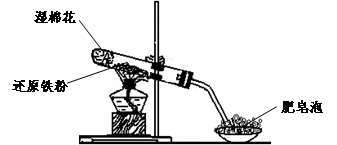
已知:①FeO + 2H+ = Fe2+ + H2O②Fe2O3 + 6H+ = 2Fe3+ +3 H2O ③Fe3O4 + 8H+ = Fe2+ +2Fe3+ +4 H2O
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为 。
(2)该同学欲确定反应一段时间后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是(只有一个选项符合题意) ,若溶液未变红色则说明硬质试管中固体物质的成分是(只有一个选项符合题意) 。
| A.一定有Fe3O4,可能有Fe | B.只有Fe(OH)3 | C.一定有Fe3O4和Fe |
| D.一定有Fe(OH)3,可能有Fe E.只有Fe3O4 |


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com