
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
| ‘™Àÿ | –‘÷ ªÚΩ·ππ–≈œ¢ |
| X | µ•÷ Œ™À´‘≠◊”∑÷◊”£¨∑÷◊”÷–∫¨”–3∂‘π≤”√µÁ◊”∂‘£¨≥£Œ¬œ¬µ•÷ ∆¯Ã–‘÷ Œ»∂®£¨µ´∆‰‘≠◊”ΩœªÓ∆√£Æ |
| Y | ∂˛º€—Ù¿Î◊”µƒÕ‚ŒßµÁ◊”≤„≈≈≤ºŒ™3d9 |
| T | ‘≠◊”∫ÀÕ‚sπϵ¿µÁ◊”◊Ð ˝µ»”⁄pπϵ¿µÁ◊”◊Ð ˝£ª»ÀÃ⁄∫¨¡ø◊Ó∂ýµƒ‘™Àÿ£¨«“∆‰µ•÷ «≥£º˚µƒ÷˙»ºº¡ |
| Q | µ⁄»˝÷Ð∆⁄÷˜◊‘™Àÿ÷–‘≠◊”∞Îæ∂◊Ó–° |



| ‘™Àÿ | –‘÷ ªÚΩ·ππ–≈œ¢ | X | µ•÷ Œ™À´‘≠◊”∑÷◊”£¨∑÷◊”÷–∫¨”–3∂‘π≤”√µÁ◊”∂‘£¨≥£Œ¬œ¬µ•÷ ∆¯Ã–‘÷ Œ»∂®£¨µ´∆‰‘≠◊”ΩœªÓ∆√£Æ | Y | ∂˛º€—Ù¿Î◊”µƒÕ‚ŒßµÁ◊”≤„≈≈¡–Œ™3d9 | T | ‘≠◊”∫ÀÕ‚sπϵ¿µÁ◊”◊Ð ˝µ»”⁄pπϵ¿µÁ◊”◊Ð ˝£ª»ÀÃ⁄∫¨¡ø◊Ó∂ýµƒ‘™Àÿ£¨«“∆‰µ•÷ «≥£º˚µƒ÷˙»ºº¡£Æ | Q | µ⁄»˝÷Ð∆⁄÷˜◊‘™Àÿ÷–‘≠◊”∞Îæ∂◊Ó–°£Æ |
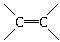
( 9∑÷)A°¢B∂º «∂Ã÷Ð∆⁄‘™Àÿ£¨‘≠◊”◊ÓÕ‚≤„µÁ◊”≈≈≤º Ω∑÷±Œ™(n£´1)sx°¢nsx+1npx+3°£A”ÎBø…–Œ≥…ªØ∫œŒÔD°£D»Ð”⁄ÀÆ ±”–∆¯Ã“ð≥ˆ£¨∏√∆¯ÃÂƒÐ π¥¯ª–«µƒƒæÃı∏¥»º°£«Îªÿ¥œ¬¡–Œ £∫
(1)±»ΩœµÁ¿ÎƒÐ£∫I1(A)________I1(B)(ÃÓ°∞>°±ªÚ°∞<°±£¨œ¬Õ¨)£¨±»ΩœµÁ∏∫–‘£∫A________B°£
(2)Õ®≥£A‘™ÀÿµƒªØ∫œº€ «________£¨∂‘A‘™Àÿ≥ œ÷’‚÷÷º€Ã¨Ω¯––Ω‚ Õ£∫
¢Ÿ”√‘≠◊”Ω·ππµƒπ€µ„Ω¯––Ω‚ Õ£∫ _______________________________________°£
¢⁄”√µÁ¿ÎƒÐµƒπ€µ„Ω¯––Ω‚ Õ£∫ ___________________________________________°£
¢€–¥≥ˆD∏˙ÀÆ∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫_______________________________________°£
œ¬Õº «Na°¢Cu°¢Si°¢H°¢C°¢Nµ»‘™Àÿµ•÷ µƒ»€µ„∏þµÕÀ≥–Ú£¨∆‰÷–c°¢dæ˘ «»»∫ÕµÁµƒ¡ºµºÃ°£
(1)«Î–¥≥ˆ…œÕº÷–dµ•÷ ∂‘”¶‘™Àÿ‘≠◊”µƒµÁ◊”≈≈≤º Ω_____________°£
(2)µ•÷ a°¢f∂‘”¶µƒ‘™Àÿ“‘‘≠◊”∏ˆ ˝±»2°√1–Œ≥…µƒ∑÷◊”(œýÕ¨Ãıº˛œ¬∂‘«‚∆¯µƒœý∂‘√Ð∂»Œ™14)÷–∫¨_____________∏ˆ¶ƒº¸∫Õ_____________∏ˆ¶–º¸°£
(3)a”Îbµƒ◊È≥…‘™Àÿ–Œ≥…µƒ 10µÁ◊”÷––‘∑÷◊”µƒø’º‰ππ–Õ «_____________£ª”…∏√∑÷◊”ππ≥…µƒŒÔ÷ “◊“∫ªØµƒ‘≠“Ú «____________________________________________________°£
(4)e∂‘”¶µƒ‘™Àÿ–Œ≥…µƒ—ıªØŒÔµƒæßÿý–ÕŒ™____________æßð£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com