
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
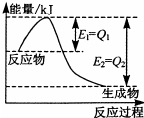 ‘À”√ªØ—ß∑¥”¶‘≠¿Ì—–æøµ™°¢¡Ú°¢¬»µ»µ•÷ º∞∆‰ªØ∫œŒÔµƒ∑¥”¶”–÷ÿ“™µƒ“‚“£Æ
‘À”√ªØ—ß∑¥”¶‘≠¿Ì—–æøµ™°¢¡Ú°¢¬»µ»µ•÷ º∞∆‰ªØ∫œŒÔµƒ∑¥”¶”–÷ÿ“™µƒ“‚“£Æ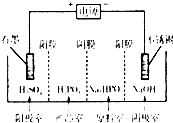 “—÷™£∫Cu£®OH£©2 «∂˛‘™»ıºÓ£ª—«¡◊À·£®H3PO3£© «∂˛‘™»ıÀ·£¨”ÎNaOH»Ð“∫∑¥”¶£¨…˙≥…Na2HPO3£Æ
“—÷™£∫Cu£®OH£©2 «∂˛‘™»ıºÓ£ª—«¡◊À·£®H3PO3£© «∂˛‘™»ıÀ·£¨”ÎNaOH»Ð“∫∑¥”¶£¨…˙≥…Na2HPO3£Æ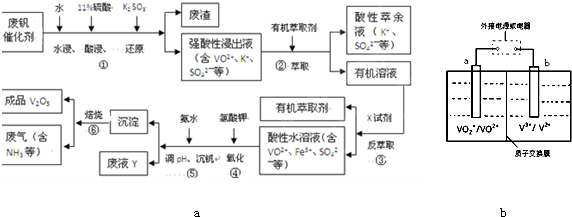
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| ∑∞≥¡µÌ¬ /% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
| ∑≈µÁ |
| ≥‰µÁ |
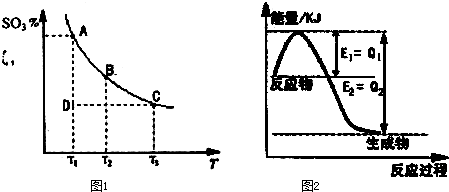
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com