
题目列表(包括答案和解析)

- 4 |
人体血液里Ca2+的浓度一般采用g/cm3来表示(即1 cm3血样中含有的Ca2+的质量)。抽取 一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得弱酸草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
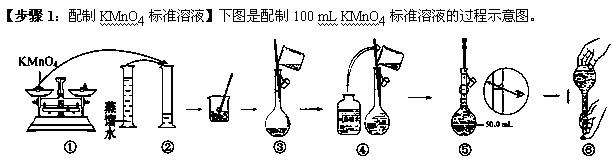 (1)请你观察图示判断,其中不正确的两项操作有 (填序号);
(1)请你观察图示判断,其中不正确的两项操作有 (填序号);
(2)其中确定100 mL溶液体积的仪器是__________________
(3)如果用图示的操作所配制的溶液进行实验,在其他操作正确的情况下,所配制的溶液浓度将
______(填“偏大”或“偏小”)。
【步骤2:测定血液样品中Ca2+的浓度】抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol/L 酸性KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(4)写出草酸与酸性KMnO4溶液反应的离子方程式 。
(5)滴定的终点为 。
(6)经过计算,血液样品中Ca2+的浓度为__________g/cm3。

| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |

| OH- |
| H+ |
| c(HCO3-):c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
为测定人体血液中Ca2+的含量,设计了如下方案:

有关反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4 K2SO4+2MnSO4+10CO2↑+8H2O。若血液样品为15mL,滴定生成的草酸消耗了0.001mol·L-1的KMnO4溶液15.0mL,则这种血液样品中的含钙量为
A.0.001mol·L-1 B.0.0025mol·L-1 C.0.0003mol·L-1 D.0.0035mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com