
题目列表(包括答案和解析)

请完成下列问题:
(1)指出K可能所属的晶体类型:_____________________。
(2)写出指定物质的化学式:C_______________,F______________。
(3)写出图中下列反应的离子方程式:反应③___________,反应⑤_____________。
(4)写出反应④的化学方程式:_____________________________。
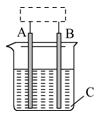
 (2010?潍坊一模)研究化学反应原理对于生产生活是很有意义的.
(2010?潍坊一模)研究化学反应原理对于生产生活是很有意义的.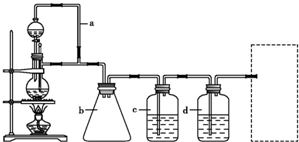 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:CH3CH-CH2+CO+H2
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:CH3CH-CH2+CO+H2| 一定条件 |
| H2 |
| Ni,△ |
| 浓H2SO4 |
| △ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com