
题目列表(包括答案和解析)
| ||
| ||
| ||
| △ |
| ||
| △ |

元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4,M原子的最外层电子数与次外层电子数之比为3∶4,且M原子的质子数是Y原子的2倍;N-、Z+、X+ 离子半径逐渐减小;化合物XN常温下为气体,据此回答: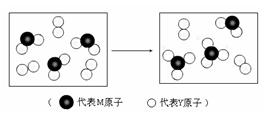
(1)写出Z与N形成化合物的电子式 。
(2)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式: 。
(3)下图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:
。
部分中学化学常见元素原子结构及性质如表所示:
序号元素结构及性质
①AA单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5
②BB原子最外层电子数是内层电子总数的
③CC是常见化肥的主要元素,单质常温下呈气态
④DD单质被誉为“信息革命的催化剂”,是常用的半导体材料
⑤E通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物
⑥FF在周期表中可以排在ⅠA族,也有人提出排在ⅦA族
(1)A原子在周期表中的位置为________。
(2)B与C形成的化合物的化学式为________,它属于________化合物(填“离子”或“共价”)。
(3)F与E可以形成10电子和18电子的两种化合物X和Y,区别X与Y的水溶液的实验方法是________________________________________________________________。
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱_____________________________________________________________。
(5)列举一个实验事实证明A、B两种元素单质还原性的强弱_________________________________________________________________。
元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4,M原子的最外层电子数与次外层电子数之比为3∶4,且M原子的质子数是Y原子的2倍;N-、Z+、X+ 离子半径逐渐减小;化合物XN常温下为气体,据此回答:
(1)写出Z与N形成化合物的电子式 。
(2)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式: 。
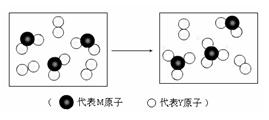
(3)下图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com