
题目列表(包括答案和解析)
4. 下列说法你认为缺乏科学依据的是
A.在水溶液中发生化学反应,反应速度比较快而且充分
B.水中Ca2+、Mg2+的增多会引起水体的富营养化污染
C.有人进入久未开启的菜窖窒息死亡
D.“曾青得铁则化为铜”是指将铁片放入氯化铜、硝酸铜等溶液中都可置换出铜
3. 下图表示的实验方法或操作正确的是:
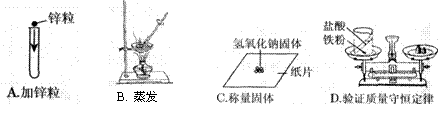
2. 对容器口进行磨砂处理可提高容器的密封性。下列仪器中对容器口没有进行磨砂处理
的是

1. 下列物质属于纯净物的是:
A.天然气 B. 乙醇汽油 C. 纯碱 D. 加铁酱油
27.(6分) 星期天,小强的妈妈要焙制面包,叫小强取商店买回一包纯碱(含有少量氯化钠,其余杂质忽略不计),小强仔细看了包装说明(如下图),并产生疑问:

回到学校,他取出从家里带来的一小包纯碱样品进行实验:准确称取5.5 g样品放入烧杯中,在滴加盐酸至刚好完全反应(忽略CO2溶于水),共用去稀盐酸25 g,得溶液质量为28.3 g。求:
(1)通过计算判断纯碱样品中碳酸钠的质量分数是否与包装说明相符;(计算结果精确到0.1%)
26.(4分)某工厂化验室用15%的氢氧化钠溶液洗涤75g石油产品中残余的硫酸,共消耗氢氧化钠溶液40g,洗涤后的溶液呈中性。计算:
(1)石油产品中残余硫酸的溶质质量分数;
(2)生成硫酸钠的质量。
25.(5分)育才学校化学活动小组查阅资料发现,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质,他们要除去杂质得到精盐,设计了下列实验方案(序号①~⑧表示实验操作,用于沉淀的试剂均稍过量):

根据上述方案,回答下列问题:
(1)操作①能否改用硝酸钡溶液?说明原因。 。
(2)第⑤步操作的名称是 。
(3)实验中加入“Na2CO3溶液”的目的是 。
(4)滤液的主要成分有 。
(5)利用提供的沉淀试剂,再写出一种添加试剂的操作顺序(填序号): 。
24.(6分)我们的日常生活离不开金属。
(1)地壳中含量最多的金属元素是 。
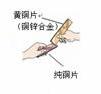
(2)下图是两块金属片相互刻划后,在纯铜片上有明显的划痕。该实验探究的目的是 。
(3)清末铝制艺术品至今保存完好,艺术品未被锈蚀的主要原因是 。
A.铝不易被氧化
B.铝的金属活动性比较弱
C.铝表面的氧化膜具有保护作用
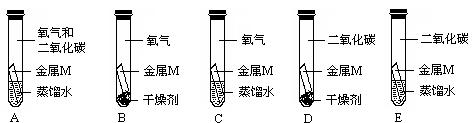
(4)据有关资料报导,每年因锈蚀而报废的金属相当于年产量的20%-40%。金属M长期露置于空气中,表面已被锈蚀。经检测,锈蚀物中除含有M外,还含有C、H、O三种元素。根据质量守恒定律推测:使金属M锈蚀的物质中一定有 (填化学式,下同),可能有 。
(5)小芳同学为了验证空气中的O2是否参加了反应,设计了如下几个实验,你认为其中必须要做的实验
是 。
说明:所用蒸馏水经煮沸迅速冷却;固体干燥剂只吸水且不与其他物质反应。
23.(6分)现有两包样品,若取少量分别溶于水得甲、乙两溶液,它们中的溶质是由KNO3、FeCl3、Fe2(SO4)3、NaNO3、NaOH、Na2SO4中的一种或几种组成,为确定其组成,有同学进行了下图所示实验(假设每步均恰好完全反应),其中白色沉淀B和C均为不溶于稀硝酸的白色沉淀。试推测:

(1)A是 ,溶液甲中一定不含 。
(2)若测定溶液甲中溶质只有FeCl3,则从原两包样品中各取少量混合,溶液乙中一定含有 。
(3)若溶液甲中不止一种溶质,则溶液乙中最多含 种溶质。
(4)溶液甲最多含有 种物质,其组成是 。
22.(5分)某同学为探究可燃物燃烧的条件,他查阅资料得知:白磷着火点为40℃ ,红磷着火点为240℃,它们在空气中燃烧都会生成刺激呼吸道的白烟--五氧化二磷,五氧化二磷易溶于水,并能与水反应。他按下图所示装置进行对比实验:
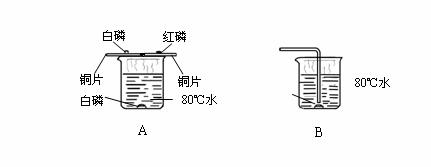
(1)用图A所示装置进行实验,观察到的现象是铜片上的白磷燃烧产生白烟,铜片上的红磷和水中的白磷不燃烧再用图B所示装置进行实验;观察到不通氧气时,热水中的白磷不燃烧,通氧气时,热水中的白磷燃烧。根据上述实验得出,可燃物燃烧的条件是 。
(2)根据燃烧的条件,选择填空。用扇子扇炉火不会熄灭,而是越扇越旺,原因是 ;用扇子扇蜡烛的烛火一扇就立即熄灭,原因是 (填序号)。
A.可快速地提供燃烧所需的氧气
B.空气流动虽带走热量,但温度未降到着火点以下
C.主要是空气流动带走热量,温度降到着火点以下
(3)图A与图B所示实验相比,符合环保要求的是 。
(4)为探究实验后溶液的性质,在图B烧杯中滴入几滴石蕊试液,溶液呈红色,说明五氧化二磷与水反应所得溶液呈 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com