
题目列表(包括答案和解析)
30.(3分)20g硫酸铜溶液与10g氢氧化钠溶液混合后,恰好完全反应,得到1.96g沉淀,求硫酸铜溶液中的溶质的质量分数。
29. (5分) 现有A、B、C、D、E五种化合物分别由Na+、Ba2+、 Mg2+ 、OH- 、CO2-3 、SO2-4离子组成,根据下列事实写出有关物质的化学式(一种离子可以参与构成多种物质)。
①A是不溶于水也不溶于硝酸的物质
②B的水溶液呈碱性,若向其中加入C,则生成A。
③D可溶于水,在D中加入B产生白色沉淀,再加入盐酸沉淀部分溶解。
④E可溶于水,加入B也能生成白色沉淀,加盐酸则沉淀全部溶解,并产生无色气体。




 A
B
C
D
E
。
A
B
C
D
E
。
28.(6分)下图表示各物质间的转化关系:
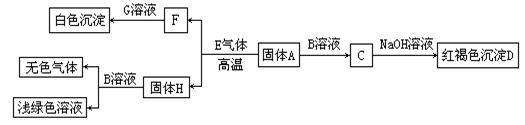
根据推断,将下列字母所代表的物质的化学式填在相应的横线上:
A ;D ;E ;F ;G ;H 。
27.(4分)在一次自主探究实验中,教师为同学们提供下列药品:CuSO4溶液、Na2CO3溶液、Ba(NO3)2溶液、NaOH溶液、稀盐酸。A、B、C三组同学任选药品相互混合进行探究。探究时发现:CuSO4溶液与Na2CO3溶液混合产生的沉淀不是白色的。实验后,同学在集中清理废液时发现:
(1)A组废液中有蓝色沉淀;B组废液中无沉淀;C组废液中有白色沉淀。
(2)先将A组废液倒入废液桶中,然后依次倒入B、C组废液。倒入B组废液时,沉淀全部溶解;再倒入C组废液,观察到有气泡产生,测得混合溶液pH<7。
由此可以推断:
A组同学在实验中一定未使用的一种药品是 。
B组同学在实验中一定使用了的一种药品是 。
C组同学实验使用的药品中一定含有的阴离子是 。
三组废液混合后,废液中含有的沉淀是 。
26.(6分) 某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
|
检测次数 |
溶液中检测出的物质 |
|
第一次 |
KCl、K2SO4、Na2CO3、NaCl |
|
第二次 |
KCl、BaCl2、Na2SO4、K2CO3 |
|
第三次 |
Na2SO4、KCl、K2CO3、NaCl |
(1)三次检测结果中第__________次检测结果不正确。
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子,先向溶液中加入过量的_______________溶液,其目的是__________________;然后继续加入过量的_____________溶液,其目的是______________________;过滤后,再向滤液中加入_____________溶液。
25.(6分)某同学收集了班级同学“氢气还原氧化铜”实验后的固体残渣(含铜和氧化铜),进行如下实验:
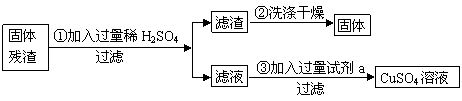
(1)步骤①中发生反应的化学方程式为: 。
 (2)过滤时,需要的仪器组合为 。
(2)过滤时,需要的仪器组合为 。
A. ①②③④ B. ①②⑤⑥ C. ①②④⑤ D. ③④⑤⑥
(3)步骤②得到的固体为 (填物质名称)。
(4)步骤①所得滤液中溶质的化学式是 。
(5)步骤③中加入的试剂a为 。
A. 氢氧化铜 B. 铜 C. 镁 D. 硫酸铜
(6)步骤③中加入的试剂a为什么需要过量? __ 。
24.(2分) 将Mg、Al、Zn分别放入相同溶质质量分数的盐酸中,反应完成后,放出的氢气质量相同,其可能原因是 。 ①放入的三种金属质量相同,盐酸足量 ②放入的Mg、Al、Zn的质量比为12︰9︰32.5,盐酸足量 ③盐酸的质量相同,放入足量的三种金属 ④放入的盐酸质量比为3︰2︰1,反应后无盐酸剩余
23.(5分)有一混合溶液,可能由H2SO4、Na2CO3、Na2SO4、NaCl、NaNO3、CuSO4六种溶液中的若干种混合而成。
为研究其组成,小明同学进行了下列探究:
[提示假设]混合溶液由两种物质组成;
[实验与推断]请你根据小明同学的实验操作,分析实验现象,做出相应判断:
|
步骤 |
实验操作 |
实验现象 |
推断 |
|
(1) |
观察混合溶液 |
混合溶液无色、澄清 |
一定没有
|
|
(2) |
用pH试纸测定混合溶液的pH |
测定结果,pH=2 |
一定没有
|
|
(3) |
相混合溶液中滴入足量Ba(NO3)2溶液 |
有白色沉淀出现 |
该沉淀是
|
|
(4) |
向上述过滤所得的滤液中滴加AgNO3溶液 |
无明显现象 |
一定没有
|
[实验结论]混合溶液可能的组成是 。
22.(3分)氢氧化钾是我国古代纺织业常用作漂洗的洗涤剂,古人将贝壳(主要成分为碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中相互作用,就生成了氢氧化钾,请用化学方程式表示上述反应:
分解反应
化合反应
复分解反应
21.(8分)按要求写出下列反应的化学方程式,并回答相关问题。
(1)铜棒插入硝酸汞溶液中
(2)氧化铁跟盐酸反应
(3)氢氧化钠溶液跟稀硫酸反应
(4)二氧化硫是形成酸雨的主要气体之一,工业上为了防止二氧化硫对大气的污染,通常用氢氧化钠溶液吸收它
(5)写出下列变化的化学方程式




 石灰石 生石灰
消石灰 烧碱
石灰石 生石灰
消石灰 烧碱
①
②
③
其中属于中和反应的是 。(填序号)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com