
题目列表(包括答案和解析)
8.8g+3.6g-2.8g=9.6g
∴B和D的质量比为:9.6g:3.6g=8:3
答:略.
例1:实验室用加热氯酸钾和少量二氧化锰的混合物来制取氧气,已知反应前二氧化锰占混合物质量的20%,加热一段时间后,剩余固体中二氧化锰占25%,求氯酸钾的分解百分率.
解:设原混合物中二氧化锰质量为1g,
则原混合物质量为:1g÷20%=5g
剩余固体质量为:1g÷25%=4g
由质量守恒定律得:氧气质量为5g-4g=1g
设参加反应的氯酸钾质量为x
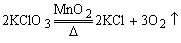
245 96
x 1g
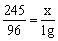 x=2.55g
x=2.55g
则KClO3的分解率:
答:KClO3的分解率为63.75%.
例2:实验室中,用氢气还原氧化铜25g,当大部分固体变红时,停止加热,冷却后称得残留固体为21g,求参加反应的氧化铜的质量.
解:设参加反应的氧化铜质量为x,则生成铜的质量为21g-(25g-x)=x-4g

80 64
x x-4g

x=20g
答:参加反应的氧化铜质量为20g.
例3:煅烧含CaCO380%的石灰石100t,生成CO2多少吨?若石灰石中的杂质全部进入生石灰中,可得这样的生石灰多少吨?
解:设生成CO2的质量为x

100 44
100t×80% x
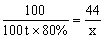 x=35.2t
x=35.2t
生石灰质量:100t-35.2t=64.8t
答:生成CO2 35.2t,得生石灰64.8t.
例4:某钢铁厂用580吨含Fe3O480%的磁铁矿(其余为不含铁的杂质),可炼得含杂质为4%的生铁多少吨?
解:设可炼得生铁的质量为x

232 168
580t×80% x·(1-4%)
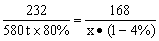 x=350t
x=350t
答:略.
例5:在反应A+3B=2C+2D中,C和D的相对分子质量比为22:9,2.8gA与一定量B完全反应后,生成8.8gC,求反应中B和D的质量比是多少.
解:设生成D的质量为x
A+3B=2C+2D
44 18
8.8g x
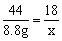 x=3.6g
x=3.6g
则参加反应的B的质量为:
5.常用方法:
(1)守恒法 (2)关系式法 (3)差量法
(4)极值法 (5)讨论法 (6)特殊值法
4.常用换算计算式:
(1)气体密度(g/L)
(2)物质纯度
3.注意事项:
(1)化学方程式必须书写正确
(2)同一题目中不同未知量不能用同一字母表示
(3)各相关物质的相对分子质量必须计算准确
(4)各相关量必须写在对应物质化学式的下面
(5)代入化学方程式中进行计算的相关量必须是纯净物的(不包括未参加反应的质量)
2.一般解题步骤:
(1)审清题意,设未知量
(2)正确写出有关的化学方程式
(3)求出相关物质的质量比,并把相关的已知量和未知量写在相应质量比的下边
(4)列出比例式
(5)求出未知量
(6)简明地写出答案
可概括为:解、设、方、关、已未知、比例、求解、答仔细.
1.化学方程式在量的方面的含义:
例如: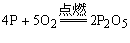
在量的方面:(1)表示反应物与生成物的质量比为124:160:284
(2)反应物总质量份数(124+160)等于生成物总质量份数(284)符合质量守恒定律
24、(5分)水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要关心水、爱护水、节约用水。
(1)我国规定生活饮用水的水质必须达到下述四项指标:a.不得呈现异色 b.不得有异味 c.应澄清透明 d.不得含有细菌和病毒。其中“c指标”可以通过 操作达到。
(2)生活中可以采用 区分硬水和软水,可以通过 的方法降低水的硬度。
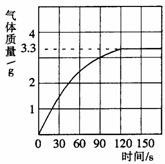 (3)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如下图所示。
(3)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如下图所示。
①从图中可以看出,12.5g水垢与盐酸反应后生成的二氧化碳最多是
g。
②水垢中碳酸钙的质量分数是多少?
23.(2分)“三鹿奶粉事件”的“元凶”是三聚氰胺,其化学式为C3H6N6。三聚氰胺常被用作化工原料,微溶于水,有轻微毒性。三聚氰胺的相对分子质量是 ,其中碳、氢、氮原子的个数比为_____________,碳、氢、氮的元素质量比为 ,因三聚氰胺的含氮量较高,所以被不法分子添加至奶制品中,以“提高”蛋白质含量。252克三聚氰胺中氮元素质量为 克。
22、 (4分)某小组同学在协助老师整理化学试剂时,发现一瓶标签残缺的无色液体(如下图)(温馨提示:标签上的5%表示该混合物中主要成分所占的质量分数)。他们对此瓶无色液体是什么产生了兴趣,于是进行了如下探究。
(4分)某小组同学在协助老师整理化学试剂时,发现一瓶标签残缺的无色液体(如下图)(温馨提示:标签上的5%表示该混合物中主要成分所占的质量分数)。他们对此瓶无色液体是什么产生了兴趣,于是进行了如下探究。
[大胆猜想]猜想一:水 猜想二:稀硫酸 猜想三:过氧化氢溶液
小组同学对标签又进行了仔细的观察、分析,他们一致认为猜想一不合理。理由是
。
[设计方案]同学们结合所学知识设计出如下探究方案:
向盛有少量二氧化锰的试管中加入适量的该液体,并将带火星的木条放在试管口。
[实验与事实]按上述方案进行实验,发现有大量气泡产生,带火星的木条复燃。
[结论与解释](1)以上事实证明猜想 是正确的;
(2)产生气体的反应可用化学方程式表示为 。
[反思与评价](1)在实验中,某同学提出应该先将气体收集,然后用带火星的木条检验,你认为
(填“有”或“没有”)必要。
(2)为避免在今后的实验中出现标签残缺的情况,在倾倒液体时应注意 。
[拓展与迁移] 根据探究结果,重新贴好标签。标签上化学式中氧元素的化合价为 价(已知氢元素显+1价)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com