
题目列表(包括答案和解析)
27.(6分)欲测定某石灰石样品中碳酸钙的质量分数(石灰石样品中的杂质受热不分解,且不与酸反应),甲、乙两位同学分别设计了如下两个实验方案:
方案一:①称取石灰石样品质量8g;②用酒精灯加热样品,直至质量不再改变;③将固体残余物放在干燥的器皿中冷却后称得质量6.9 g;④计算。
方案二:①称取石灰石样品质量8 g;②加入质量分数为7.3%的盐酸100 g,使碳酸钙完全反应;③向反应后的溶液中加入含溶质3.2 g的氢氧化钠溶液,恰好中和多余的盐酸;④计算。
请回答下列有关问题:
(1)100g质量分数为7.3%的盐酸中,溶质氯化氢的质量为 g;
(2)你认为上述方案中,切实可行的是方案 ,不选用另一方案的原因是
;
(3)求方案二样品中碳酸钙的质量分数。
试题结束,请认真检查!考试终了钟声响起再交卷。
26.(4分)化学课外活动小组的同学对某炼铁厂生产的生铁(杂质不与酸反应)进行组成分析。其实验数据如下表,请计算生铁的纯度。(精确到0.1%)
实验记录
|
实验步骤 |
数据 |
|
(1)称取生铁样品放入烧杯中 |
14.5g |
|
(2)加入足量15%的盐酸 |
200.0g |
|
(3)称量反应后烧杯中物质总质量 |
214.0g |
25.(10分)某化学兴趣小组想探究某一温度下氯化钠饱和溶液的酸碱度。探究过程如下:
[猜想或假设]溶液的pH可能为:①pH<7,② ,③ 。
[设计和实验]要测定该溶液的酸碱度,除有正确的操作步骤外,其中不能采用下列物质中的
(填序号)来进行实验。
①pH试纸 ②紫色石蕊试液 ③酚酞试液
组内同学进行了如下实验:
甲同学:取pH试纸放在玻璃片上,用玻璃棒蘸取氯化钠溶液沾在pH试纸上,把试纸显示的颜色与标准比色卡比较,测得pH=7。
乙同学:取pH试纸放在玻璃片上,先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取氯化钠溶液沾在pH试纸上,把试纸显示的颜色与标准比色卡比较,测得pH=7。
丙同学:将pH试纸直接浸入氯化钠溶液中,把试纸显示的颜色与标准比色卡比较,测得pH=7。
[评价与反思]三位同学中操作正确的是 同学。
指出其于同学的操作错误:
同学: ;
同学: ;
[结论与分析]丙同学得出:“凡是盐溶液的pH都等于7”,你认为该同学结论
(填“正确”或“不正确”)。
如不正确,请举一例说明 (如正确,该处不填)。
24.(11分)金属材料是现代生活和工业生产中应用极为普遍的一类物质。
(1)钛合金是21世纪的重要材料,具有熔点高、可塑性好、抗腐蚀性强、与人体有很好的“相容性”等优良性能。金属的下列用途:①用来做保险丝 ②用来制人造骨 ③用于制造船舶 ④用于制造航天飞机。其中与钛合金性能符合的是 (填序号)。
(2)铁是一种最主要的金属材料,实验室里用一氧化碳还原氧化铁得到铁,实验过程中,先通入一氧化碳目的是 。
炼铁厂常以焦炭、赤铁矿、空气等为主要原料炼铁,反应过程如下:



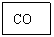








写出② ③两步的化学方程式 、 。
 (3)矿物的储量有限,而且不可再生,我们必须保护金属资源并进行金属的回收利用。
(3)矿物的储量有限,而且不可再生,我们必须保护金属资源并进行金属的回收利用。
某兴趣小组同学欲从含有硫酸、硫酸亚铁和硫酸铜的废液中,回收全部金属铜,应先加入 。充分反应后过滤,滤渣中含有 。继续处理可以得到纯净的金属铜和硫酸亚铁固体。
(4)在学习了金属资源保护内容以后,兴趣小组同学对金属的锈蚀做了观察,发现残留水的铁锅在与水面接触的部位最易生锈;家用的铜质水龙头也生了一层绿色的铜锈。回忆已有的知识,铁生锈的原因是 。那么铜生锈的原因是什么?查阅有关资料:铜锈的主要成份是Cu2(OH)2CO3。他们除依照铁钉锈蚀条件的探究方法进行实验外,还补充做了铜锈蚀与 有关系的实验。请写出一种防止铁或铜等金属制品生锈的具体方法 。
23.(6分)在实验室里常采用过氧化氢和二氧化锰混合的方法制取氧气。请回答下列问题:
(1)反应的化学方程式为 。
(2)用下图所给仪器可以组装出多套氧气的发生装置和收集装置。请你组装一套氧气的发生装置和收集装置,写出所选择的仪器编号 。

(3)简要说明你组装的气体发生装置的优点 。
(4)用你组装的装置收集氧气,如何知道氧气已收集满? 。
(5)这套气体发生装置也可以用来制取二氧化碳。如果选用碳酸钠粉末和稀盐酸来制取二氧化碳,为了控制反应速率,应对该气体发生装置如何改进?(可另增仪器)
。
22.(7分)A、B、C、D、E是初中化学中常见的物质,A为暗紫色固体,B为黑色固体。请根据图中物质间的相互转化关系,回答有关问题:

(l)检验气体甲的方法是_________________________________________。
(2)在固体C受热分解的过程中,固体B起___________作用。
(3)写出加热固体A的化学方程式:___________________________________。
(4)操作1的步骤是_________________,所需使用的仪器有_______________。
(5)固体F含有的物质可能是______________________________。(填化学式)
21.(8分) 根据下列要求写出反应的化学方程式:
(1)高温煅烧石灰石
(2)铁在氧气中燃烧
(3)锌粒与稀硫酸反应
(4)盐酸和氢氧化钠溶液反应
20.(2分)在反应2A+B=====3C+D中,A和B的相时分子质量之比为5:1,已知20g A与一定量B恰好完全反应,生成5g D,则在此反应中B和C的质量比为 。
19. (5分)木糖醇是一种理想的蔗糖替代品,适合糖尿病患者食用。
(5分)木糖醇是一种理想的蔗糖替代品,适合糖尿病患者食用。
(1)木糖醇的化学式为C5H12O5,它是由 种元素组成的,其中碳元素的质量分数为 。
(2)木糖醇和蔗糖的溶解度曲线如图,据图回答:
①30℃时,木糖醇的溶解度 蔗糖的溶解度。(选填“大于”、“小于”或“等于”)
②60℃时,向l00克水中加入80克木糖醇,充分溶解后,所得的溶液是 溶液(选填“饱和”或“不饱和”),该溶液的溶质质量分数为 。
18.(2分) 人皮肤pH一般在4.5~5.6之间,则皮肤表面显 性,如果某人皮肤的pH为8.2,现有下列四种pH不同的洗面奶供选购:① 4.5 ② 6.5 ③ 8.2 ④ 8.5 ;他最好购买 (填序号)号洗面奶。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com