
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
26Θ°ΝρΥαΆ≠ΓΓΓΓ ΑΉ…Ϊ≥ΝΒμ≤ΩΖ÷»ήΫβ
6.(2010Θ°’ψΫ≠…ή–Υ)26Θ°”–“ΜΑϋΑΉ…ΪΖέΡ©Θ§Ω…Ρή «”…ΝρΥαΆ≠ΓΔ¬»Μ·ΡΤΓΔΧΦΥαΡΤΓΔΝρΥαΡΤ÷–ΒΡ“Μ÷÷ΜρΦΗ÷÷Ήι≥…Θ§ΈΣΦλ―ιΤδ÷–ΒΡ≥…Ζ÷Θ§Ψ≠ Β―ιΒΟΒΫœ¬±μΘ§«κΆξ≥…œύΙΊΡΎ»ίΓΘ
|
Β―ι≤Ϋ÷ηΦΑœ÷œσ |
Ϋα¬έ |
|
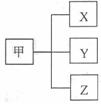
ΔΌΫΪ…Ό–μΑΉ…ΪΖέΡ©»ή”ΎΥ°ΒΟΒΫΈό…Ϊ»ή“ΚA |
ΑΉ…ΪΖέΡ©÷–“ΜΕ®ΟΜ”–____________________ |
|
ΔΎ‘ΎA÷–Φ”»κΉψΝΩœθΥα±Β»ή“ΚΘ§…ζ≥…ΑΉ…Ϊ≥ΝΒμBΘ§Ιΐ¬ΥΒΟ¬Υ“ΚC Δέ‘ΎΑΉ…Ϊ≥ΝΒμB÷–Φ”»κΉψΝΩœΓœθΥαΘ§__________________ Δή‘Ύ¬Υ“ΚC÷–Φ”»κœθΥα“χ»ή“ΚΘ§…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμ≤Μ»ή”ΎœΓœθΥα |
ΑΉ…ΪΖέΡ©÷–“ΜΕ®”–ΝρΥαΡΤΓΔΧΦΥαΡΤΚΆ¬»Μ·ΡΤ |
5.(2010Θ°’ψΫ≠Κΰ÷ί)15Θ°Ιιάύ «Έ“Ο«Ψ≠≥Θ”ΟΒΫΒΡ“Μ÷÷―ßœΑΖΫΖ®ΓΘ»τ”Οœ¬ΆΦΥυ ΨΒΡ–Έ ΫΕ‘Υυ―ß÷Σ ΕΫχ––ΙιάύΘ§‘ρ±μ÷–
ΓΓ ΒΡ―Γœν”κΆΦœύΖϊΒΡ «
|
―Γœν |
ΦΉ |
X |
Y |
Z |
|
A |
≥ΘΦϊΒΡΦν |
…’Φν |
¥ΩΦν |
λ ·Μ“ |
|
B |
≥ΘΦϊΒΡΩσΈο»ΦΝœ |
ΟΚ |
·”Ά |
Χλ»ΜΤχ |
|
C |
≥ΘΦϊΒΡΚœΫπ |
Η÷Χζ |
…ζΧζ |
―θΜ·Χζ |
|
D |
≥ΘΦϊΒΡ–––« |
ΒΊ«ρ |
ΧΪ―τ |
‘¬«ρ |
¥πΑΗΘΚA
4.(2010.’ψΫ≠ΚΦ÷ί)31Θ°Ρ≥―ß–ΘΒΡΩΈΆβΜνΕ·–ΓΉι“Σ≤βΕ®Ρ≥Ωι―ΈΦνΒΊ÷–ΒΡNaClΓΔNa2SO4ΘΜΓΔNa2CO3ΒΡΚ§ΝΩΘ§ΈΣ―ΈΦνΒΊΒΡΗΡ‘λΧαΙ©“άΨίΓΘœ¬Οφ «ΥϊΟ«ΒΡ≤βΕ®≤Ϋ÷ηΘΚ
ΓΓΓΓ (1)»ΖΕ®“Σ≤βΕ®ΒΊΩιΒΡ≤…―υΒψΓΘΓΓ
(2)ΫΪ≤…Φ·ΚΟΒΡΆΝ―υΝάΗ…ΓΔΖέΥιΓΔ≥ΤΝΩΘ§Φ”’τΝσΥ°≥δΖ÷ΫΝΑηΚσΙΐ¬ΥΘ§»Γ¬Υ“ΚΓΘ
ΓΓΓΓ (3)Ε‘Υυ»Γ¬Υ“ΚΫχ––“‘œ¬ Β―ιΘΚ( Β―ιΙΐ≥Χ÷–ΥυΦ” ‘ΦΝΨυ «ΉψΝΩΒΡΘ§ΒΟΒΫΒΡΥυ”–≥ΝΒμ÷–ΒΡ“θάκΉ”ΕΦά¥Ή‘‘≠ΆΝ»ά¬Υ≥ω“Κ÷–)
ΓΓΓΓ (4)≥ΤΝΩ Β―ι÷–ΒΟΒΫΒΡΗς÷÷≥ΝΒμ÷ ΝΩΘ§ΦΤΥψΒΟ≥ω―ΈΦνΒΊ÷–…œ ω»ΐ÷÷―ΈΒΡΚ§ΝΩΓΘ
«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)…ηΦΤ≤…―υΒψ ±”–œ¬Ν–ΥΡ÷÷ΖΫΑΗΘ§―Γ”ΟΖΫΑΗ__ΓΓΓΓ __ΫœΈΣΚœάμΓΘ
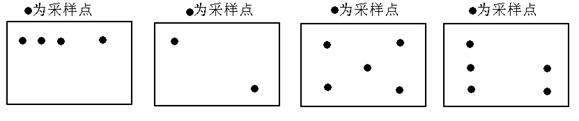
AΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ CΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ D
(2)…œ ω Β―ι÷– ‘ΦΝAΒΡΜ·―ß Ϋ «ΓΓΓΓΓΓΓΓ ΓΓΘ§ ‘ΦΝBΒΡΜ·―ß Ϋ «ΓΓΓΓΓΓΓΓ Θ§ΤχΧεΚΆ ‘ΦΝCΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «__ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3)»τ…œ ω Β―ι÷– ‘ΦΝAΈΣ¬»Μ·±Β»ή“ΚΘ§‘ρΑ¥…œ ω Β―ι≤Ϋ÷ηΉν÷’≤βΒΟΆΝ»ά÷– ΓΓΓΓΓΓΓΓΓΓΓΓΒΡΚ§ΝΩΤΪΗΏΓΘ
¥πΑΗΘΚ31Θ° (1)C,ΓΓ (2) Ba(NO3)2ΓΓ HNO3ΜρHCl ΘΜCO2 + Ba(OH)2 == BaCO3Γΐ+H2 OΘΜ
ΓΓΓΓ (3)NaCl(Μρ¬»Μ·ΡΤ)
29. (l)Ca(OH)2(Μρ«β―θΜ·ΗΤ)ΓΓΓΓ (2) Ba(N03)2 +Na2S04 =BaS04Γΐ +2 NaN03ΓΓΓΓ (3) AgCl
3.(2010Θ°’ψΫ≠Χ®÷ί)29,ΕΙΗ·Φ”ΙΛ ±–ηΦ”»κΡΐΙΧΦΝΘ§ΡΐΙΧΦΝΒΡΜ·―ß≥…Ζ÷ « ≤Ο¥ΘΩΆ®ΙΐΉ ΝœΜώœΛΘΚΡΐΙΧΦΝ÷–Ω…ΡήΚ§”–Na2SO4ΘΜΓΔCa(OH)2ΓΔMgCl2ΓΔNaClΒ»Θ§ΈΣ―ι÷ΛΤδ≥…Ζ÷Θ§–ΓΩ¬Ϋχ––ΝΥ»γœ¬ Β―ιΘΚ
ΓΓ
(1)ΗυΨί“‘…œœ÷œσΘ§ΡΐΙΧΦΝ»ή“Κ÷–ΩœΕ®ΟΜ”–ΓΓΓΓΓΓ ΓΘ
(2)–¥≥ω Β―ι2÷–ΖΔ…ζΒΡΜ·―ßΖ¥”ΠΖΫ≥Χ ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓ (3)–¥≥ω Β―ι3÷–≥ωœ÷ΒΡΑΉ…Ϊ≥ΝΒμΈο÷ ΒΡΜ·―ß ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
2.(10’ρΫ≠)29Θ°(6Ζ÷)œ¬ΆΦ±μ ΨΡ≥–©Έο÷ ΦδΉΣΜ·ΙΊœΒΓΘΤδ÷–AΓΔD «”…œύΆ§‘ΣΥΊΉι≥…ΒΡΙΧΧεΘ§«“AΈΣΉœΚΎ…ΪΘ§CΈΣΚΎ…ΪΖέΡ©Θ§BΓΔEΈΣ≥ΘΦϊΤχΧεΘΜX”κF «”…œύΆ§‘ΣΥΊΉι≥…ΒΡΈό…Ϊ“ΚΧεΘ§«“XΨΏ”–œϊΕΨ…±ΨζΉς”ΟΘΜY «“Μ÷÷Κλ…ΪΫπ τΓΘ«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
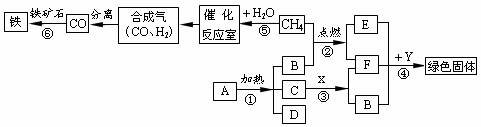
(1)AΒΡΜ·―ß Ϋ «ΓΓ ΓΓΓχΓΓ ΓΓΘΜ
(2)CΈο÷ ‘ΎΖ¥”ΠΔέ÷–ΒΡΉς”ΟΓΓ ΓΓΓχΓΓ ΓΓΓΓΘΜ
(3)–¥≥ωΖ¥”ΠΔΎΓΔΔήΓΔΔόΒΡΜ·―ßΖΫ≥Χ Ϋ:
ΔΎ ΓΓΓΓΓΓΓΓΓΓΓχ ΓΓΓΓΓΓΓΓΘΜΔήΓΓΓΓΓΓΓΓ Γχ ΓΓΓΓΓΓΓΓΓΓΘΜΔόΓΓΓΓΓΓ Γχ ΓΓΓΓΓΓΓΓΘΜ
(4)»τΫΪΚœ≥…Τχ÷–ΝΫΤχΧεΑ¥Ζ÷Ή” ΐ÷°±»ΈΣ1:1Ϋχ––Μ·Κœ(‘≠Ή”άϊ”Ο¬ ΈΣ100%)Θ§Ω…Κœ≥…Εύ÷÷”–ΜζΜ·ΙΛ≤ζΤΖΘ§–¥≥ωΤδ÷–“Μ÷÷Ω…Ρή≤ζΤΖΒΡΜ·―ß ΫΓΓΓΓ Γχ ΓΓΓΓΓΘ
(1)KMnO4ΓΓ
(2)¥ΏΜ·ΦΝΜρ¥ΏΜ·Ής”Ο
(3)ΔΎ CH4+2O2  ΓΓCO2+2H2O
ΓΓCO2+2H2O
Δή2Cu+O2+H2O+CO2ΘΫCu2(OH)2CO3
ΔόFe2O3+3CO 2Fe+3CO2(–¥≥…FeOΓΔFe3O4ΓΔFexOyΒΡ–Έ Ϋ«“’ΐ»ΖΗχΖ÷)
2Fe+3CO2(–¥≥…FeOΓΔFe3O4ΓΔFexOyΒΡ–Έ Ϋ«“’ΐ»ΖΗχΖ÷)
(4)CH2OΜρC2H4O2ΓΔC3H6O3ΓΔC4H8O4ΓΔC6H12O6(ΤδΥϋΚœάμ¥πΑΗΨυΗχΖ÷Θ§‘ΣΥΊΥ≥–ρ≤Μœό)
1.(10’ρΫ≠)28Θ°(6Ζ÷)œ÷”–“ΜΑϋΙΧΧεΖέΡ©Θ§Ω…Ρή «CaCO3ΓΔNa2CO3ΓΔNa2SO4ΓΔCuSO4ΓΔNaCl÷–ΒΡ“Μ÷÷ΜρΦΗ÷÷Θ§ΈΣ»ΖΕ®ΤδΉι≥…Θ§»Γ ΝΩ ‘―υΫχ––œ¬Ν– Β―ιΓΘ«κΗυΨί Β―ιœ÷œσ≈–ΕœΘΚ
(1)»Γ ‘―υ»ή”ΎΥ°Θ§ΒΟΒΫΈό…Ϊ≥Έ«ε»ή“ΚΘ§‘ρ¥ΥΙΧΧεΖέΡ©÷–“ΜΕ®ΟΜ”–ΓΓ Γχ ΓΓΓΓΓΓΓΔΓΓ Γχ ΓΓΓΓΓΘ
(2)»Γ…œ ω»ή“Κ ΝΩΘ§ΒΈΦ”ΙΐΝΩΒΡBaCl2»ή“ΚΘ§≥ωœ÷ΑΉ…Ϊ≥ΝΒμΘ§‘ΌΦ”»κΙΐΝΩΒΡœΓœθΥαΘ§≥ΝΒμ≤ΩΖ÷œϊ ß≤Δ≤ζ…ζΤχ≈ίΓΘ‘ρ¥ΥΙΧΧεΖέΡ©÷–“ΜΕ®”–ΓΓΓΓ Γχ ΓΓΓΓΓΔΓΓΓΓ Γχ ΓΓΓΓΓΘ
(3)»Γ≤Ϋ÷η(2) Β―ιΚσΒΡ…œ≤ψ«ε“ΚΘ§Φ”»κœΓœθΥαΓΔœθΥα“χ»ή“ΚΘ§≥ωœ÷ΑΉ…Ϊ≥ΝΒμΘ§”…¥ΥΗΟΆ§―ßΒΟ≥ω¥ΥΙΧΧεΖέΡ©÷–“ΜΕ®Κ§”–NaClΘ§Ρψ»œΈΣ¥ΥΫα¬έ «Ζώ’ΐ»ΖΓΓ ΓΓΓχ ΓΓ(ΧνΓΑ «Γ±ΜρΓΑΖώΓ±)ΓΘ
(4)Ε‘”Ύ «ΖώΚ§”–NaClΘ§Ρψ»œΈΣ”ΠΕ‘≤Ϋ÷η(2)Ής»γΚΈΗΡΫχΓΓΓΓ ΓΓΓχ ΓΓΓΓΓΓ(»τ≤Ϋ÷η(3)ΧνΓΑ «Γ±Θ§¥ΥΩ’≤ΜΉς¥π)ΓΘ
(1)CaCO3ΓΓΓΓ CuSO4
(2)Na2CO3ΓΓ Na2SO4
(3)Ζώ
(4)ΫΪBaCl2»ή“ΚΜΜ≥…Ba(NO3)2»ή“ΚΜρBa(OH)2»ή“Κ
4.(2010Θ°’ψΫ≠Κΰ÷ί)20Θ°–ΓΟςΆ§―ßΆυ«β―θΜ·ΡΤ»ή“Κ÷–ΒΈΦ”œΓ―ΈΥα―–ΨΩ÷–ΚΆΖ¥”Π ±Θ§ΆϋΦ«ΝΥΒΈΦ”ΥαΦν÷Η ΨΦΝΓΘΈΣΝΥ»Ζ»œΒΈΦ”ΒΡ―ΈΥα «Ζώ“―Ψ≠ΙΐΝΩΘ§¥”…’±≠÷–»Γ…ΌΝΩΖ¥”ΠΚσΒΡ»ή“Κ”Ύ ‘Ιή÷–Θ§”ΟΡ≥÷÷ ‘ΦΝΫχ––Φλ
ΓΓ ―ιΓΘœ¬±μ «–ΓΟςΆ§―ß…ηΦΤΒΡ Β―ιΖΫΑΗΘ§Τδ÷–≤Μ’ΐ»ΖΒΡ «
|
Β―ιΖΫΑΗ |
Ι”ΟΒΡ ‘ΦΝ |
≈–ΕœΒΡΖΫΖ®ΓΓ |
|
A |
ΧζΖέ |
»γΙϊ”–Τχ≈ί≤ζ…ζΘ§±μΟς―ΈΥα“―Ψ≠ΙΐΝΩ |
|
B |
pH ‘÷Ϋ |
»γΙϊpH<7Θ§±μΟς―ΈΥα“―Ψ≠ΙΐΝΩ |
|
CΓΓ |
œθΥα“χ»ή“Κ |
»γΙϊ”–ΑΉ…Ϊ≥ΝΒμ≤ζ…ζΘ§±μΟς―ΈΥα“―Ψ≠ΙΐΝΩ |
|
D |
Ήœ…Ϊ ·»ο ‘ΦΝ |
»γΙϊ»ή“Κ±δ≥…Κλ…ΪΘ§±μΟς―ΈΥα“―Ψ≠ΙΐΝΩ |
3.(10’ρΫ≠)18Θ°œ¬Ν–ΗςΉι»ή“ΚΘ§≤ΜΦ”ΤδΥϋ ‘ΦΝΨΆΡήΦχ±πΒΡ «
AΘ°NaOHΓΔNaClΓΔMgCl2ΓΔFeCl3ΓΓΓΓΓΓ ΓΓΓΓBΘ°Na2CO3ΓΔœΓH2SO4ΓΔœΓHClΓΔNaNO3ΓΓΓΓΓΓΓΓ
CΘ°Na2SO4ΓΔBaCl2ΓΔKNO3ΓΔNaCl ΓΓΓΓΓΓDΘ°K2SO4ΓΔNa2CO3ΓΔBaCl2ΓΔœΓHNO3
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com