
题目列表(包括答案和解析)
10.镁、铁在日常生活中都有广泛的用途,如:
(1)镁在空气中燃烧时能发出耀眼的白光,可用来制造镁闪光灯,其反应的化学方程式是
___________________________________________。
(2)市场上出售的补血麦片中含有微量颗粒细小的还原铁粉,铁粉与人体胃液中的盐酸反应,起到补血的作用,写出这个反应的化学方程式:___________________________________。
思路解析:物质的用途取决于物质的性质。根据性质判断物质为什么这样用。
答案:(1)2Mg+O2 2MgO
2MgO
(2)Fe+2HCl====FeCl2+H2↑
9.从考古文物出土情况来看,金器保存完好,铜器表面会生锈,铁器几乎保存不了,锈迹斑斑或者烂掉,说明金、铜、铁的活泼性顺序是______________________________________。
思路解析:金属保存的越完好,说明化学性质越稳定。金是化学性质很稳定的金属,很难和其他物质发生化学反应,所以保存完好。铜的化学性质比较稳定,但也会锈蚀。铁的化学性质比较活泼,在潮湿的地下,很容易锈蚀。
答案:金<铜<铁
8.下列说法是否正确?在括号中用“√”表示正确,用“×”表示错误。
(1)可以用铁罐贮运稀硫酸。( )
(2)铁的导电性比铜的导电性强。( )
(3)铝能制成很薄的铝箔是由于铝具有良好的延展性。( )
思路解析:本题考查金属的基本性质,并根据基本性质判断金属的用途。(1)铁可与稀硫酸反应,故不可以用来盛放、运输稀硫酸;(2)铁的导电性比铜的差,属于金属物理性质的考查;(3)铝具有很好的延展性,可以压成很薄的铝箔或者拉制成电缆。
答案:(1)× (2)× (3)√
我综合 我发展
7.铁在常温下与氧气反应生成氧化铁(Fe2O3),在氧气中点燃,生成四氧化三铁(Fe3O4)。说明反应条件不同,可能会导致反应产物不一样。请你举出其他由于反应条件不同导致反应产物不一样的化学反应的例子。
思路解析:本题考查反应条件对化学反应的影响。可以寻找生活中常见的一些例子,如碳的不充分燃烧可以引起煤气中毒,而碳在氧气充足的条件下反应生成CO2。
答案:如C在充足的氧气中燃烧,生成CO2;在氧气不足时,生成CO。
6.写出下列变化的化学反应方程式。
(1)用砂纸打磨过的铝片放置在空气中:__________________________________________。
(2)铁钉在稀硫酸溶液中:_____________________________________________________。
(3)铁丝浸泡在硫酸铜溶液中:_________________________________________________。
思路解析:本题考查金属铁的化学性质,可以与稀酸等发生置换反应,再者,铝在空气中容易被氧化。
答案:(1)4Al+3O2 2Al2O3
(2)Fe+H2SO4====FeSO4+H2↑ (3)Fe+CuSO4====FeSO4+Cu
2Al2O3
(2)Fe+H2SO4====FeSO4+H2↑ (3)Fe+CuSO4====FeSO4+Cu
5.镁带在耐高温的容器中密封(内含空气)加热,在图8-1中能正确表示容器里所盛的物质总质量的是( )
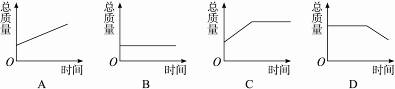
图8-1
思路解析:镁带与空气中的氧气反应,生成氧化镁,但化学反应遵循质量守恒定律,即使氧气消耗,体系的总质量不发生变化。因此该曲线应该是不变化的。
答案:B
4.面对纷繁复杂的化学变化,如果我们逐个进行学习和研究,时间上不允许,同时也不便于寻找规律,因此有必要对化学反应进行分类学习。下列反应属于置换反应类型的是( )
A.Zn+H2SO4====ZnSO4+H2↑
B.3Fe+2O2 Fe3O4
Fe3O4
C.CH4+2O2 CO2+2H2O
D.2HgO
CO2+2H2O
D.2HgO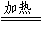 2Hg+O2↑
2Hg+O2↑
思路解析:置换反应的特征是单质和化合物反应生成新的单质和新的化合物。要注意反应物和生成物的单质和化合物各一种。A符合。
答案:A
3.铝是生活中最为常见的金属之一。关于铝的“自我保护”能力极强的原因,这一问题引起了同学们的极大兴趣,纷纷提出自己的看法:①铝的化学性质本来不活泼,难被腐蚀;②市场上的铝材料通常是铝合金,合金是不发生化学反应的;③铝性质活泼,表面能产生一层结构致密的氧化膜。你所认同的是( )
A.① B.② C.③ D.①②③
思路解析:①错误,因为铝的化学性质很活泼;②错误,合金同样发生化学反应,但合金的机械性能优于纯金属;③正确,由于铝与氧气生成了一层致密的氧化物保护膜,所以铝的性质虽然活泼,但不易被腐蚀。
答案:C
2.下列化学方程式正确的是( )
A.2Fe+6HCl====2FeCl3+3H2↑
B.CO2+Ca(OH)2====CaCO3↓+H2O
C.CaCO3+HCl====CaCl+CO2↑+H2O
D.Mg+O2 MgO
MgO
思路解析:A.铁与盐酸反应,生成的是FeCl2而不是FeCl3;C.CaCO3和稀HCl反应生成CaCl2、CO2、H2O,而不是CaCl;D.方程式Mg+O2 MgO没有配平。
MgO没有配平。
答案:B
1.下列各组物质在常温下能发生反应的是( )
A.铝和硫酸镁 B.锌和水 C.铜和稀硫酸 D.锌和硝酸汞
思路解析:铝不如镁活泼,故硫酸镁和铝不发生反应;锌与冷水和热水都不反应;铜和稀硫酸不反应,因为铜在金属活动顺序表中位于H之后;锌比汞活泼,可以从含汞的化合物溶液中置换出单质汞。
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com