
题目列表(包括答案和解析)
1.某些花岗岩石材中含有放射性元素氡。一种氡原子的质子数为86,中子数为136,这种氡原子核外电子数为( )
A.50 B.86 C.136 D.222
思路解析:此题考查对原子结构以及原子结构中粒子数之间等量关系的理解程度,解此题的关键在于掌握原子结构中的等量关系。即核电荷数 =质子数 =电子数(电荷等量关系),相对原子质量 =质子数+中子数(质量等量关系)。由题意,氡元素的质子数为86,则原子核外电子数为86;又由于中子数为136,则相对原子质量为222。
答案:B
9.在下列示意图表示的粒子中,属于原子的有(用序号填空,下同)________,属于阴离子的有________,属于阳离子的有________,属于同种元素的有________,达到稳定结构的有________,具有相同的电子层结构的是________。
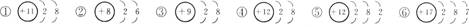
通过以上各图还可总结出,原子和离子的区别在于:
(1)________________________________________________________________。
(2)________________________________________________________________。
(3)________________________________________________________________。
思路解析:同种元素的粒子,质子数必相同。由于原子呈电中性,对阳离子而言,核电荷数必大于核外电子数。问题的关键是如何找出原子和离子的区别,可以从质子数与核外电子的关系、粒子的带电性等方面加以考虑。
答案:②⑤⑥ ③ ①④ ④⑤ ①③④⑥ ?①③④
(1)原子整体上不显电性,离子显电性
(2)原子中质子数等于电子数,离子中质子数不等于电子数
(3)离子的最外层电子数一般是8电子(只有一个电子层时为2电子)的相对稳定结构,原子中除稀有气体外,其余的一般不是相对稳定结构
8.元素Z的核电荷数为8,阴离子Z2-与元素Y的阳离子Y3+的电子层结构相同,则元素Y的核电荷数是_________。
思路解析:离子是由原子失去或得到电子而形成的,且离子所带的电荷数等于原子形成离子时失去或得到的电子的数目,又Z2-的核外电子数为8+2=10,设Y的核电荷数为b,则Y3+核外电子数为b-3,又Z2-与Y3+电子层结构相同,则8+2=b-3,因此b=8+2+3=13。
答案:13
我创新 我超越
7.根据粒子结构示意图给出的信息,下列说法正确的是( )

A.①②③表示的是三个原子 B.③表示的元素是非金属元素
C.①③表示的是阳离子 D.①②表示的元素化学性质相似
思路解析:此题根据粒子结构示意图,判断元素种类、粒子种类、元素的性质以及结构的稳定性。解题的关键在于:
(1)由质子数和电子数的差值判断粒子种类(原子、阳离子、阴离子),①②为原子,而③为阳离子。
(2)由核内质子数决定元素种类,核内质子数不同,则表示不同元素。
(3)由原子最外层电子数决定元素的性质,①②为非金属元素,③为金属元素。且最外层电子数相同,性质相似,如①②元素化学性质相似。
(4)由最外层电子数决定粒子结构的稳定性。一般最外层电子数为8的结构称为“8电子稳定结构”。
答案:D
6.某粒子由12个质子、12个中子和10个电子构成,该粒子是( )
A.分子 B.原子 C.阴离子 D.阳离子
思路解析:此题考查由粒子中质子数、电子数的关系去判断粒子种类的能力。解此题的关键在于要明确判断粒子种类(分子、原子、阴离子、阳离子)的依据是粒子中质子数和电子数的大小。当质子数=电子数时,呈中性,为分子、原子;当质子数>电子数时,带正电荷,为阳离子;当质子数<电子数时,带负电,为阴离子。
答案:D
5.已知几种离子或原子的结构、带电情况如下表所示。通过此表可以总结出:带负电荷的原子属于阴离子。还能总结出:
|
粒子结构示意图 |
 |
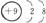 |
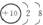 |
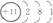 |
 |
|
粒子类型 |
阴离子 |
阴离子 |
原子 |
阳离子 |
阳离子 |
|
粒子所带电荷 |
2个单位负电荷 |
1个单位负电荷 |
不带电 |
1个单位正电荷 |
2个单位正电荷 |
(1)________________________________________________________________。
(2)________________________________________________________________。
思路解析:可以从多个角度来分析,如最外层电子数、质子数与核外电子数的关系,离子类型与所带电荷的关系,核外电子的排布规律等。
答案:(1)带正电荷的原子属于阳离子
(2)最外层为稳定结构的粒子不一定是中性原子
(3)核电荷数大于电子总数的原子带正电荷
(4)第一电子层最多能容纳2个电子
(5)离子所带电荷与原子得失电子的数目有关
我综合 我发展
4.1个氢原子由一个质子和一个电子构成,不含中子,当一个氢原子失去1个电子后,它不会变成( )
A.质子 B.原子核 C.阳离子 D.带负电的离子
思路解析:本题经过仔细分析不难得出,一个氢原子失去一个电子后,就变成了一个质子,带一个单位的正电荷。
答案:D
3.对于钠原子和钠离子两种粒子的比较,下列说法不正确的是( )
A.它们的电子数相同 B.它们的化学性质不相同
C.它们的质子数相同 D.它们都是构成物质的粒子
思路解析:钠离子是由钠原子失去最外层的一个电子而形成的,在此过程中,钠原子失去最外层的一个电子,电子数变了,化学性质也不相同,但质子数不变。
答案:A
2.元素的化学性质主要取决于( )
A.核外电子数 B.核电荷数 C.中子数 D.最外层电子数
思路解析:原子的结构都有一个达到稳定结构的趋势,只有通过得失电子使最外层达到一个稳定结构,所以元素的化学性质主要表现在原子最外层电子的得失上。
答案:D
1.镁原子与镁离子比较具有相同的_________,它们的不同之处有_________。
思路解析:原子得失电子变成离子,所以原子与离子之间只是电子数不同,质子数没有发生变化。
答案:质子数(核电荷数) 电子数
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com